 II. Трансферазы. а) п/кл фосфотрансферазы. Все трансферазы переносят функционольные группы. Фосфотрансферазы катализируют перенос фосфатной группы. Коферментом является АТФ. В этой молекуле остатки фосфорной кислоты связаны между собой макроэргической связью. Кроме АТФ могут учавствовать молекулы ЦТФ, ГТФ, УТФ. б) п/кл аминотрансферазы. Ферменты отвечают за перенос аминогрупп. Коферментом является передоксильфосфат, является производным пиридоксина витамина В6. в) п/кл ацилтрансферазы. Переносят остатки органических кислот. Коферментом является кофермент А, производное пантотеновой кислоты. г) п/кл переносящие одноуглеродные группы(СН, СН3). Коферментом является тетрагидрофолиевая кислота, производная витамина фолиевая кислота.
II. Трансферазы. а) п/кл фосфотрансферазы. Все трансферазы переносят функционольные группы. Фосфотрансферазы катализируют перенос фосфатной группы. Коферментом является АТФ. В этой молекуле остатки фосфорной кислоты связаны между собой макроэргической связью. Кроме АТФ могут учавствовать молекулы ЦТФ, ГТФ, УТФ. б) п/кл аминотрансферазы. Ферменты отвечают за перенос аминогрупп. Коферментом является передоксильфосфат, является производным пиридоксина витамина В6. в) п/кл ацилтрансферазы. Переносят остатки органических кислот. Коферментом является кофермент А, производное пантотеновой кислоты. г) п/кл переносящие одноуглеродные группы(СН, СН3). Коферментом является тетрагидрофолиевая кислота, производная витамина фолиевая кислота.
 III. Гидролазы. Ферменты, катализирующие расщепление веществ с участием воды. Они не нуждаются в коферментах. IV. Лиазы. Ферменты, катализирующие присоединение веществ по двойным связям. V. Изомеразы. Катализируют внутримолекулярные перегруппировки. Имеют окончание –изомераза или –мутаза. Могут осуществлять рацимизацию, транс-,цисизомеризацию, внутримолекулярный перенос функциональных групп. Коферментом является цианкобаламин производное витамина В12. VI. Лигазы = синтетазы. Ферменты, осуществляющие энергозависимый синтез. Поставщиком обычно является внутриклеточный пирофосфат(АТФ, АДФ).
III. Гидролазы. Ферменты, катализирующие расщепление веществ с участием воды. Они не нуждаются в коферментах. IV. Лиазы. Ферменты, катализирующие присоединение веществ по двойным связям. V. Изомеразы. Катализируют внутримолекулярные перегруппировки. Имеют окончание –изомераза или –мутаза. Могут осуществлять рацимизацию, транс-,цисизомеризацию, внутримолекулярный перенос функциональных групп. Коферментом является цианкобаламин производное витамина В12. VI. Лигазы = синтетазы. Ферменты, осуществляющие энергозависимый синтез. Поставщиком обычно является внутриклеточный пирофосфат(АТФ, АДФ).
 Механизм действия ферментов Биологический ферментативный катализ является примером каталитического процесса и для него выполняются все законы. Классические катализаторы действуют за счет энергии активации. Энергия активации энергия, необходимая молекуле вещества для преодоления энергетического барьера. Катализаторы не меняют G они снижают энергию активации. Снижение энергии активации увеличивает количество молекул, способных преодолеть энергетический барьер реакции и происходит это не линейно, не пропорционально.
Механизм действия ферментов Биологический ферментативный катализ является примером каталитического процесса и для него выполняются все законы. Классические катализаторы действуют за счет энергии активации. Энергия активации энергия, необходимая молекуле вещества для преодоления энергетического барьера. Катализаторы не меняют G они снижают энергию активации. Снижение энергии активации увеличивает количество молекул, способных преодолеть энергетический барьер реакции и происходит это не линейно, не пропорционально.
 Снижение энергии активации достигается за счет: 1. ориентации субстратов. 2. Теория стерического взаимодействия (взаимодействие ключ-замок). Фишер предположил, что активный центр фермента пространственно соответствует молекуле субстрата. За счет своей пространственной специфичности фермент и субстрат ориентируются специфично.
Снижение энергии активации достигается за счет: 1. ориентации субстратов. 2. Теория стерического взаимодействия (взаимодействие ключ-замок). Фишер предположил, что активный центр фермента пространственно соответствует молекуле субстрата. За счет своей пространственной специфичности фермент и субстрат ориентируются специфично.
 3. теория индуцированного соответствия. Предложил Кошланд. После образования комплекса фермент-субстрат, в молекуле фермента могут наблюдаться некие конформационные изменения, которые индуцируют соответствующие изменения в молекуле субстрата.
3. теория индуцированного соответствия. Предложил Кошланд. После образования комплекса фермент-субстрат, в молекуле фермента могут наблюдаться некие конформационные изменения, которые индуцируют соответствующие изменения в молекуле субстрата.
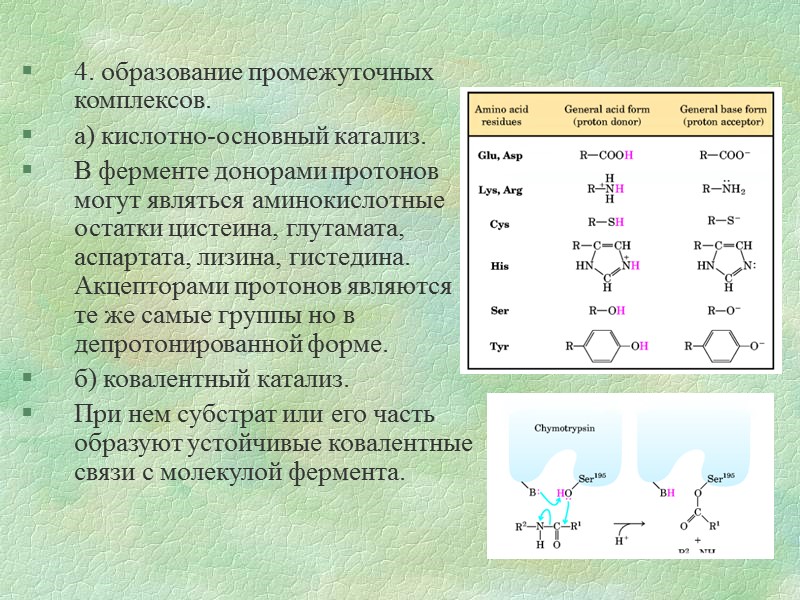
 4. образование промежуточных комплексов. а) кислотно-основный катализ. В ферменте донорами протонов могут являться аминокислотные остатки цистеина, глутамата, аспартата, лизина, гистедина. Акцепторами протонов являются те же самые группы но в депротонированной форме. б) ковалентный катализ. При нем субстрат или его часть образуют устойчивые ковалентные связи с молекулой фермента.
4. образование промежуточных комплексов. а) кислотно-основный катализ. В ферменте донорами протонов могут являться аминокислотные остатки цистеина, глутамата, аспартата, лизина, гистедина. Акцепторами протонов являются те же самые группы но в депротонированной форме. б) ковалентный катализ. При нем субстрат или его часть образуют устойчивые ковалентные связи с молекулой фермента.
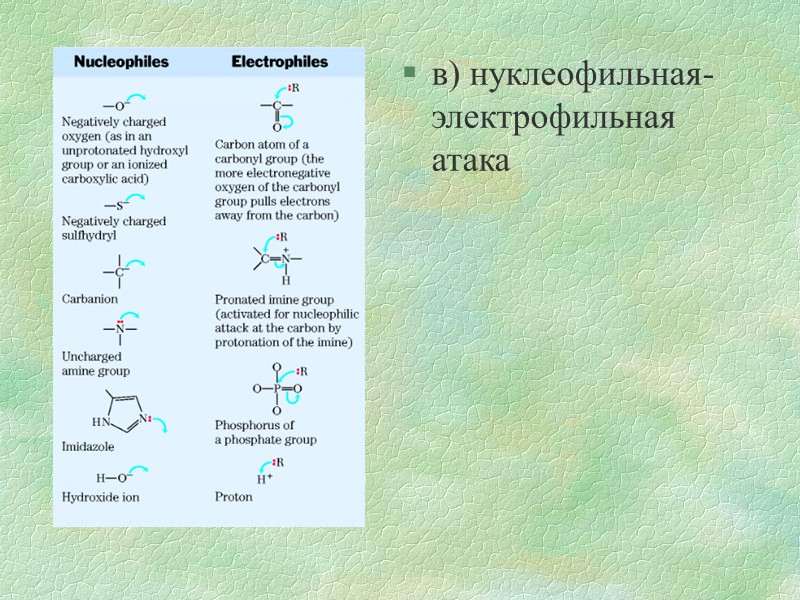
 в) нуклеофильная-электрофильная атака
в) нуклеофильная-электрофильная атака
 Факторы, влияющие на активность фермента Концентрация субстрата. В 1913г. Михаэлис и Ментен проедложили уравнение = max[S]/Km+[S]
Факторы, влияющие на активность фермента Концентрация субстрата. В 1913г. Михаэлис и Ментен проедложили уравнение = max[S]/Km+[S]
 Km - константа Михаэлиса. Лимитирующим фактором протекания реакции, является образование фермент-субстратного комплекса. Km= концентрации субстрата при которой скорость реакции равна ½ скорости максимальной. Т.к. это концентрация, то она выражается моль/литр и тп. Уравнение Михаэлиса-Ментен описявает односубстратные не аллостерические ферменты.
Km - константа Михаэлиса. Лимитирующим фактором протекания реакции, является образование фермент-субстратного комплекса. Km= концентрации субстрата при которой скорость реакции равна ½ скорости максимальной. Т.к. это концентрация, то она выражается моль/литр и тп. Уравнение Михаэлиса-Ментен описявает односубстратные не аллостерические ферменты.
 Уравнение Лайнуивера-Берка
Уравнение Лайнуивера-Берка

























