2323b5078223fa3d60547b6e38e22a42.ppt
- Количество слайдов: 85
 HEMATOLOJİK MALİGNİTELERDE GÜNCEL TEDAVİLER Dr Selami K Toprak 2017
HEMATOLOJİK MALİGNİTELERDE GÜNCEL TEDAVİLER Dr Selami K Toprak 2017


 www. kokhucredernegi. org. tr 4
www. kokhucredernegi. org. tr 4







 13
13








 Otolog Kök Hücre Transplantasyonunda Son Gelişmeler
Otolog Kök Hücre Transplantasyonunda Son Gelişmeler
 AJANDA Kök hücre transplantasyonu gelişimi Periferik kök hücre mobilizasyonu ve rejimler Plerixafor ve klinik geliştirme Predict Çalışması Mobilizasyon başarısızlıkları EBMT mobilizasyon yaklaşımı Sonuçlar | 26
AJANDA Kök hücre transplantasyonu gelişimi Periferik kök hücre mobilizasyonu ve rejimler Plerixafor ve klinik geliştirme Predict Çalışması Mobilizasyon başarısızlıkları EBMT mobilizasyon yaklaşımı Sonuçlar | 26
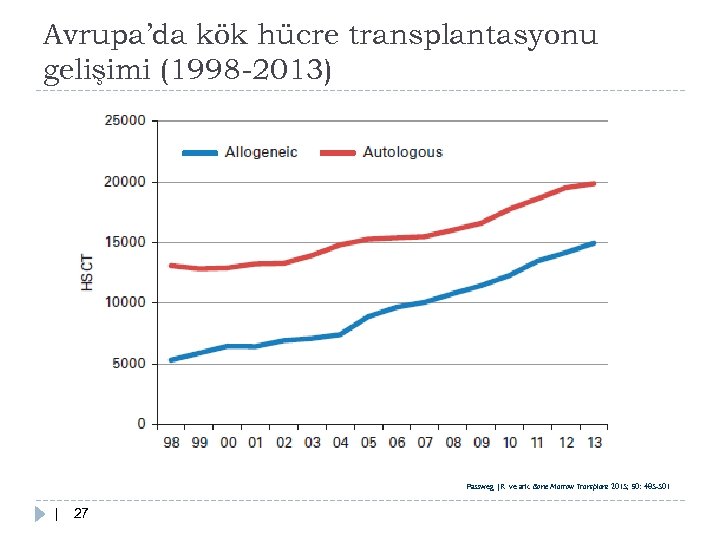 Avrupa’da kök hücre transplantasyonu gelişimi (1998 -2013) Passweg JR ve ark. Bone Marrow Transplant 2015; 50: 485 -501 | 27
Avrupa’da kök hücre transplantasyonu gelişimi (1998 -2013) Passweg JR ve ark. Bone Marrow Transplant 2015; 50: 485 -501 | 27
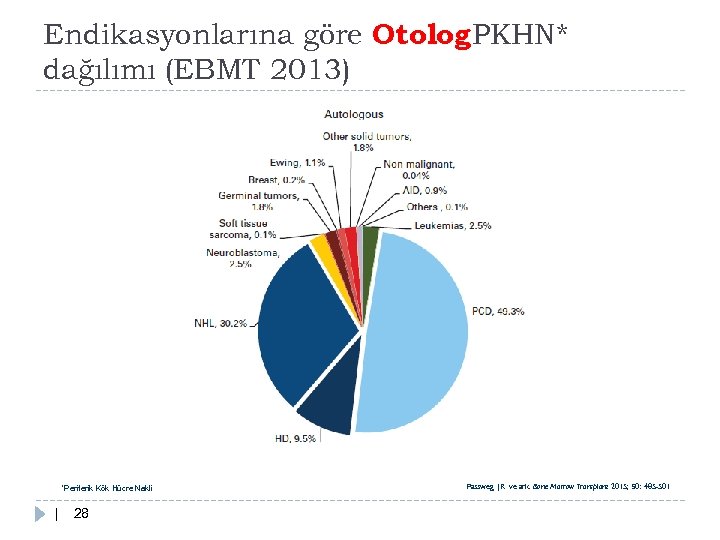 Endikasyonlarına göre Otolog PKHN* dağılımı (EBMT 2013) *Periferik Kök Hücre Nakli | 28 Passweg JR ve ark. Bone Marrow Transplant 2015; 50: 485 -501
Endikasyonlarına göre Otolog PKHN* dağılımı (EBMT 2013) *Periferik Kök Hücre Nakli | 28 Passweg JR ve ark. Bone Marrow Transplant 2015; 50: 485 -501
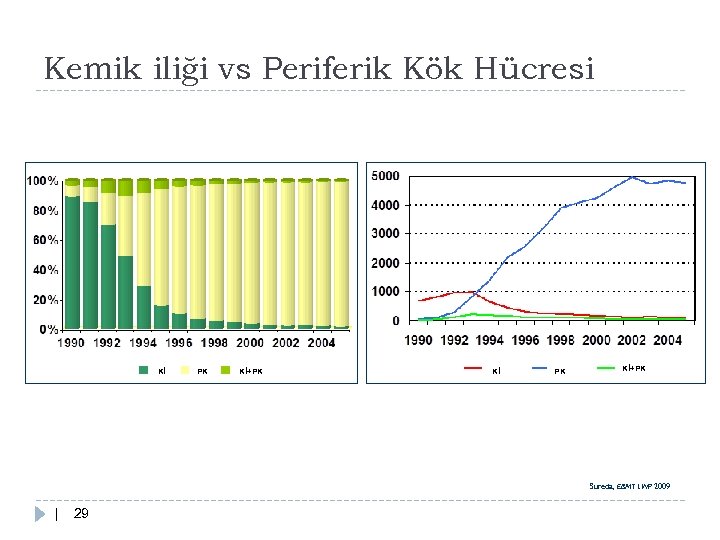 Kemik iliği vs Periferik Kök Hücresi Kİ PK Kİ+PK Sureda, EBMT LWP 2009 | 29
Kemik iliği vs Periferik Kök Hücresi Kİ PK Kİ+PK Sureda, EBMT LWP 2009 | 29
 Periferik kök hücre mobilizasyonunda en sık kullanılan ajanlar ● Hematopoetik büyüme faktörleri ● G-CSF + GM-CSF ● Pegfilgrastim ● Kemoterapi ● Siklofosfamid, etoposid, melfalan ● Hastalığa özel rejimler (ICE, RICE, IVE) ● Kemoterapi + G-CSF ● Plerixafor + G-CSF ICE: İfosfamid, karboplatin, etoposid; RICE: Rituximab, ifosfamid, karboplatin, etoposid; IVE: İfosfamid, epirubisin, etoposid | 30 1 Hacıoğlu, Sarı, Altuntaş Periferik Kök Hücre Mobilizasyonu 2 Smith TJ, ve ark. J Clin Oncol. 2006; 24: 3187 -3205. 3. Leukine® [prescribing information]. Sanofi-Aventis US LLC, 2012. 3. Mozobil™ [prescribing information]. Cambridge, MA: Genzyme Corp; 2010. 4. Lemoli RM, ve ark. Haematologica. 2008; 93: 321 -324. 5. Hicks ML, ve ark. Transfusion. 47; 2007: 629 -635.
Periferik kök hücre mobilizasyonunda en sık kullanılan ajanlar ● Hematopoetik büyüme faktörleri ● G-CSF + GM-CSF ● Pegfilgrastim ● Kemoterapi ● Siklofosfamid, etoposid, melfalan ● Hastalığa özel rejimler (ICE, RICE, IVE) ● Kemoterapi + G-CSF ● Plerixafor + G-CSF ICE: İfosfamid, karboplatin, etoposid; RICE: Rituximab, ifosfamid, karboplatin, etoposid; IVE: İfosfamid, epirubisin, etoposid | 30 1 Hacıoğlu, Sarı, Altuntaş Periferik Kök Hücre Mobilizasyonu 2 Smith TJ, ve ark. J Clin Oncol. 2006; 24: 3187 -3205. 3. Leukine® [prescribing information]. Sanofi-Aventis US LLC, 2012. 3. Mozobil™ [prescribing information]. Cambridge, MA: Genzyme Corp; 2010. 4. Lemoli RM, ve ark. Haematologica. 2008; 93: 321 -324. 5. Hicks ML, ve ark. Transfusion. 47; 2007: 629 -635.
 Kök hücre mobilizasyonunu etkileyen değişkenler Hasta popülasyonunda farklılıklar Farklı kemoterapi tedavileri Cihaz farklılıkları Teknik farklılıklar Farklı araştırma protokolleri Uygulayıcılar arası farklılıklar Hasta toleransı | 31
Kök hücre mobilizasyonunu etkileyen değişkenler Hasta popülasyonunda farklılıklar Farklı kemoterapi tedavileri Cihaz farklılıkları Teknik farklılıklar Farklı araştırma protokolleri Uygulayıcılar arası farklılıklar Hasta toleransı | 31
 Mobilizasyon başarısına etki eden faktörler ● ● Yaş (>60 yaş) Hastalık ● Primer hastalık: Lenfoma hastaları (%20 -40) ● Refrakter hastalık ● İleri devre hastalık ● Önceki kemoterapiler ● Sayı: Kür sayısı ile artan risk (>4 kür) ● Tipi: ● ● ● ● Alkilleyici ajanlar (melfalan vb) Mobilizasyondan 2 ay önce fludarabin tedavisi Mobilizasyon öncesi lenalidomit kullanımı (>4 kür) Kemik iliği tutulumu Kemik iliği alanlarına radyoterapi Trombositopeni Mobilizasyon öncesi PK CD 34+ hücre sayısı düşüklüğü Kemo-mobilizasyon sonrası nötrofil iyileşme süresinde gecikme Hacıoğlu, Sarı, Altuntaş Periferik Kök Hücre Mobilizasyonu | 32
Mobilizasyon başarısına etki eden faktörler ● ● Yaş (>60 yaş) Hastalık ● Primer hastalık: Lenfoma hastaları (%20 -40) ● Refrakter hastalık ● İleri devre hastalık ● Önceki kemoterapiler ● Sayı: Kür sayısı ile artan risk (>4 kür) ● Tipi: ● ● ● ● Alkilleyici ajanlar (melfalan vb) Mobilizasyondan 2 ay önce fludarabin tedavisi Mobilizasyon öncesi lenalidomit kullanımı (>4 kür) Kemik iliği tutulumu Kemik iliği alanlarına radyoterapi Trombositopeni Mobilizasyon öncesi PK CD 34+ hücre sayısı düşüklüğü Kemo-mobilizasyon sonrası nötrofil iyileşme süresinde gecikme Hacıoğlu, Sarı, Altuntaş Periferik Kök Hücre Mobilizasyonu | 32
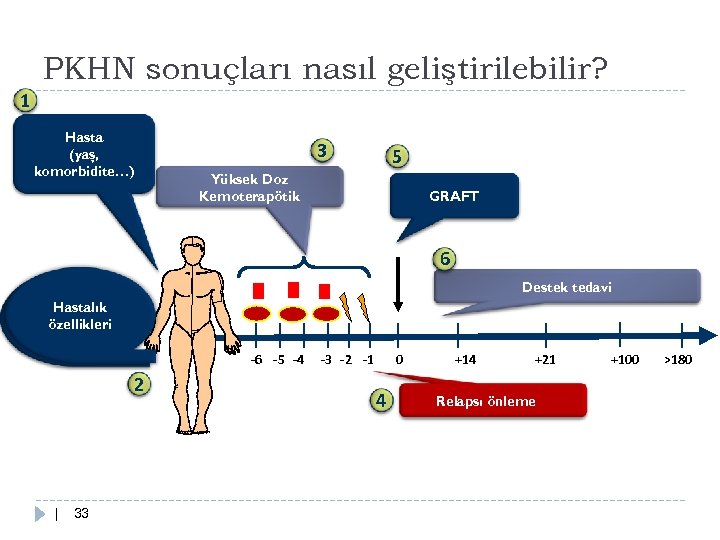 PKHN sonuçları nasıl geliştirilebilir? 1 Hasta (yaş, komorbidite…) 3 5 Yüksek Doz Kemoterapötik GRAFT 6 Destek tedavi Hastalık Disease özellikleri features -6 -5 -4 2 | 33 -3 -2 -1 0 4 +14 +21 Relapsı önleme +100 >180
PKHN sonuçları nasıl geliştirilebilir? 1 Hasta (yaş, komorbidite…) 3 5 Yüksek Doz Kemoterapötik GRAFT 6 Destek tedavi Hastalık Disease özellikleri features -6 -5 -4 2 | 33 -3 -2 -1 0 4 +14 +21 Relapsı önleme +100 >180
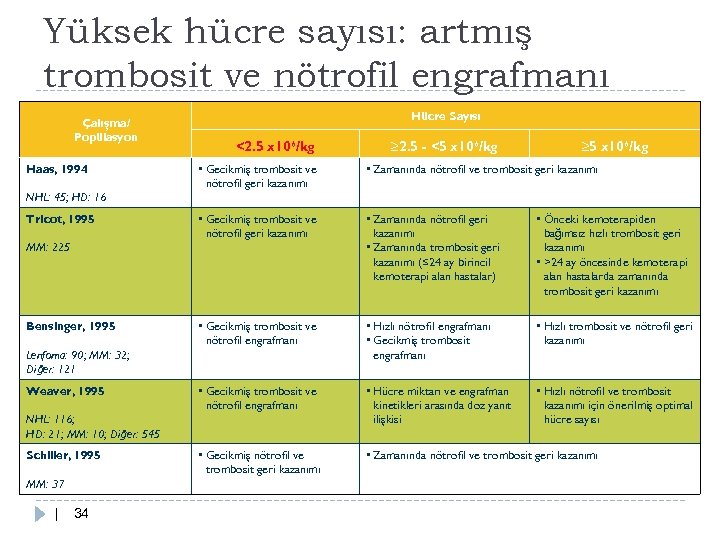 Yüksek hücre sayısı: artmış trombosit ve nötrofil engrafmanı Çalışma/ Popülasyon Haas, 1994 Hücre Sayısı <2. 5 x 106/kg ≥ 2. 5 - <5 x 106/kg ≥ 5 x 106/kg • Gecikmiş trombosit ve nötrofil geri kazanımı • Zamanında nötrofil ve trombosit geri kazanımı • Gecikmiş trombosit ve nötrofil geri kazanımı • Zamanında nötrofil geri kazanımı • Zamanında trombosit geri kazanımı (≤ 24 ay birincil kemoterapi alan hastalar) • Önceki kemoterapiden bağımsız hızlı trombosit geri kazanımı • >24 ay öncesinde kemoterapi alan hastalarda zamanında trombosit geri kazanımı • Gecikmiş trombosit ve nötrofil engrafmanı • Hızlı nötrofil engrafmanı • Gecikmiş trombosit engrafmanı • Hızlı trombosit ve nötrofil geri kazanımı • Gecikmiş trombosit ve nötrofil engrafmanı • Hücre miktarı ve engrafman kinetikleri arasında doz yanıt ilişkisi • Hızlı nötrofil ve trombosit kazanımı için önerilmiş optimal hücre sayısı • Gecikmiş nötrofil ve trombosit geri kazanımı • Zamanında nötrofil ve trombosit geri kazanımı NHL: 45; HD: 16 Tricot, 1995 MM: 225 Bensinger, 1995 Lenfoma: 90; MM: 32; Diğer: 121 Weaver, 1995 NHL: 116; HD: 21; MM: 10; Diğer: 545 Schiller, 1995 MM: 37 | 34
Yüksek hücre sayısı: artmış trombosit ve nötrofil engrafmanı Çalışma/ Popülasyon Haas, 1994 Hücre Sayısı <2. 5 x 106/kg ≥ 2. 5 - <5 x 106/kg ≥ 5 x 106/kg • Gecikmiş trombosit ve nötrofil geri kazanımı • Zamanında nötrofil ve trombosit geri kazanımı • Gecikmiş trombosit ve nötrofil geri kazanımı • Zamanında nötrofil geri kazanımı • Zamanında trombosit geri kazanımı (≤ 24 ay birincil kemoterapi alan hastalar) • Önceki kemoterapiden bağımsız hızlı trombosit geri kazanımı • >24 ay öncesinde kemoterapi alan hastalarda zamanında trombosit geri kazanımı • Gecikmiş trombosit ve nötrofil engrafmanı • Hızlı nötrofil engrafmanı • Gecikmiş trombosit engrafmanı • Hızlı trombosit ve nötrofil geri kazanımı • Gecikmiş trombosit ve nötrofil engrafmanı • Hücre miktarı ve engrafman kinetikleri arasında doz yanıt ilişkisi • Hızlı nötrofil ve trombosit kazanımı için önerilmiş optimal hücre sayısı • Gecikmiş nötrofil ve trombosit geri kazanımı • Zamanında nötrofil ve trombosit geri kazanımı NHL: 45; HD: 16 Tricot, 1995 MM: 225 Bensinger, 1995 Lenfoma: 90; MM: 32; Diğer: 121 Weaver, 1995 NHL: 116; HD: 21; MM: 10; Diğer: 545 Schiller, 1995 MM: 37 | 34
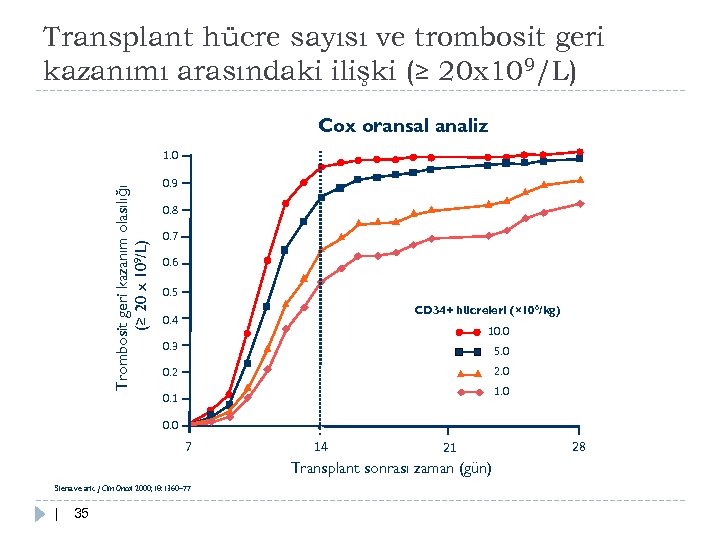 Transplant hücre sayısı ve trombosit geri kazanımı arasındaki ilişki (≥ 20 x 109/L) Cox oransal analiz Trombosit geri kazanım olasılığı (≥ 20 x 109/L) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 CD 34+ hücreleri (× 106/kg) 0. 4 10. 0 0. 3 5. 0 0. 2 2. 0 1. 0 0. 1 0. 0 7 14 21 Transplant sonrası zaman (gün) Siena ve ark. J Clin Oncol 2000; 18: 1360– 77 | 35 28
Transplant hücre sayısı ve trombosit geri kazanımı arasındaki ilişki (≥ 20 x 109/L) Cox oransal analiz Trombosit geri kazanım olasılığı (≥ 20 x 109/L) 1. 0 0. 9 0. 8 0. 7 0. 6 0. 5 CD 34+ hücreleri (× 106/kg) 0. 4 10. 0 0. 3 5. 0 0. 2 2. 0 1. 0 0. 1 0. 0 7 14 21 Transplant sonrası zaman (gün) Siena ve ark. J Clin Oncol 2000; 18: 1360– 77 | 35 28
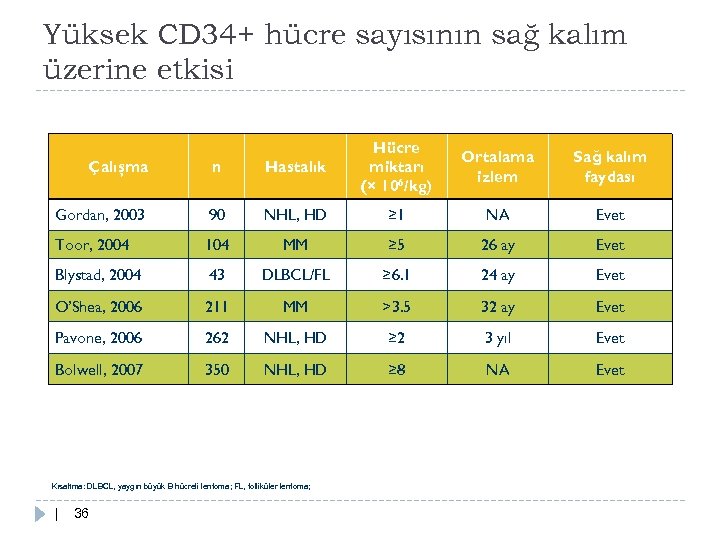 Yüksek CD 34+ hücre sayısının sağ kalım üzerine etkisi Çalışma n Hastalık Hücre miktarı (× 106/kg) Gordan, 2003 90 NHL, HD ≥ 1 NA Evet Toor, 2004 104 MM ≥ 5 26 ay Evet Blystad, 2004 43 DLBCL/FL ≥ 6. 1 24 ay Evet O’Shea, 2006 211 MM >3. 5 32 ay Evet Pavone, 2006 262 NHL, HD ≥ 2 3 yıl Evet Bolwell, 2007 350 NHL, HD ≥ 8 NA Evet Kısaltma: DLBCL, yaygın büyük B hücreli lenfoma; FL, folliküler lenfoma; | 36 Ortalama izlem Sağ kalım faydası
Yüksek CD 34+ hücre sayısının sağ kalım üzerine etkisi Çalışma n Hastalık Hücre miktarı (× 106/kg) Gordan, 2003 90 NHL, HD ≥ 1 NA Evet Toor, 2004 104 MM ≥ 5 26 ay Evet Blystad, 2004 43 DLBCL/FL ≥ 6. 1 24 ay Evet O’Shea, 2006 211 MM >3. 5 32 ay Evet Pavone, 2006 262 NHL, HD ≥ 2 3 yıl Evet Bolwell, 2007 350 NHL, HD ≥ 8 NA Evet Kısaltma: DLBCL, yaygın büyük B hücreli lenfoma; FL, folliküler lenfoma; | 36 Ortalama izlem Sağ kalım faydası
 Sonuçları nasıl geliştirebiliriz? Geliştirebilir miyiz? ● Mobilizasyon başarısızlıkları ● Graft kalitesini arttırmak ● Graft miktarı / içeriği ● Düşük toksisite / hastaneye yatış süresi ● Kemoterapi? ● Selektif mobilizasyon ● T hücreleri / NK hücreleri • Otolog transplant • Allojeneik transplant ● | Maliyet 37
Sonuçları nasıl geliştirebiliriz? Geliştirebilir miyiz? ● Mobilizasyon başarısızlıkları ● Graft kalitesini arttırmak ● Graft miktarı / içeriği ● Düşük toksisite / hastaneye yatış süresi ● Kemoterapi? ● Selektif mobilizasyon ● T hücreleri / NK hücreleri • Otolog transplant • Allojeneik transplant ● | Maliyet 37
 “… kemo-mobilizasyon ile görülen en yaygın advers olay febril nötropeni olup çalışmaların %43’ünde bildirilmiştir…” “Kemoterapinin kullanıldığı çalışmalarda, hastaların hastaneye başvurma oranı %20 -48 aralığındadır” Sheppard ve ark. ASBMT 2012; 18: 1191 -1203 | 38
“… kemo-mobilizasyon ile görülen en yaygın advers olay febril nötropeni olup çalışmaların %43’ünde bildirilmiştir…” “Kemoterapinin kullanıldığı çalışmalarda, hastaların hastaneye başvurma oranı %20 -48 aralığındadır” Sheppard ve ark. ASBMT 2012; 18: 1191 -1203 | 38
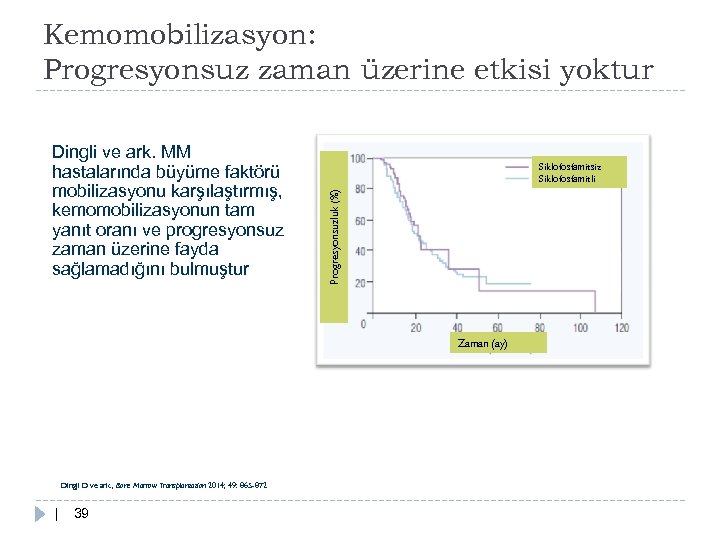 Kemomobilizasyon: Progresyonsuz zaman üzerine etkisi yoktur Siklofosfamitsiz Siklofosfamitli Progresyonsuzluk (%) Dingli ve ark. MM hastalarında büyüme faktörü mobilizasyonu karşılaştırmış, kemomobilizasyonun tam yanıt oranı ve progresyonsuz zaman üzerine fayda sağlamadığını bulmuştur Zaman (ay) Dingli D ve ark. , Bone Marrow Transplantation 2014; 49: 865 -872 | 39
Kemomobilizasyon: Progresyonsuz zaman üzerine etkisi yoktur Siklofosfamitsiz Siklofosfamitli Progresyonsuzluk (%) Dingli ve ark. MM hastalarında büyüme faktörü mobilizasyonu karşılaştırmış, kemomobilizasyonun tam yanıt oranı ve progresyonsuz zaman üzerine fayda sağlamadığını bulmuştur Zaman (ay) Dingli D ve ark. , Bone Marrow Transplantation 2014; 49: 865 -872 | 39
 «Mobilizasyon başarısızlığının» tanımlanmasındaki farklılıklar “Mobilizasyon başarısızlığı” tanımında ve mobilizasyon uygulamalarında belirgin farklılıklar vardır Periferal kan CD 34+ miktarı 10 hücre/µl’nin altında olan hastalar genellikle afereze gitmediklerinden başarısızlık olarak sayılmayabilirler | Hedef hücre sayısı farklı şekilde tanımlanabilir (optimal sayı) “Başarılı” mobilizasyon, önceki mobilizasyondan toplanan hücreler ile nakil olmuş hastaları içerebilir 40
«Mobilizasyon başarısızlığının» tanımlanmasındaki farklılıklar “Mobilizasyon başarısızlığı” tanımında ve mobilizasyon uygulamalarında belirgin farklılıklar vardır Periferal kan CD 34+ miktarı 10 hücre/µl’nin altında olan hastalar genellikle afereze gitmediklerinden başarısızlık olarak sayılmayabilirler | Hedef hücre sayısı farklı şekilde tanımlanabilir (optimal sayı) “Başarılı” mobilizasyon, önceki mobilizasyondan toplanan hücreler ile nakil olmuş hastaları içerebilir 40
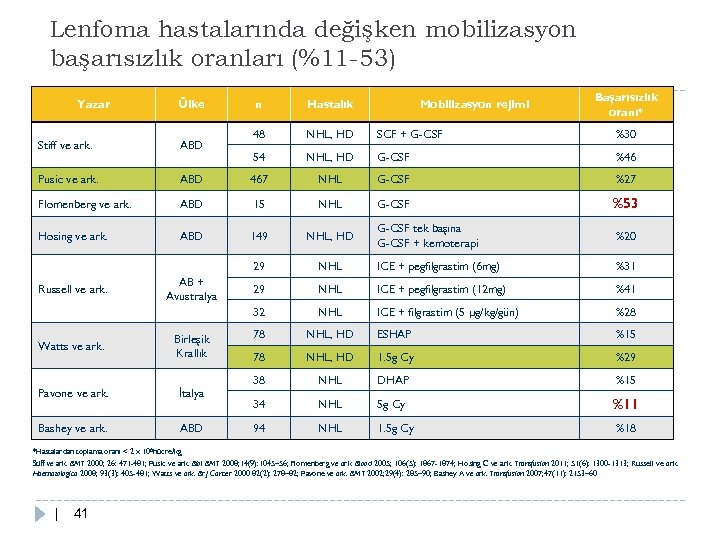 Lenfoma hastalarında değişken mobilizasyon başarısızlık oranları (%11 -53) Yazar Ülke Mobilizasyon rejimi Başarısızlık oranı* n Hastalık 48 NHL, HD SCF + G-CSF %30 54 NHL, HD G-CSF %46 Stiff ve ark. ABD Pusic ve ark. ABD 467 NHL G-CSF %27 Flomenberg ve ark. ABD 15 NHL G-CSF %53 Hosing ve ark. ABD 149 NHL, HD G-CSF tek başına G-CSF + kemoterapi %20 29 NHL ICE + pegfilgrastim (6 mg) %31 29 NHL ICE + pegfilgrastim (12 mg) %41 32 NHL ICE + filgrastim (5 µg/kg/gün) %28 78 NHL, HD ESHAP %15 78 NHL, HD 1. 5 g Cy %29 38 NHL DHAP %15 34 NHL 5 g Cy %11 94 NHL 1. 5 g Cy %18 Russell ve ark. Watts ve ark. AB + Avustralya Birleşik Krallık Pavone ve ark. İtalya Bashey ve ark. ABD *Hastalardan toplama oranı < 2 x 106 hücre/kg Stiff ve ark. BMT 2000; 26: 471 -481; Pusic ve ark. Biol BMT 2008; 14(9): 1045– 56; Flomenberg ve ark. Blood 2005; 106(5): 1867 -1874; Hosing C ve ark. Transfusion 2011; 51(6): 1300 -1313; Russell ve ark. Haematologica 2008; 93(3): 405 -481; Watts ve ark. Br J Cancer 2000 82(2): 278– 82; Pavone ve ark. BMT 2002; 29(4): 285– 90; Bashey A ve ark. Transfusion 2007; 47(11): 2153– 60 | 41
Lenfoma hastalarında değişken mobilizasyon başarısızlık oranları (%11 -53) Yazar Ülke Mobilizasyon rejimi Başarısızlık oranı* n Hastalık 48 NHL, HD SCF + G-CSF %30 54 NHL, HD G-CSF %46 Stiff ve ark. ABD Pusic ve ark. ABD 467 NHL G-CSF %27 Flomenberg ve ark. ABD 15 NHL G-CSF %53 Hosing ve ark. ABD 149 NHL, HD G-CSF tek başına G-CSF + kemoterapi %20 29 NHL ICE + pegfilgrastim (6 mg) %31 29 NHL ICE + pegfilgrastim (12 mg) %41 32 NHL ICE + filgrastim (5 µg/kg/gün) %28 78 NHL, HD ESHAP %15 78 NHL, HD 1. 5 g Cy %29 38 NHL DHAP %15 34 NHL 5 g Cy %11 94 NHL 1. 5 g Cy %18 Russell ve ark. Watts ve ark. AB + Avustralya Birleşik Krallık Pavone ve ark. İtalya Bashey ve ark. ABD *Hastalardan toplama oranı < 2 x 106 hücre/kg Stiff ve ark. BMT 2000; 26: 471 -481; Pusic ve ark. Biol BMT 2008; 14(9): 1045– 56; Flomenberg ve ark. Blood 2005; 106(5): 1867 -1874; Hosing C ve ark. Transfusion 2011; 51(6): 1300 -1313; Russell ve ark. Haematologica 2008; 93(3): 405 -481; Watts ve ark. Br J Cancer 2000 82(2): 278– 82; Pavone ve ark. BMT 2002; 29(4): 285– 90; Bashey A ve ark. Transfusion 2007; 47(11): 2153– 60 | 41
 Hata oranlarını etkileyen klinik uygulama farklılıkları G-CSF doz ve şeması Kemo-mobilizasyon süresince kemoterapinin dozu ve rejimi İşlenmiş kan hacmi İzin verilen maksimum aferez işlem sayısı Mobilizasyon sırasında hastalığın derecesi Aferezi başlatmak için kullanılan hematolojik parametreler (CD 34+ hücre sayısı, lökosit sayısı) | 42
Hata oranlarını etkileyen klinik uygulama farklılıkları G-CSF doz ve şeması Kemo-mobilizasyon süresince kemoterapinin dozu ve rejimi İşlenmiş kan hacmi İzin verilen maksimum aferez işlem sayısı Mobilizasyon sırasında hastalığın derecesi Aferezi başlatmak için kullanılan hematolojik parametreler (CD 34+ hücre sayısı, lökosit sayısı) | 42
 Plerixafor ve kök hücre mobilizasyonu | 43
Plerixafor ve kök hücre mobilizasyonu | 43
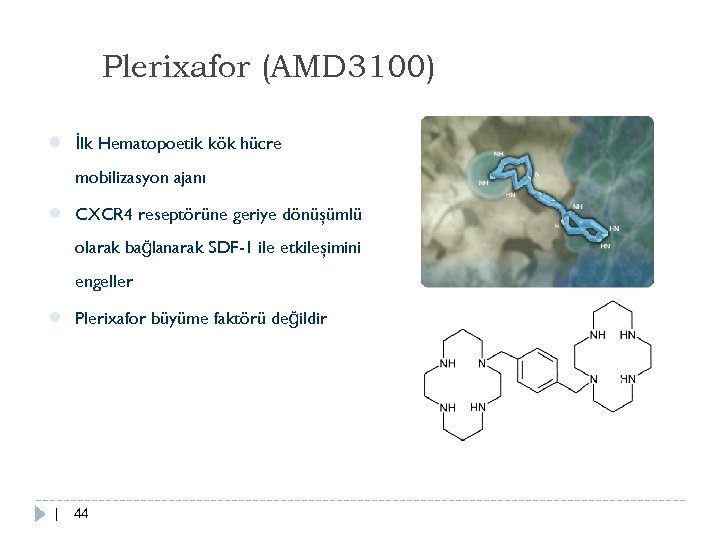 Plerixafor (AMD 3100) ● İlk Hematopoetik kök hücre mobilizasyon ajanı ● CXCR 4 reseptörüne geriye dönüşümlü olarak bağlanarak SDF-1 ile etkileşimini engeller ● | Plerixafor büyüme faktörü değildir 44
Plerixafor (AMD 3100) ● İlk Hematopoetik kök hücre mobilizasyon ajanı ● CXCR 4 reseptörüne geriye dönüşümlü olarak bağlanarak SDF-1 ile etkileşimini engeller ● | Plerixafor büyüme faktörü değildir 44
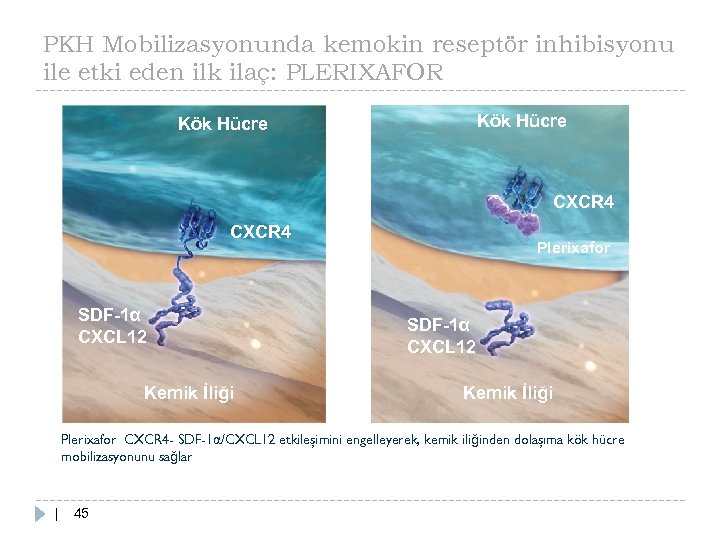 PKH Mobilizasyonunda kemokin reseptör inhibisyonu ile etki eden ilk ilaç: PLERIXAFOR Kök Hücre CXCR 4 SDF-1α CXCL 12 Kemik İliği Plerixafor CXCR 4 - SDF-1α/CXCL 12 etkileşimini engelleyerek, kemik iliğinden dolaşıma kök hücre mobilizasyonunu sağlar | 45
PKH Mobilizasyonunda kemokin reseptör inhibisyonu ile etki eden ilk ilaç: PLERIXAFOR Kök Hücre CXCR 4 SDF-1α CXCL 12 Kemik İliği Plerixafor CXCR 4 - SDF-1α/CXCL 12 etkileşimini engelleyerek, kemik iliğinden dolaşıma kök hücre mobilizasyonunu sağlar | 45
 Plerixafor keşfi ve geliştirilmesi 1991 -1992 HIV inhibitorü olarak sentez edildi 1996 -1997 HIV hücre içine giriş yapabilmesi için kemokin ko-reseptörüne ihtiyacı tanımlandı AMD 3100’ün CXCR 4’ün potent inhibitörü olduğu bulundu 1998 Sağlıklı gönüllülerde AMD 3100’ün ilk faz-I (mobilizasyon) çalışması başlatıldı 2001 2006 MM ve NHL hastalarında faz-III çalışmaları tamamlandı 2008 FDA onayı 2009 | MM ve NHL hastalarında AMD 3100 + G-CSF ilk faz-II çalışması başlatıldı EMA onayı 46
Plerixafor keşfi ve geliştirilmesi 1991 -1992 HIV inhibitorü olarak sentez edildi 1996 -1997 HIV hücre içine giriş yapabilmesi için kemokin ko-reseptörüne ihtiyacı tanımlandı AMD 3100’ün CXCR 4’ün potent inhibitörü olduğu bulundu 1998 Sağlıklı gönüllülerde AMD 3100’ün ilk faz-I (mobilizasyon) çalışması başlatıldı 2001 2006 MM ve NHL hastalarında faz-III çalışmaları tamamlandı 2008 FDA onayı 2009 | MM ve NHL hastalarında AMD 3100 + G-CSF ilk faz-II çalışması başlatıldı EMA onayı 46
 Plerixafor klinik çalışmaları | 47
Plerixafor klinik çalışmaları | 47
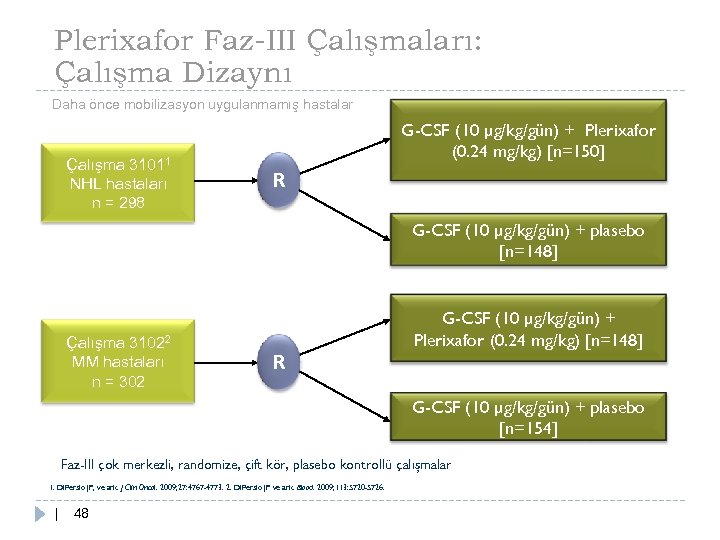 Plerixafor Faz-III Çalışmaları: Çalışma Dizaynı Daha önce mobilizasyon uygulanmamış hastalar Çalışma 31011 NHL hastaları n = 298 G-CSF (10 µg/kg/gün) + Plerixafor (0. 24 mg/kg) [n=150] R G-CSF (10 µg/kg/gün) + plasebo [n=148] Çalışma 31022 MM hastaları n = 302 G-CSF (10 µg/kg/gün) + Plerixafor (0. 24 mg/kg) [n=148] R G-CSF (10 µg/kg/gün) + plasebo [n=154] Faz-III çok merkezli, randomize, çift kör, plasebo kontrollü çalışmalar 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 48
Plerixafor Faz-III Çalışmaları: Çalışma Dizaynı Daha önce mobilizasyon uygulanmamış hastalar Çalışma 31011 NHL hastaları n = 298 G-CSF (10 µg/kg/gün) + Plerixafor (0. 24 mg/kg) [n=150] R G-CSF (10 µg/kg/gün) + plasebo [n=148] Çalışma 31022 MM hastaları n = 302 G-CSF (10 µg/kg/gün) + Plerixafor (0. 24 mg/kg) [n=148] R G-CSF (10 µg/kg/gün) + plasebo [n=154] Faz-III çok merkezli, randomize, çift kör, plasebo kontrollü çalışmalar 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 48
 Plerixafor Faz-III Çalışmaları: Dahil edilme kriterleri 1, 2 Dahil edilme kriterleri ● ● ● 18 -78 yaşları arası Biyopsi ile teşhis edilmiş hastalık Birinci veya ikinci tam ya da parsiyel remisyon Son kemoterapi siklusu > 4 hafta ECOG skoru 0 veya 1 Lab parametreleri: ● Lökosit sayısı > 2. 5 × 109/L ● Mutlak nötrofil sayısı > 1. 5 × 109/L ● Trombosit sayısı > 100 × 109/L ● Serum kreatinin ≤ 2. 2 mg/d. L ● Karaciğer fonksiyon testi < 2. 5 × ULN Dahil edilmeme kriterleri ● ● ● 1. Di. Persio JF ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 49 Önceki kök hücre toplama denemesinde başarısızlık Daha önce oto. PKHN veya allo. PKHN Kemik iliği tutulumu >20% Mobilizasyonda 1. G-CSF dozundan önce 14 gün içerisinde G-CSF kullanımı Daha önceden ibritumomab tiuxetan veya tositumomab ile radyoimmünoterapi (NHL) 1. G-CSF dozunun öncesi 7 gün içerisinde Talidomit, deksametazon, lenalidomit ve/veya bortezomib kullanımı (MM)
Plerixafor Faz-III Çalışmaları: Dahil edilme kriterleri 1, 2 Dahil edilme kriterleri ● ● ● 18 -78 yaşları arası Biyopsi ile teşhis edilmiş hastalık Birinci veya ikinci tam ya da parsiyel remisyon Son kemoterapi siklusu > 4 hafta ECOG skoru 0 veya 1 Lab parametreleri: ● Lökosit sayısı > 2. 5 × 109/L ● Mutlak nötrofil sayısı > 1. 5 × 109/L ● Trombosit sayısı > 100 × 109/L ● Serum kreatinin ≤ 2. 2 mg/d. L ● Karaciğer fonksiyon testi < 2. 5 × ULN Dahil edilmeme kriterleri ● ● ● 1. Di. Persio JF ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 49 Önceki kök hücre toplama denemesinde başarısızlık Daha önce oto. PKHN veya allo. PKHN Kemik iliği tutulumu >20% Mobilizasyonda 1. G-CSF dozundan önce 14 gün içerisinde G-CSF kullanımı Daha önceden ibritumomab tiuxetan veya tositumomab ile radyoimmünoterapi (NHL) 1. G-CSF dozunun öncesi 7 gün içerisinde Talidomit, deksametazon, lenalidomit ve/veya bortezomib kullanımı (MM)
 Plerixafor Faz-III Çalışmaları: Plerixafor uygulama takvimi 1, 2 Mobilizasyon Toplama İzlem 1. Gün 2. Gün 3. Gün 4. Gün 5. Gün 6. Gün 7. Gün 8. Gün Randomizasyon G-CSF (10 µg/kg/gün) Aferez oturumu (3 hacim ± 10% aferez) Mozobil® 0. 24 mg/kg/gün SC veya plasebo ● Plerixafor (0. 24 mg/kg) uygulaması her aferezin yaklaşık 11 saat öncesinde yapıldı 3 ● Plerixafor 4 güne kadar uygulanabilir 3 1 Di. Persio JF ve ark. Blood 2009; 113: 5720 -5726 2 Di. Persio JF ve ark. J Clin Oncol 2009; 27: 4767 -4773 3 Mozobil® [prospektüs]. Cambridge, MA: Genzyme Corp; 2008. | 50
Plerixafor Faz-III Çalışmaları: Plerixafor uygulama takvimi 1, 2 Mobilizasyon Toplama İzlem 1. Gün 2. Gün 3. Gün 4. Gün 5. Gün 6. Gün 7. Gün 8. Gün Randomizasyon G-CSF (10 µg/kg/gün) Aferez oturumu (3 hacim ± 10% aferez) Mozobil® 0. 24 mg/kg/gün SC veya plasebo ● Plerixafor (0. 24 mg/kg) uygulaması her aferezin yaklaşık 11 saat öncesinde yapıldı 3 ● Plerixafor 4 güne kadar uygulanabilir 3 1 Di. Persio JF ve ark. Blood 2009; 113: 5720 -5726 2 Di. Persio JF ve ark. J Clin Oncol 2009; 27: 4767 -4773 3 Mozobil® [prospektüs]. Cambridge, MA: Genzyme Corp; 2008. | 50
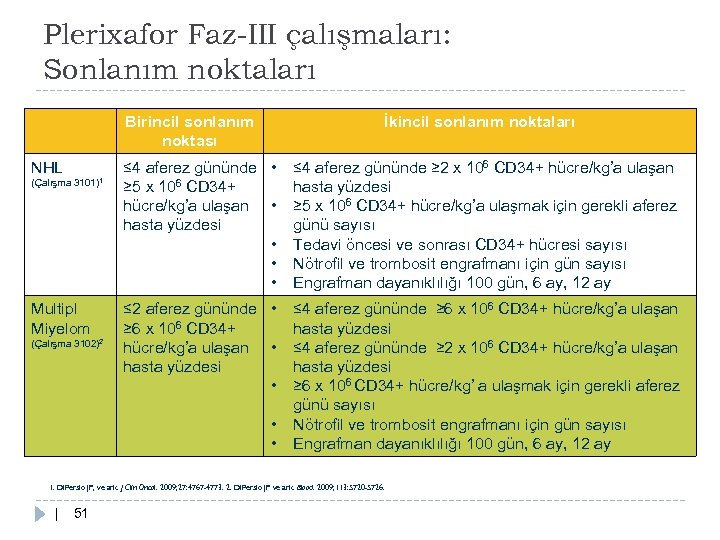 Plerixafor Faz-III çalışmaları: Sonlanım noktaları Birincil sonlanım noktası NHL (Çalışma 3101)1 Multipl Miyelom (Çalışma 3102)2 İkincil sonlanım noktaları ≤ 4 aferez gününde • ≥ 5 x 106 CD 34+ hücre/kg’a ulaşan • hasta yüzdesi • • • ≤ 4 aferez gününde ≥ 2 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≥ 5 x 106 CD 34+ hücre/kg’a ulaşmak için gerekli aferez günü sayısı Tedavi öncesi ve sonrası CD 34+ hücresi sayısı Nötrofil ve trombosit engrafmanı için gün sayısı Engrafman dayanıklılığı 100 gün, 6 ay, 12 ay ≤ 2 aferez gününde • ≥ 6 x 106 CD 34+ hücre/kg’a ulaşan • hasta yüzdesi • ≤ 4 aferez gününde ≥ 6 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≤ 4 aferez gününde ≥ 2 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≥ 6 x 106 CD 34+ hücre/kg’ a ulaşmak için gerekli aferez günü sayısı Nötrofil ve trombosit engrafmanı için gün sayısı Engrafman dayanıklılığı 100 gün, 6 ay, 12 ay • • 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 51
Plerixafor Faz-III çalışmaları: Sonlanım noktaları Birincil sonlanım noktası NHL (Çalışma 3101)1 Multipl Miyelom (Çalışma 3102)2 İkincil sonlanım noktaları ≤ 4 aferez gününde • ≥ 5 x 106 CD 34+ hücre/kg’a ulaşan • hasta yüzdesi • • • ≤ 4 aferez gününde ≥ 2 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≥ 5 x 106 CD 34+ hücre/kg’a ulaşmak için gerekli aferez günü sayısı Tedavi öncesi ve sonrası CD 34+ hücresi sayısı Nötrofil ve trombosit engrafmanı için gün sayısı Engrafman dayanıklılığı 100 gün, 6 ay, 12 ay ≤ 2 aferez gününde • ≥ 6 x 106 CD 34+ hücre/kg’a ulaşan • hasta yüzdesi • ≤ 4 aferez gününde ≥ 6 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≤ 4 aferez gününde ≥ 2 x 106 CD 34+ hücre/kg’a ulaşan hasta yüzdesi ≥ 6 x 106 CD 34+ hücre/kg’ a ulaşmak için gerekli aferez günü sayısı Nötrofil ve trombosit engrafmanı için gün sayısı Engrafman dayanıklılığı 100 gün, 6 ay, 12 ay • • 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 51
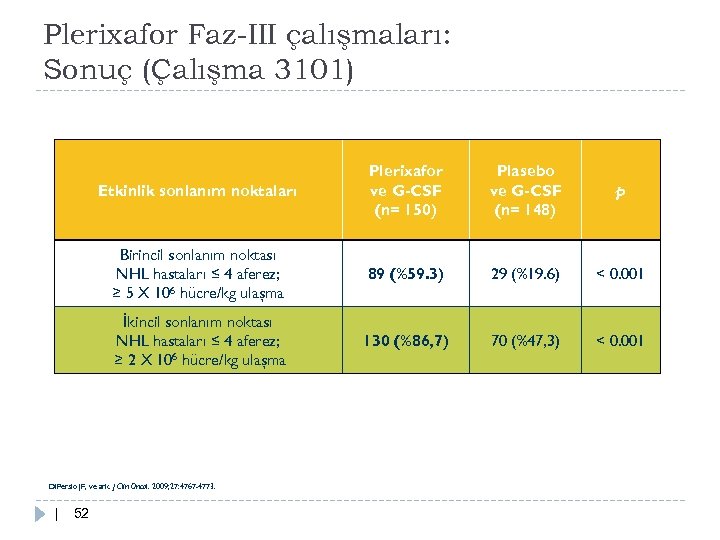 Plerixafor Faz-III çalışmaları: Sonuç (Çalışma 3101) Etkinlik sonlanım noktaları Plerixafor ve G-CSF (n= 150) Plasebo ve G-CSF (n= 148) p Birincil sonlanım noktası NHL hastaları ≤ 4 aferez; ≥ 5 X 106 hücre/kg ulaşma 89 (%59. 3) 29 (%19. 6) < 0. 001 İkincil sonlanım noktası NHL hastaları ≤ 4 aferez; ≥ 2 X 106 hücre/kg ulaşma 130 (%86, 7) 70 (%47, 3) < 0. 001 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. | 52
Plerixafor Faz-III çalışmaları: Sonuç (Çalışma 3101) Etkinlik sonlanım noktaları Plerixafor ve G-CSF (n= 150) Plasebo ve G-CSF (n= 148) p Birincil sonlanım noktası NHL hastaları ≤ 4 aferez; ≥ 5 X 106 hücre/kg ulaşma 89 (%59. 3) 29 (%19. 6) < 0. 001 İkincil sonlanım noktası NHL hastaları ≤ 4 aferez; ≥ 2 X 106 hücre/kg ulaşma 130 (%86, 7) 70 (%47, 3) < 0. 001 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. | 52
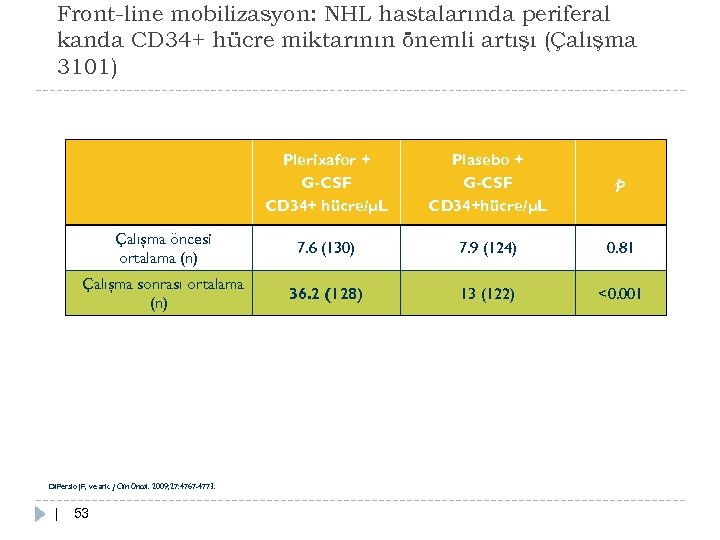 Front-line mobilizasyon: NHL hastalarında periferal kanda CD 34+ hücre miktarının önemli artışı (Çalışma 3101) Plerixafor + G-CSF CD 34+ hücre/µL Plasebo + G-CSF CD 34+hücre/µL p Çalışma öncesi ortalama (n) 7. 6 (130) 7. 9 (124) 0. 81 Çalışma sonrası ortalama (n) 36. 2 (128) 13 (122) <0. 001 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. | 53
Front-line mobilizasyon: NHL hastalarında periferal kanda CD 34+ hücre miktarının önemli artışı (Çalışma 3101) Plerixafor + G-CSF CD 34+ hücre/µL Plasebo + G-CSF CD 34+hücre/µL p Çalışma öncesi ortalama (n) 7. 6 (130) 7. 9 (124) 0. 81 Çalışma sonrası ortalama (n) 36. 2 (128) 13 (122) <0. 001 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. | 53
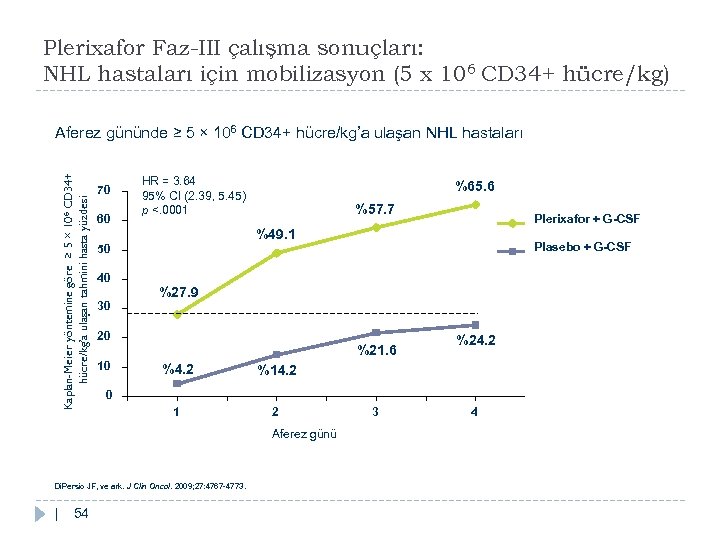 Plerixafor Faz-III çalışma sonuçları: NHL hastaları için mobilizasyon (5 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 5 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Aferez gününde ≥ 5 × 106 CD 34+ hücre/kg’a ulaşan NHL hastaları 70 60 HR = 3. 64 95% CI (2. 39, 5. 45) p <. 0001 %65. 6 %57. 7 %49. 1 40 30 %27. 9 20 10 %21. 6 %4. 2 1 2 %24. 2 %14. 2 0 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 54 Plasebo + G-CSF 50 Aferez günü | Plerixafor + G-CSF 3 4
Plerixafor Faz-III çalışma sonuçları: NHL hastaları için mobilizasyon (5 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 5 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Aferez gününde ≥ 5 × 106 CD 34+ hücre/kg’a ulaşan NHL hastaları 70 60 HR = 3. 64 95% CI (2. 39, 5. 45) p <. 0001 %65. 6 %57. 7 %49. 1 40 30 %27. 9 20 10 %21. 6 %4. 2 1 2 %24. 2 %14. 2 0 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 54 Plasebo + G-CSF 50 Aferez günü | Plerixafor + G-CSF 3 4
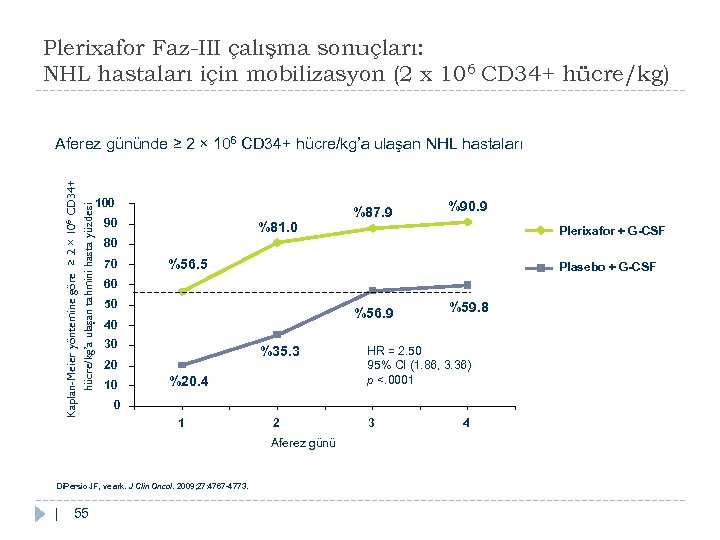 Plerixafor Faz-III çalışma sonuçları: NHL hastaları için mobilizasyon (2 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 2 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Aferez gününde ≥ 2 × 106 CD 34+ hücre/kg’a ulaşan NHL hastaları 100 90 %81. 0 70 Plerixafor + G-CSF %56. 5 Plasebo + G-CSF 60 50 %56. 9 40 30 %35. 3 20 10 %20. 4 %59. 8 HR = 2. 50 95% CI (1. 86, 3. 36) p <. 0001 0 1 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 55 %90. 9 80 2 Aferez günü | %87. 9 3 4
Plerixafor Faz-III çalışma sonuçları: NHL hastaları için mobilizasyon (2 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 2 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Aferez gününde ≥ 2 × 106 CD 34+ hücre/kg’a ulaşan NHL hastaları 100 90 %81. 0 70 Plerixafor + G-CSF %56. 5 Plasebo + G-CSF 60 50 %56. 9 40 30 %35. 3 20 10 %20. 4 %59. 8 HR = 2. 50 95% CI (1. 86, 3. 36) p <. 0001 0 1 Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 55 %90. 9 80 2 Aferez günü | %87. 9 3 4
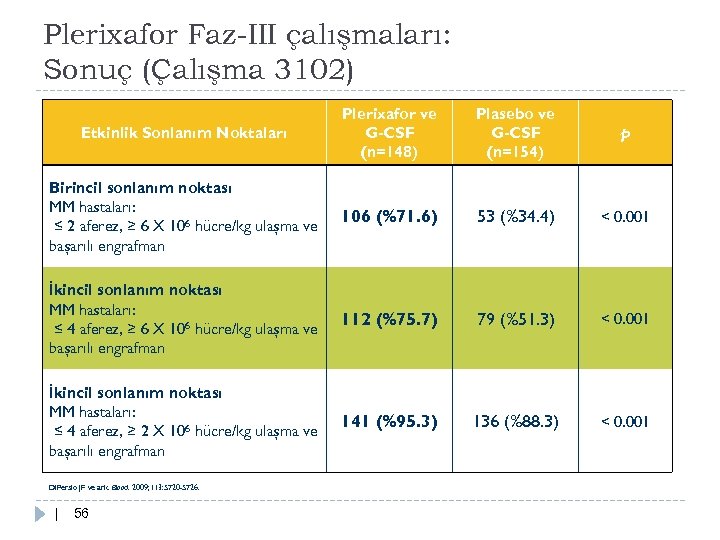 Plerixafor Faz-III çalışmaları: Sonuç (Çalışma 3102) Etkinlik Sonlanım Noktaları Plerixafor ve G-CSF (n=148) Plasebo ve G-CSF (n=154) p Birincil sonlanım noktası MM hastaları: ≤ 2 aferez, ≥ 6 X 106 hücre/kg ulaşma ve başarılı engrafman 106 (%71. 6) 53 (%34. 4) < 0. 001 İkincil sonlanım noktası MM hastaları: ≤ 4 aferez, ≥ 6 X 106 hücre/kg ulaşma ve başarılı engrafman 112 (%75. 7) 79 (%51. 3) < 0. 001 İkincil sonlanım noktası MM hastaları: ≤ 4 aferez, ≥ 2 X 106 hücre/kg ulaşma ve başarılı engrafman 141 (%95. 3) 136 (%88. 3) < 0. 001 Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 56
Plerixafor Faz-III çalışmaları: Sonuç (Çalışma 3102) Etkinlik Sonlanım Noktaları Plerixafor ve G-CSF (n=148) Plasebo ve G-CSF (n=154) p Birincil sonlanım noktası MM hastaları: ≤ 2 aferez, ≥ 6 X 106 hücre/kg ulaşma ve başarılı engrafman 106 (%71. 6) 53 (%34. 4) < 0. 001 İkincil sonlanım noktası MM hastaları: ≤ 4 aferez, ≥ 6 X 106 hücre/kg ulaşma ve başarılı engrafman 112 (%75. 7) 79 (%51. 3) < 0. 001 İkincil sonlanım noktası MM hastaları: ≤ 4 aferez, ≥ 2 X 106 hücre/kg ulaşma ve başarılı engrafman 141 (%95. 3) 136 (%88. 3) < 0. 001 Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 56
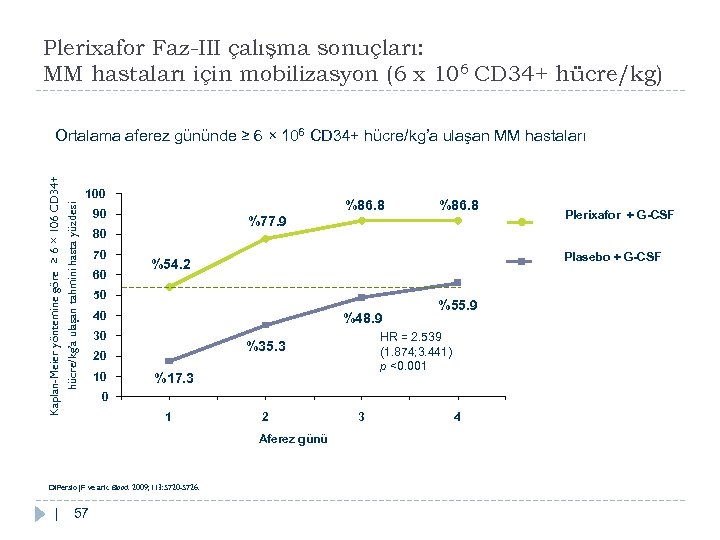 Plerixafor Faz-III çalışma sonuçları: MM hastaları için mobilizasyon (6 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 6 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Ortalama aferez gününde ≥ 6 × 106 CD 34+ hücre/kg’a ulaşan MM hastaları 100 %86. 8 90 %77. 9 80 70 60 40 %48. 9 30 %17. 3 0 1 2 Aferez günü Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 57 %55. 9 HR = 2. 539 (1. 874; 3. 441) p <0. 001 %35. 3 20 Plerixafor + G-CSF Plasebo + G-CSF %54. 2 50 10 %86. 8 3 4
Plerixafor Faz-III çalışma sonuçları: MM hastaları için mobilizasyon (6 x 106 CD 34+ hücre/kg) Kaplan-Meier yöntemine göre ≥ 6 × 106 CD 34+ hücre/kg’a ulaşan tahmini hasta yüzdesi Ortalama aferez gününde ≥ 6 × 106 CD 34+ hücre/kg’a ulaşan MM hastaları 100 %86. 8 90 %77. 9 80 70 60 40 %48. 9 30 %17. 3 0 1 2 Aferez günü Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 57 %55. 9 HR = 2. 539 (1. 874; 3. 441) p <0. 001 %35. 3 20 Plerixafor + G-CSF Plasebo + G-CSF %54. 2 50 10 %86. 8 3 4
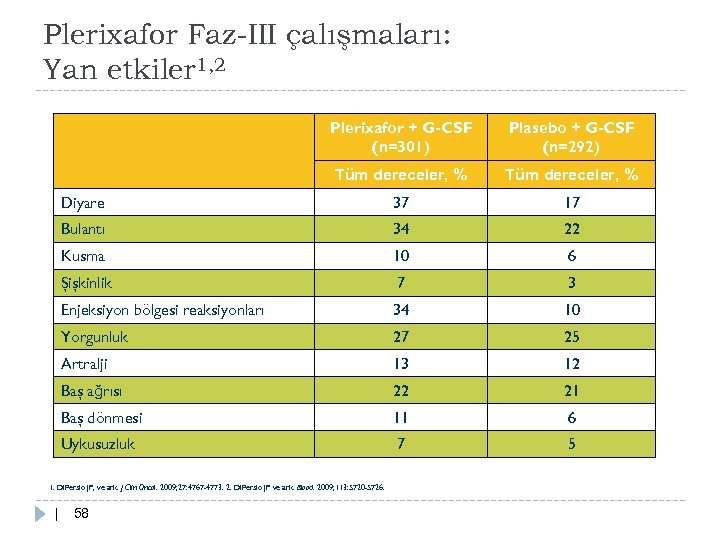 Plerixafor Faz-III çalışmaları: Yan etkiler 1, 2 Plerixafor + G-CSF (n=301) Plasebo + G-CSF (n=292) Tüm dereceler, % Diyare 37 17 Bulantı 34 22 Kusma 10 6 Şişkinlik 7 3 Enjeksiyon bölgesi reaksiyonları 34 10 Yorgunluk 27 25 Artralji 13 12 Baş ağrısı 22 21 Baş dönmesi 11 6 Uykusuzluk 7 5 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 58
Plerixafor Faz-III çalışmaları: Yan etkiler 1, 2 Plerixafor + G-CSF (n=301) Plasebo + G-CSF (n=292) Tüm dereceler, % Diyare 37 17 Bulantı 34 22 Kusma 10 6 Şişkinlik 7 3 Enjeksiyon bölgesi reaksiyonları 34 10 Yorgunluk 27 25 Artralji 13 12 Baş ağrısı 22 21 Baş dönmesi 11 6 Uykusuzluk 7 5 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 58
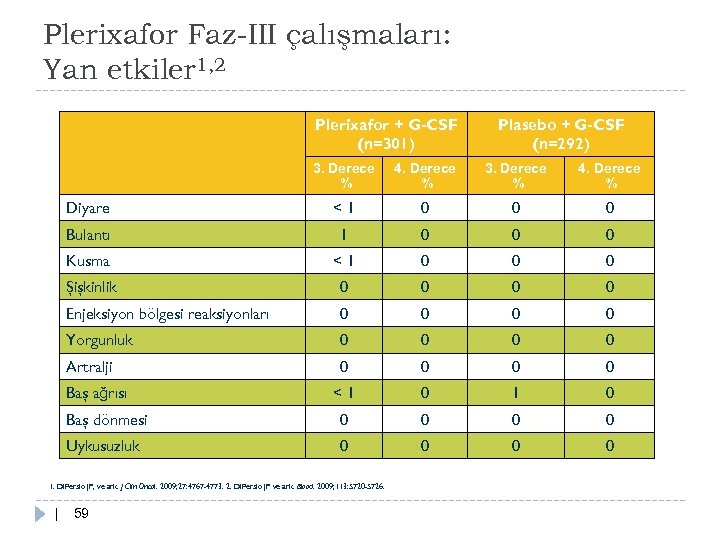 Plerixafor Faz-III çalışmaları: Yan etkiler 1, 2 Plerixafor + G-CSF (n=301) Plasebo + G-CSF (n=292) 3. Derece % 4. Derece % Diyare <1 0 0 0 Bulantı 1 0 0 0 Kusma <1 0 0 0 Şişkinlik 0 0 Enjeksiyon bölgesi reaksiyonları 0 0 Yorgunluk 0 0 Artralji 0 0 <1 0 Baş dönmesi 0 0 Uykusuzluk 0 0 Baş ağrısı 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 59
Plerixafor Faz-III çalışmaları: Yan etkiler 1, 2 Plerixafor + G-CSF (n=301) Plasebo + G-CSF (n=292) 3. Derece % 4. Derece % Diyare <1 0 0 0 Bulantı 1 0 0 0 Kusma <1 0 0 0 Şişkinlik 0 0 Enjeksiyon bölgesi reaksiyonları 0 0 Yorgunluk 0 0 Artralji 0 0 <1 0 Baş dönmesi 0 0 Uykusuzluk 0 0 Baş ağrısı 1. Di. Persio JF, ve ark. J Clin Oncol. 2009; 27: 4767 -4773. 2. Di. Persio JF ve ark. Blood. 2009; 113: 5720 -5726. | 59
 PREDICT Çalışması Russell ve ark. Haematologica 2013; 98(2): 172 -178 | 60
PREDICT Çalışması Russell ve ark. Haematologica 2013; 98(2): 172 -178 | 60
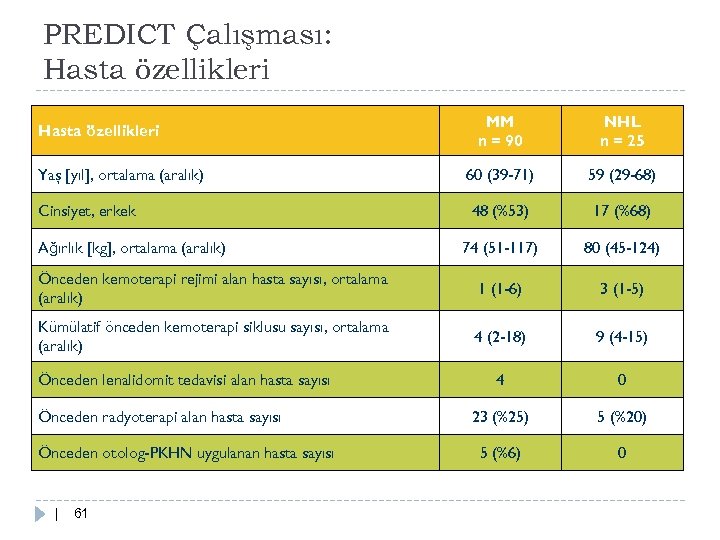 PREDICT Çalışması: Hasta özellikleri MM n = 90 NHL n = 25 60 (39 -71) 59 (29 -68) 48 (%53) 17 (%68) 74 (51 -117) 80 (45 -124) Önceden kemoterapi rejimi alan hasta sayısı, ortalama (aralık) 1 (1 -6) 3 (1 -5) Kümülatif önceden kemoterapi siklusu sayısı, ortalama (aralık) 4 (2 -18) 9 (4 -15) 4 0 23 (%25) 5 (%20) 5 (%6) 0 Hasta özellikleri Yaş [yıl], ortalama (aralık) Cinsiyet, erkek Ağırlık [kg], ortalama (aralık) Önceden lenalidomit tedavisi alan hasta sayısı Önceden radyoterapi alan hasta sayısı Önceden otolog-PKHN uygulanan hasta sayısı | 61
PREDICT Çalışması: Hasta özellikleri MM n = 90 NHL n = 25 60 (39 -71) 59 (29 -68) 48 (%53) 17 (%68) 74 (51 -117) 80 (45 -124) Önceden kemoterapi rejimi alan hasta sayısı, ortalama (aralık) 1 (1 -6) 3 (1 -5) Kümülatif önceden kemoterapi siklusu sayısı, ortalama (aralık) 4 (2 -18) 9 (4 -15) 4 0 23 (%25) 5 (%20) 5 (%6) 0 Hasta özellikleri Yaş [yıl], ortalama (aralık) Cinsiyet, erkek Ağırlık [kg], ortalama (aralık) Önceden lenalidomit tedavisi alan hasta sayısı Önceden radyoterapi alan hasta sayısı Önceden otolog-PKHN uygulanan hasta sayısı | 61
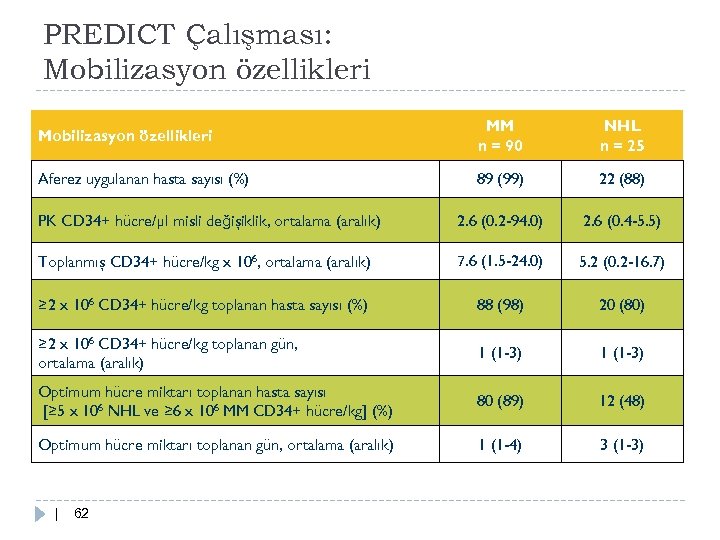 PREDICT Çalışması: Mobilizasyon özellikleri MM n = 90 NHL n = 25 Aferez uygulanan hasta sayısı (%) 89 (99) 22 (88) PK CD 34+ hücre/µl misli değişiklik, ortalama (aralık) 2. 6 (0. 2 -94. 0) 2. 6 (0. 4 -5. 5) Toplanmış CD 34+ hücre/kg x 106, ortalama (aralık) 7. 6 (1. 5 -24. 0) 5. 2 (0. 2 -16. 7) ≥ 2 x 106 CD 34+ hücre/kg toplanan hasta sayısı (%) 88 (98) 20 (80) ≥ 2 x 106 CD 34+ hücre/kg toplanan gün, ortalama (aralık) 1 (1 -3) Optimum hücre miktarı toplanan hasta sayısı [≥ 5 x 106 NHL ve ≥ 6 x 106 MM CD 34+ hücre/kg] (%) 80 (89) 12 (48) Optimum hücre miktarı toplanan gün, ortalama (aralık) 1 (1 -4) 3 (1 -3) | 62
PREDICT Çalışması: Mobilizasyon özellikleri MM n = 90 NHL n = 25 Aferez uygulanan hasta sayısı (%) 89 (99) 22 (88) PK CD 34+ hücre/µl misli değişiklik, ortalama (aralık) 2. 6 (0. 2 -94. 0) 2. 6 (0. 4 -5. 5) Toplanmış CD 34+ hücre/kg x 106, ortalama (aralık) 7. 6 (1. 5 -24. 0) 5. 2 (0. 2 -16. 7) ≥ 2 x 106 CD 34+ hücre/kg toplanan hasta sayısı (%) 88 (98) 20 (80) ≥ 2 x 106 CD 34+ hücre/kg toplanan gün, ortalama (aralık) 1 (1 -3) Optimum hücre miktarı toplanan hasta sayısı [≥ 5 x 106 NHL ve ≥ 6 x 106 MM CD 34+ hücre/kg] (%) 80 (89) 12 (48) Optimum hücre miktarı toplanan gün, ortalama (aralık) 1 (1 -4) 3 (1 -3) | 62
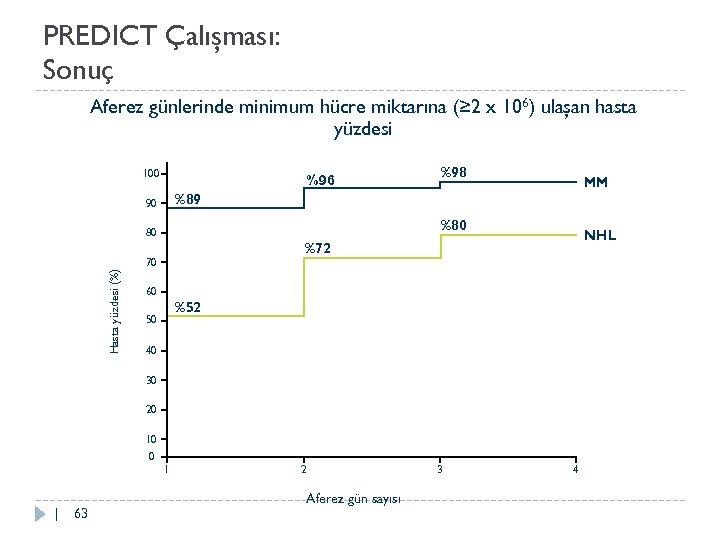 PREDICT Çalışması: Sonuç Aferez günlerinde minimum hücre miktarına (≥ 2 x 106) ulaşan hasta yüzdesi 100 %96 MM %89 90 %80 80 NHL %72 70 Hasta yüzdesi (%) %98 60 %52 50 40 30 20 10 0 1 | 63 2 3 Aferez gün sayısı 4
PREDICT Çalışması: Sonuç Aferez günlerinde minimum hücre miktarına (≥ 2 x 106) ulaşan hasta yüzdesi 100 %96 MM %89 90 %80 80 NHL %72 70 Hasta yüzdesi (%) %98 60 %52 50 40 30 20 10 0 1 | 63 2 3 Aferez gün sayısı 4
 Mobilizasyon başarısızlıkları | 64
Mobilizasyon başarısızlıkları | 64
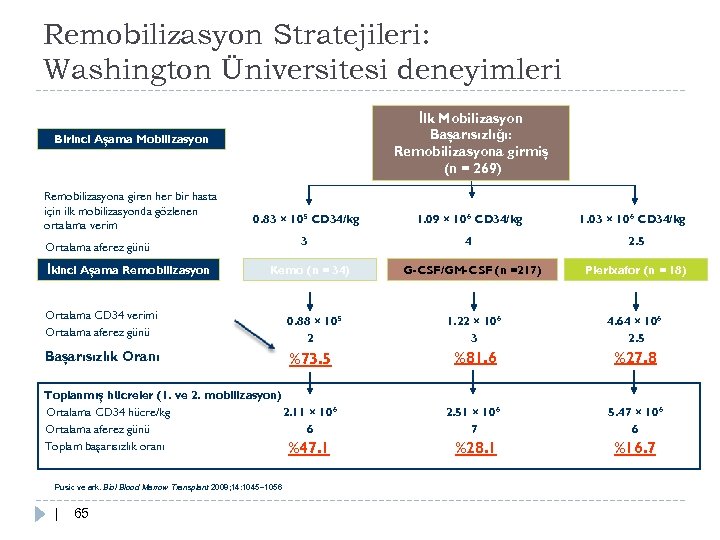 Remobilizasyon Stratejileri: Washington Üniversitesi deneyimleri İlk Mobilizasyon Başarısızlığı: Remobilizasyona girmiş (n = 269) Birinci Aşama Mobilizasyon Remobilizasyona giren her bir hasta için ilk mobilizasyonda gözlenen ortalama verim 0. 83 × 105 CD 34/kg 1. 09 × 106 CD 34/kg 3 4 Ortalama aferez günü İkinci Aşama Remobilizasyon Kemo (n = 34) Ortalama CD 34 verimi Ortalama aferez günü 0. 88 × 105 2 Başarısızlık Oranı %73. 5 Toplanmış hücreler (1. ve 2. mobilizasyon) Ortalama CD 34 hücre/kg 2. 11 × 106 Ortalama aferez günü 6 Toplam başarısızlık oranı %47. 1 Pusic ve ark. Biol Blood Marrow Transplant 2008; 14: 1045– 1056 | 65 1. 03 × 106 CD 34/kg 2. 5 G-CSF/GM-CSF (n =217) Plerixafor (n = 18) 1. 22 × 106 3 4. 64 × 106 2. 5 %81. 6 %27. 8 2. 51 × 106 7 5. 47 × 106 6 %28. 1 %16. 7
Remobilizasyon Stratejileri: Washington Üniversitesi deneyimleri İlk Mobilizasyon Başarısızlığı: Remobilizasyona girmiş (n = 269) Birinci Aşama Mobilizasyon Remobilizasyona giren her bir hasta için ilk mobilizasyonda gözlenen ortalama verim 0. 83 × 105 CD 34/kg 1. 09 × 106 CD 34/kg 3 4 Ortalama aferez günü İkinci Aşama Remobilizasyon Kemo (n = 34) Ortalama CD 34 verimi Ortalama aferez günü 0. 88 × 105 2 Başarısızlık Oranı %73. 5 Toplanmış hücreler (1. ve 2. mobilizasyon) Ortalama CD 34 hücre/kg 2. 11 × 106 Ortalama aferez günü 6 Toplam başarısızlık oranı %47. 1 Pusic ve ark. Biol Blood Marrow Transplant 2008; 14: 1045– 1056 | 65 1. 03 × 106 CD 34/kg 2. 5 G-CSF/GM-CSF (n =217) Plerixafor (n = 18) 1. 22 × 106 3 4. 64 × 106 2. 5 %81. 6 %27. 8 2. 51 × 106 7 5. 47 × 106 6 %28. 1 %16. 7
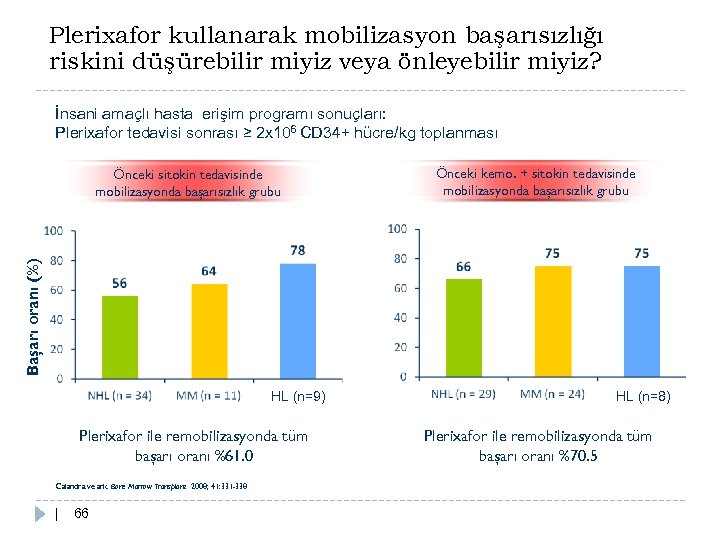 Plerixafor kullanarak mobilizasyon başarısızlığı riskini düşürebilir miyiz veya önleyebilir miyiz? İnsani amaçlı hasta erişim programı sonuçları: Plerixafor tedavisi sonrası ≥ 2 x 106 CD 34+ hücre/kg toplanması Önceki kemo. + sitokin tedavisinde mobilizasyonda başarısızlık grubu Başarı oranı (%) Önceki sitokin tedavisinde mobilizasyonda başarısızlık grubu HL (n=9) Plerixafor ile remobilizasyonda tüm başarı oranı %61. 0 Calandra ve ark. Bone Marrow Transplant 2008; 41: 331 -338 | 66 HL (n=8) Plerixafor ile remobilizasyonda tüm başarı oranı %70. 5
Plerixafor kullanarak mobilizasyon başarısızlığı riskini düşürebilir miyiz veya önleyebilir miyiz? İnsani amaçlı hasta erişim programı sonuçları: Plerixafor tedavisi sonrası ≥ 2 x 106 CD 34+ hücre/kg toplanması Önceki kemo. + sitokin tedavisinde mobilizasyonda başarısızlık grubu Başarı oranı (%) Önceki sitokin tedavisinde mobilizasyonda başarısızlık grubu HL (n=9) Plerixafor ile remobilizasyonda tüm başarı oranı %61. 0 Calandra ve ark. Bone Marrow Transplant 2008; 41: 331 -338 | 66 HL (n=8) Plerixafor ile remobilizasyonda tüm başarı oranı %70. 5
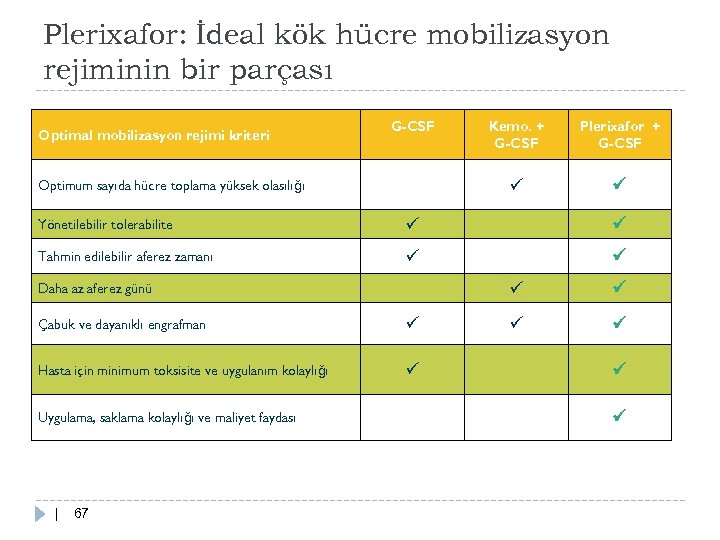 Plerixafor: İdeal kök hücre mobilizasyon rejiminin bir parçası Optimal mobilizasyon rejimi kriteri Optimum sayıda hücre toplama yüksek olasılığı Kemo. + G-CSF Plerixafor + G-CSF Yönetilebilir tolerabilite Tahmin edilebilir aferez zamanı Daha az aferez günü Çabuk ve dayanıklı engrafman Hasta için minimum toksisite ve uygulanım kolaylığı Uygulama, saklama kolaylığı ve maliyet faydası | 67
Plerixafor: İdeal kök hücre mobilizasyon rejiminin bir parçası Optimal mobilizasyon rejimi kriteri Optimum sayıda hücre toplama yüksek olasılığı Kemo. + G-CSF Plerixafor + G-CSF Yönetilebilir tolerabilite Tahmin edilebilir aferez zamanı Daha az aferez günü Çabuk ve dayanıklı engrafman Hasta için minimum toksisite ve uygulanım kolaylığı Uygulama, saklama kolaylığı ve maliyet faydası | 67
 Plerixafor genel olarak iyi tolere edilir ve tipik kemoterapilerin yan etki ile ilgisi yoktur Plerixafor kullanımı ile ilgili yan etkiler tipik olarak hafif ya da orta şiddettedir ve G-CSF’nin tek başına kullanımı ile benzer özelliktedir Plerixafor kullanımı ile görülen en sık izlenen yan etkiler Gİ bozukluklar (diyare, bulantı) ve enjeksiyon bölgesi reaksiyonlarıdır Plerixafor tedavisinde febril nötropeni izlenmez | 68
Plerixafor genel olarak iyi tolere edilir ve tipik kemoterapilerin yan etki ile ilgisi yoktur Plerixafor kullanımı ile ilgili yan etkiler tipik olarak hafif ya da orta şiddettedir ve G-CSF’nin tek başına kullanımı ile benzer özelliktedir Plerixafor kullanımı ile görülen en sık izlenen yan etkiler Gİ bozukluklar (diyare, bulantı) ve enjeksiyon bölgesi reaksiyonlarıdır Plerixafor tedavisinde febril nötropeni izlenmez | 68
 Kemoterapi temelli mobilizasyonun dezavantajları ● ● İnfeksiyon riski ● ● Aferez başlatma kriteri çeşitlidir 2, 3, 4, 5, 6 Kemomobilizasyon ve CD 34+ hücre piki arasındaki geçen süre tahmin edilemez 1, 3 Hastaneye yatış ihtiyacı Transfüzyon desteği ihtiyacı Artan maliyetler 1 Hicks ML, ve ark. Transfusion. 2007; 47(4): 629 -635; 2 Desikan KR, ve ark. J Clin Oncol. 1998; 16(4): 1547 -1553; 3 Bargetzi MJ, ve ark. Bone Marrow Transplant. 2003; 31(2): 99 -103; 4 Humpe A, ve ark. Transfusion. 2000; 40(11): 1363 -1370; 5 Venditti A, ve ark. Bone Marrow Transplant. 1999; 24(9): 1019 -1027; 6 Arora M, ve ark. Biol Blood Marrow Transplant. 2004; 10(6): 395 -404. | 69
Kemoterapi temelli mobilizasyonun dezavantajları ● ● İnfeksiyon riski ● ● Aferez başlatma kriteri çeşitlidir 2, 3, 4, 5, 6 Kemomobilizasyon ve CD 34+ hücre piki arasındaki geçen süre tahmin edilemez 1, 3 Hastaneye yatış ihtiyacı Transfüzyon desteği ihtiyacı Artan maliyetler 1 Hicks ML, ve ark. Transfusion. 2007; 47(4): 629 -635; 2 Desikan KR, ve ark. J Clin Oncol. 1998; 16(4): 1547 -1553; 3 Bargetzi MJ, ve ark. Bone Marrow Transplant. 2003; 31(2): 99 -103; 4 Humpe A, ve ark. Transfusion. 2000; 40(11): 1363 -1370; 5 Venditti A, ve ark. Bone Marrow Transplant. 1999; 24(9): 1019 -1027; 6 Arora M, ve ark. Biol Blood Marrow Transplant. 2004; 10(6): 395 -404. | 69
 Sitokin mobilizasyonunun avantajları ● Mobilizasyon için tahmin edilebilir kinetikler ● Kemoterapi temelli mobilizasyon ile karşılaştırıldığında düşük toksisite ve kaynak kullanımı ● Hastane yatış ve transfüzyona ihtiyaç duymama ● Uygulayıcı için kolaylık | 70
Sitokin mobilizasyonunun avantajları ● Mobilizasyon için tahmin edilebilir kinetikler ● Kemoterapi temelli mobilizasyon ile karşılaştırıldığında düşük toksisite ve kaynak kullanımı ● Hastane yatış ve transfüzyona ihtiyaç duymama ● Uygulayıcı için kolaylık | 70
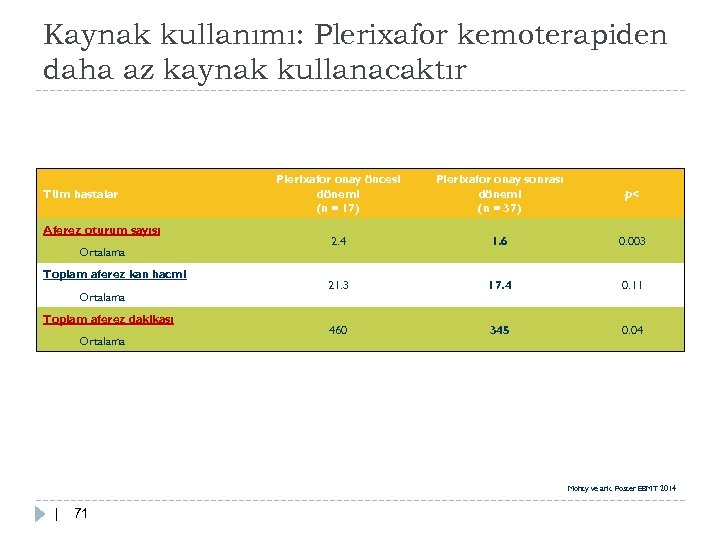 Kaynak kullanımı: Plerixafor kemoterapiden daha az kaynak kullanacaktır Tüm hastalar Aferez oturum sayısı Ortalama Toplam aferez kan hacmi Ortalama Toplam aferez dakikası Ortalama Plerixafor onay öncesi dönemi (n = 17) Plerixafor onay sonrası dönemi (n = 37) p< 2. 4 1. 6 0. 003 21. 3 17. 4 0. 11 460 345 0. 04 Mohty ve ark. Poster EBMT 2014 | 71
Kaynak kullanımı: Plerixafor kemoterapiden daha az kaynak kullanacaktır Tüm hastalar Aferez oturum sayısı Ortalama Toplam aferez kan hacmi Ortalama Toplam aferez dakikası Ortalama Plerixafor onay öncesi dönemi (n = 17) Plerixafor onay sonrası dönemi (n = 37) p< 2. 4 1. 6 0. 003 21. 3 17. 4 0. 11 460 345 0. 04 Mohty ve ark. Poster EBMT 2014 | 71
 Kemomobilizasyon ile tek başına sitokin kullanımından daha fazla PKH verimi sonucu alınabilir. Bununla birlikte kemomobilizasyondan sonra hastaların büyük yüzdesinde febril nötropeni ve yüksek oranda hastane yatışı olmaktadır G-CSF’ye Plerixafor ilavesi kemoterapi kadar etkili olabilir Plerixafor’un “just in time” “on demand” “pre emptif” olarak kullanımı etkili ve uygun maliyetli görünmektedir | 72
Kemomobilizasyon ile tek başına sitokin kullanımından daha fazla PKH verimi sonucu alınabilir. Bununla birlikte kemomobilizasyondan sonra hastaların büyük yüzdesinde febril nötropeni ve yüksek oranda hastane yatışı olmaktadır G-CSF’ye Plerixafor ilavesi kemoterapi kadar etkili olabilir Plerixafor’un “just in time” “on demand” “pre emptif” olarak kullanımı etkili ve uygun maliyetli görünmektedir | 72
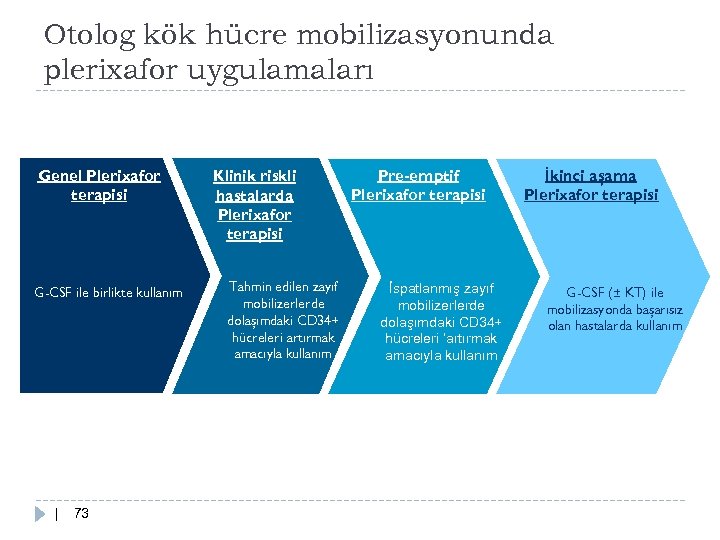 Otolog kök hücre mobilizasyonunda plerixafor uygulamaları Genel Plerixafor terapisi G-CSF ile birlikte kullanım | 73 Klinik riskli hastalarda Plerixafor terapisi Tahmin edilen zayıf mobilizerlerde dolaşımdaki CD 34+ hücreleri artırmak amacıyla kullanım Pre-emptif Plerixafor terapisi İspatlanmış zayıf mobilizerlerde dolaşımdaki CD 34+ hücreleri ‘artırmak amacıyla kullanım İkinci aşama Plerixafor terapisi G-CSF (± KT) ile mobilizasyonda başarısız olan hastalarda kullanım
Otolog kök hücre mobilizasyonunda plerixafor uygulamaları Genel Plerixafor terapisi G-CSF ile birlikte kullanım | 73 Klinik riskli hastalarda Plerixafor terapisi Tahmin edilen zayıf mobilizerlerde dolaşımdaki CD 34+ hücreleri artırmak amacıyla kullanım Pre-emptif Plerixafor terapisi İspatlanmış zayıf mobilizerlerde dolaşımdaki CD 34+ hücreleri ‘artırmak amacıyla kullanım İkinci aşama Plerixafor terapisi G-CSF (± KT) ile mobilizasyonda başarısız olan hastalarda kullanım
 Kılavuzlar | 74
Kılavuzlar | 74
 Autologous haematopoietic stem cell mobilisation in patients with multiple myeloma and lymphoma (2014) M Mohty, France; K Hübel, Germany; N Kröger, Germany; M Aljurf, Saudi Arabia; J Apperley, UK; G Basak, Poland; A Bazarbachi, Lebanon; K Douglas, UK; I Gabriel, UK; L Garderet, France; C Geraldes, Portugal; O Jaksic, Croatia; M Kattan, USA; Z Koristek, Czech Republic; F Lanza, Italy; RM Lemoli, Italy; L Mendeleeva, Russia; G Mikala, Hungary; N Mikhailova, Russia; A Nagler, Israel; HC Schouten, The Netherlands; D Selleslag, Belgium; S Suciu, Belgium; A Sureda, UK; N Worel, Austria; P Wuchter, Germany; C Chabannon, France; and RF Duarte, Spain A position statement on behalf of the EBMT investigators All authors contributed equally to this work ● 28 EBMT uzmanı; ● MM ve lenfomada PKHN için en iyi yaklaşımlar ● Zayıf mobilizerler için potansiyel optimizasyon seçenekleri Mohty ve ark. Bone Marrow Transplantation 2014; 49: 865 -872 | 75
Autologous haematopoietic stem cell mobilisation in patients with multiple myeloma and lymphoma (2014) M Mohty, France; K Hübel, Germany; N Kröger, Germany; M Aljurf, Saudi Arabia; J Apperley, UK; G Basak, Poland; A Bazarbachi, Lebanon; K Douglas, UK; I Gabriel, UK; L Garderet, France; C Geraldes, Portugal; O Jaksic, Croatia; M Kattan, USA; Z Koristek, Czech Republic; F Lanza, Italy; RM Lemoli, Italy; L Mendeleeva, Russia; G Mikala, Hungary; N Mikhailova, Russia; A Nagler, Israel; HC Schouten, The Netherlands; D Selleslag, Belgium; S Suciu, Belgium; A Sureda, UK; N Worel, Austria; P Wuchter, Germany; C Chabannon, France; and RF Duarte, Spain A position statement on behalf of the EBMT investigators All authors contributed equally to this work ● 28 EBMT uzmanı; ● MM ve lenfomada PKHN için en iyi yaklaşımlar ● Zayıf mobilizerler için potansiyel optimizasyon seçenekleri Mohty ve ark. Bone Marrow Transplantation 2014; 49: 865 -872 | 75
 Konsensus: MM hastaları için PKHN stratejileri Kararlı durum mobilizasyon MM Kemoterapi temelli mobilizasyon (siklofosfamid veya etoposid) Lokal kılavuzlara göre kararlı durum veya kemomobilizasyonun kullanımına karar verilir Ancak, kararlı durum mobilizasyonda yeterli CD 34+ hücre sayısını elde etmek olasılığı düşük Siklofosfamid monoterapisi: | 76 1. 5– 4. 0 g/m 2 aralığı uygundur
Konsensus: MM hastaları için PKHN stratejileri Kararlı durum mobilizasyon MM Kemoterapi temelli mobilizasyon (siklofosfamid veya etoposid) Lokal kılavuzlara göre kararlı durum veya kemomobilizasyonun kullanımına karar verilir Ancak, kararlı durum mobilizasyonda yeterli CD 34+ hücre sayısını elde etmek olasılığı düşük Siklofosfamid monoterapisi: | 76 1. 5– 4. 0 g/m 2 aralığı uygundur
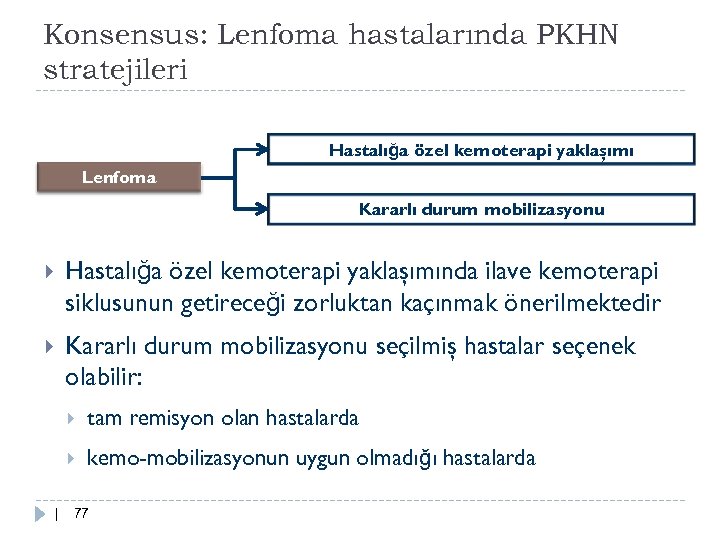 Konsensus: Lenfoma hastalarında PKHN stratejileri Hastalığa özel kemoterapi yaklaşımı Lenfoma Kararlı durum mobilizasyonu Hastalığa özel kemoterapi yaklaşımında ilave kemoterapi siklusunun getireceği zorluktan kaçınmak önerilmektedir Kararlı durum mobilizasyonu seçilmiş hastalar seçenek olabilir: | tam remisyon olan hastalarda kemo-mobilizasyonun uygun olmadığı hastalarda 77
Konsensus: Lenfoma hastalarında PKHN stratejileri Hastalığa özel kemoterapi yaklaşımı Lenfoma Kararlı durum mobilizasyonu Hastalığa özel kemoterapi yaklaşımında ilave kemoterapi siklusunun getireceği zorluktan kaçınmak önerilmektedir Kararlı durum mobilizasyonu seçilmiş hastalar seçenek olabilir: | tam remisyon olan hastalarda kemo-mobilizasyonun uygun olmadığı hastalarda 77
 Konsensus: Mobilizasyon protokollerinin optimizasyonu Kararlı durum re-mobilizasyon yaklaşımı Kemo-mobilizasyon stratejisinin değişimi Kararlı durum kemo-mobilizasyon Kemo-mobilizasyon alternatif kemo-mobilizasyon yaklaşımı Plerixafor gibi son mobilizasyon ajanlarının ilavesi | 78
Konsensus: Mobilizasyon protokollerinin optimizasyonu Kararlı durum re-mobilizasyon yaklaşımı Kemo-mobilizasyon stratejisinin değişimi Kararlı durum kemo-mobilizasyon Kemo-mobilizasyon alternatif kemo-mobilizasyon yaklaşımı Plerixafor gibi son mobilizasyon ajanlarının ilavesi | 78
 Zayıf PKH toplamayı tahmin etme belirteçleri Zayıf PKH toplamayı tahmin için tanımlanmış belirteçler Yaş (yaşlı hastalar)1, 2 Hastalık (daha ileri evre)1 -3 Önceden kemoterapi tedavisi • Yüksek sayıda birincil tedavi aşamaları 1 -4 • Kemoterapi tipi (fludarabin, lenalidomit veya melfalan)1 -5 Önceden radyasyon tedavisi 1, 2 Aferez öncesi periferal kandan düşük CD 34+ hücre sayısı 3, 4, 7 Mobilizasyon öncesi düşük trombosit sayısı 8, 9 Zayıf PKH toplama için muhtemel en güçlü tahmin aracı aferez öncesi periferik kandaki CD 34+ hücre sayısıdır 1, 3, 4, 7 1. 2. 3. 4. | 79 Olivieri ve ark. Bone Marrow Transplant 2012; 47: 342 -51. Perseghin ve ark. Transfus Apher Sci 2009; 41: 33 -7. Sancho ve ark. Cytotherapy 2012; 14: 823 -9. Wuchter ve ark. Biol Blood Marrow Transplant 2010; 16: 490 -9. 5. 6. 7. 8. 9. Kumar ve ark. Leukemia 2007; 21: 2035 -42. Sinha ve ark. Leukemia 2012; 26: 1119 -2. Sinha ve ark. Bone Marrow Transplant 2011; 46: 943 -9. Duarte ve ark. Bone Marrow Transplant 2011; 46(Suppl 1): abst. O 377. Nakasone ve ark. Am J Hematol 2009; 84: 809 -14.
Zayıf PKH toplamayı tahmin etme belirteçleri Zayıf PKH toplamayı tahmin için tanımlanmış belirteçler Yaş (yaşlı hastalar)1, 2 Hastalık (daha ileri evre)1 -3 Önceden kemoterapi tedavisi • Yüksek sayıda birincil tedavi aşamaları 1 -4 • Kemoterapi tipi (fludarabin, lenalidomit veya melfalan)1 -5 Önceden radyasyon tedavisi 1, 2 Aferez öncesi periferal kandan düşük CD 34+ hücre sayısı 3, 4, 7 Mobilizasyon öncesi düşük trombosit sayısı 8, 9 Zayıf PKH toplama için muhtemel en güçlü tahmin aracı aferez öncesi periferik kandaki CD 34+ hücre sayısıdır 1, 3, 4, 7 1. 2. 3. 4. | 79 Olivieri ve ark. Bone Marrow Transplant 2012; 47: 342 -51. Perseghin ve ark. Transfus Apher Sci 2009; 41: 33 -7. Sancho ve ark. Cytotherapy 2012; 14: 823 -9. Wuchter ve ark. Biol Blood Marrow Transplant 2010; 16: 490 -9. 5. 6. 7. 8. 9. Kumar ve ark. Leukemia 2007; 21: 2035 -42. Sinha ve ark. Leukemia 2012; 26: 1119 -2. Sinha ve ark. Bone Marrow Transplant 2011; 46: 943 -9. Duarte ve ark. Bone Marrow Transplant 2011; 46(Suppl 1): abst. O 377. Nakasone ve ark. Am J Hematol 2009; 84: 809 -14.
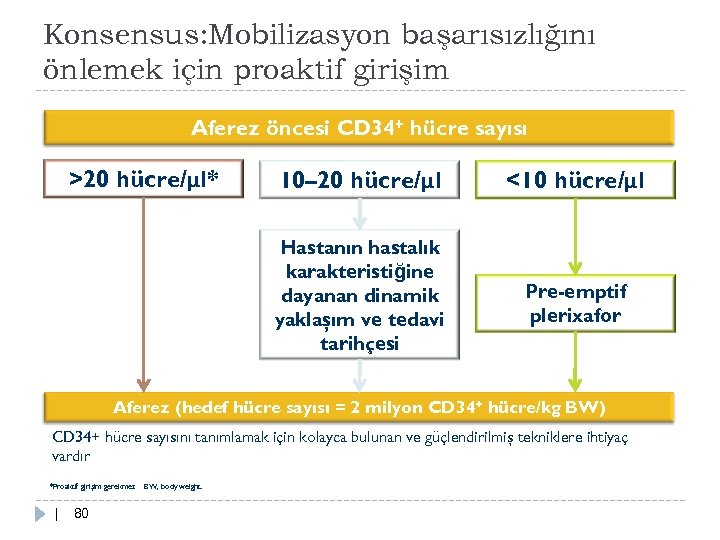 Konsensus: Mobilizasyon başarısızlığını önlemek için proaktif girişim Aferez öncesi CD 34+ hücre sayısı >20 hücre/μl* 10– 20 hücre/μl <10 hücre/μl Hastanın hastalık karakteristiğine dayanan dinamik yaklaşım ve tedavi tarihçesi Pre-emptif plerixafor Aferez (hedef hücre sayısı = 2 milyon CD 34+ hücre/kg BW) CD 34+ hücre sayısını tanımlamak için kolayca bulunan ve güçlendirilmiş tekniklere ihtiyaç vardır *Proaktif girişim gerekmez | 80 BW, body weight.
Konsensus: Mobilizasyon başarısızlığını önlemek için proaktif girişim Aferez öncesi CD 34+ hücre sayısı >20 hücre/μl* 10– 20 hücre/μl <10 hücre/μl Hastanın hastalık karakteristiğine dayanan dinamik yaklaşım ve tedavi tarihçesi Pre-emptif plerixafor Aferez (hedef hücre sayısı = 2 milyon CD 34+ hücre/kg BW) CD 34+ hücre sayısını tanımlamak için kolayca bulunan ve güçlendirilmiş tekniklere ihtiyaç vardır *Proaktif girişim gerekmez | 80 BW, body weight.
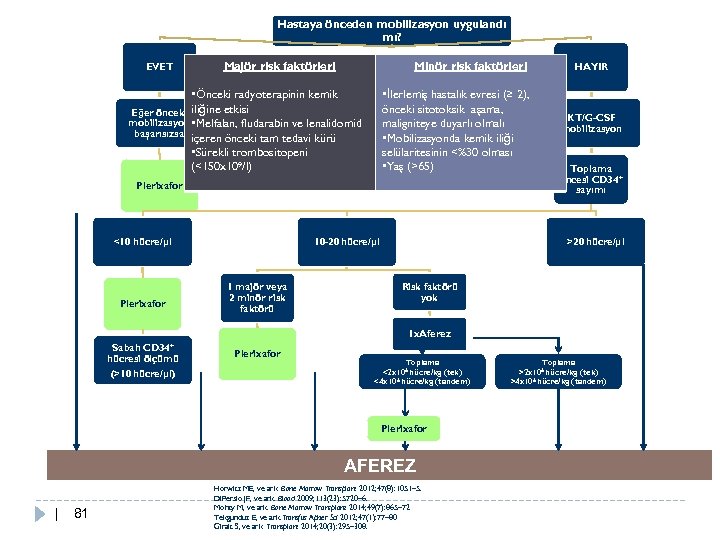 Hastaya önceden mobilizasyon uygulandı mı? EVET Majör risk faktörleri Minör risk faktörleri • Önceki radyoterapinin kemik Eğer önceki iliğine etkisi mobilizasyon • Melfalan, fludarabin ve lenalidomid başarısızsa içeren önceki tam tedavi kürü • Sürekli trombositopeni (<150 x 109/l) • İlerlemiş hastalık evresi (≥ 2), önceki sitotoksik aşama, maligniteye duyarlı olmalı • Mobilizasyonda kemik iliği selülaritesinin <%30 olması • Yaş (>65) Plerixafor <10 hücre/µl Plerixafor 10 -20 hücre/µl 1 majör veya 2 minör risk faktörü HAYIR KT/G-CSF mobilizasyon Toplama öncesi CD 34+ sayımı >20 hücre/µl Risk faktörü yok 1 x. Aferez Sabah CD 34+ hücresi ölçümü (>10 hücre/µl) Plerixafor Toplama <2 x 106 hücre/kg (tek) <4 x 106 hücre/kg (tandem) Plerixafor AFEREZ | 81 Horwitz ME, ve ark. Bone Marrow Transplant 2012; 47(8): 1051– 5. Di. Persio JF, ve ark. Blood 2009; 113(23): 5720– 6. Mohty M, ve ark. Bone Marrow Transplant 2014; 49(7): 865– 72 Tekgunduz E, ve ark. Transfus Apher Sci 2012; 47(1): 77– 80 Giralt S, ve ark. Transplant 2014; 20(3): 295– 308. Toplama >2 x 106 hücre/kg (tek) >4 x 106 hücre/kg (tandem)
Hastaya önceden mobilizasyon uygulandı mı? EVET Majör risk faktörleri Minör risk faktörleri • Önceki radyoterapinin kemik Eğer önceki iliğine etkisi mobilizasyon • Melfalan, fludarabin ve lenalidomid başarısızsa içeren önceki tam tedavi kürü • Sürekli trombositopeni (<150 x 109/l) • İlerlemiş hastalık evresi (≥ 2), önceki sitotoksik aşama, maligniteye duyarlı olmalı • Mobilizasyonda kemik iliği selülaritesinin <%30 olması • Yaş (>65) Plerixafor <10 hücre/µl Plerixafor 10 -20 hücre/µl 1 majör veya 2 minör risk faktörü HAYIR KT/G-CSF mobilizasyon Toplama öncesi CD 34+ sayımı >20 hücre/µl Risk faktörü yok 1 x. Aferez Sabah CD 34+ hücresi ölçümü (>10 hücre/µl) Plerixafor Toplama <2 x 106 hücre/kg (tek) <4 x 106 hücre/kg (tandem) Plerixafor AFEREZ | 81 Horwitz ME, ve ark. Bone Marrow Transplant 2012; 47(8): 1051– 5. Di. Persio JF, ve ark. Blood 2009; 113(23): 5720– 6. Mohty M, ve ark. Bone Marrow Transplant 2014; 49(7): 865– 72 Tekgunduz E, ve ark. Transfus Apher Sci 2012; 47(1): 77– 80 Giralt S, ve ark. Transplant 2014; 20(3): 295– 308. Toplama >2 x 106 hücre/kg (tek) >4 x 106 hücre/kg (tandem)
 Sonuçlar PKHN her bir hasta için uyarlanan uygun stratejilerle optimize edilebilir hastalık ve tedavi özellikleri temeline dayanan bireysel toplama hedefi olmalıdır Zayıf PKH toplama için aferez öncesi düşük CD 34+ hücre sayısı ideal bir tahmin aracıdır CD 34+ hücre sayısının belirlenmesi önerilir | hastalar için risk olan zayıf PKH toplama öngörülebilir mobilizasyon başarısızlığını önlemek için proaktif davranılabilir 82
Sonuçlar PKHN her bir hasta için uyarlanan uygun stratejilerle optimize edilebilir hastalık ve tedavi özellikleri temeline dayanan bireysel toplama hedefi olmalıdır Zayıf PKH toplama için aferez öncesi düşük CD 34+ hücre sayısı ideal bir tahmin aracıdır CD 34+ hücre sayısının belirlenmesi önerilir | hastalar için risk olan zayıf PKH toplama öngörülebilir mobilizasyon başarısızlığını önlemek için proaktif davranılabilir 82
 Endikasyon ve kullanım Mozobil™ (plerixafor), granulosit kolon stimülasyon faktörleri (G-CSF) ile birlikte kombine kullanılarak, hematopoetik kök hücreleri periferik kana mobilize etmekte ve non-Hodgkin lenfoma (NHL) ve multipl miyelom (MM)’lu hastalarda bir sonraki otolog transplantasyonunda endikedir. Her bir tek kullanımlık flakon, 24 mg plerixafor içerecek şekilde 1. 2 ml’de 20 mg/ml olarak doldurulmuştur. ≤ 83 kg: 20 mg doz veya 0. 24 mg/kg > 83 kg: 0. 24 mg/kg
Endikasyon ve kullanım Mozobil™ (plerixafor), granulosit kolon stimülasyon faktörleri (G-CSF) ile birlikte kombine kullanılarak, hematopoetik kök hücreleri periferik kana mobilize etmekte ve non-Hodgkin lenfoma (NHL) ve multipl miyelom (MM)’lu hastalarda bir sonraki otolog transplantasyonunda endikedir. Her bir tek kullanımlık flakon, 24 mg plerixafor içerecek şekilde 1. 2 ml’de 20 mg/ml olarak doldurulmuştur. ≤ 83 kg: 20 mg doz veya 0. 24 mg/kg > 83 kg: 0. 24 mg/kg
 Plerixafor ile ● Artmış mobilizasyon & otolog transplantasyon için optimum CD 34+ hücre toplanması sağlanır ● ● ● Daha az aferez prosedürleri gerektirir Kök hücre mobilizasyon ve aferez zamanını tahmin edebilmeyi sağlar Başarılı ve dayanıklı graft sağlar Plerixafor ile Artmış etkinlik ve var olan medikal kaynakların optimum kullanımı sağlanır | 84
Plerixafor ile ● Artmış mobilizasyon & otolog transplantasyon için optimum CD 34+ hücre toplanması sağlanır ● ● ● Daha az aferez prosedürleri gerektirir Kök hücre mobilizasyon ve aferez zamanını tahmin edebilmeyi sağlar Başarılı ve dayanıklı graft sağlar Plerixafor ile Artmış etkinlik ve var olan medikal kaynakların optimum kullanımı sağlanır | 84
 TEŞEKKÜRLER | 85
TEŞEKKÜRLER | 85
