02 - Гомогенный катализ.pptx
- Количество слайдов: 26
 Гомогенный катализ
Гомогенный катализ
 Гомогенный катализ – процесс, в котором реагенты и катализатор находятся в одной фазе. Гомогенный катализ протекает в жидкой и значительно реже в газовой фазе. Различают кислотный (основной), металлокомплексный и фермента тивный виды гомогенного катализа. Гомогенный катализ наиболее распространён в производстве органи ческих соединений.
Гомогенный катализ – процесс, в котором реагенты и катализатор находятся в одной фазе. Гомогенный катализ протекает в жидкой и значительно реже в газовой фазе. Различают кислотный (основной), металлокомплексный и фермента тивный виды гомогенного катализа. Гомогенный катализ наиболее распространён в производстве органи ческих соединений.
 Реакции в растворах часто ускоряются в присутствии веществ, относя щихся к разновидностям кислот и оснований, названных именами Арре ниуса, Льюиса, Бренстеда. По Аррениусу, кислота – соединение, дающее при диссоциации в во де катионы Н+, а основание – анионы ОН–. По Бренстеду, кислота – вещество, являющееся донором протона, а основание – акцептором протона. По Льюису, кислота – это акцептор неподелённой пары электронов, а основание – вещество, являющееся донором неподелённой пары элект ронов, которая может быть использована для образования устойчивой электронной конфигурации другого атома. Реакции, катализируемые кислотами и основаниями: – специфический кислотный или основной катализ, – общий кислотный или основной катализ, – электрофильный или нуклеофильный катализ.
Реакции в растворах часто ускоряются в присутствии веществ, относя щихся к разновидностям кислот и оснований, названных именами Арре ниуса, Льюиса, Бренстеда. По Аррениусу, кислота – соединение, дающее при диссоциации в во де катионы Н+, а основание – анионы ОН–. По Бренстеду, кислота – вещество, являющееся донором протона, а основание – акцептором протона. По Льюису, кислота – это акцептор неподелённой пары электронов, а основание – вещество, являющееся донором неподелённой пары элект ронов, которая может быть использована для образования устойчивой электронной конфигурации другого атома. Реакции, катализируемые кислотами и основаниями: – специфический кислотный или основной катализ, – общий кислотный или основной катализ, – электрофильный или нуклеофильный катализ.
 Специфический кислотный катализ Катализаторами являются кислоты Аррениуса – ионы Н 3 О+: S + Н 3 О+ ↔ SH+ + H 2 O → P + Н 3 О+ Первая стадия – внедрение протона в реагирующую часть молекулы субстрата – протекает быстро. Вторая стадия, в которой образовавшийся катион SН+ отщепляет про тон с образованием продукта, протекает медленно и является лимити рующей стадией процесса.
Специфический кислотный катализ Катализаторами являются кислоты Аррениуса – ионы Н 3 О+: S + Н 3 О+ ↔ SH+ + H 2 O → P + Н 3 О+ Первая стадия – внедрение протона в реагирующую часть молекулы субстрата – протекает быстро. Вторая стадия, в которой образовавшийся катион SН+ отщепляет про тон с образованием продукта, протекает медленно и является лимити рующей стадией процесса.
 Специфический основной катализ Катализаторами являются основания Аррениуса – ионы ОН–: SH + ОН– ↔ S– + H 2 O → S* + OH– → P + OH– Первая стадия быстрая Вторая – медленная, лимитирующая весь процесс.
Специфический основной катализ Катализаторами являются основания Аррениуса – ионы ОН–: SH + ОН– ↔ S– + H 2 O → S* + OH– → P + OH– Первая стадия быстрая Вторая – медленная, лимитирующая весь процесс.
 Общий кислотный катализ Отличается от специфического тем, что здесь катализаторами про цесса служат кислоты Бренстеда (НА), т. е. ион Н 3 О+ не является донором процесса, и реакция идет по схеме: S + HA → SH+ + A– → P + HA Лимитирующей является первая стадия процесса – образование иона SH+.
Общий кислотный катализ Отличается от специфического тем, что здесь катализаторами про цесса служат кислоты Бренстеда (НА), т. е. ион Н 3 О+ не является донором процесса, и реакция идет по схеме: S + HA → SH+ + A– → P + HA Лимитирующей является первая стадия процесса – образование иона SH+.
 Общий основной катализ Катализаторами процесса выступают основания Бренстеда (В), т. е. акцептором протона не является анион OH–: SH + B → S– +BH+ → S* + B → P + B Самой медленной стадией является образование активного аниона.
Общий основной катализ Катализаторами процесса выступают основания Бренстеда (В), т. е. акцептором протона не является анион OH–: SH + B → S– +BH+ → S* + B → P + B Самой медленной стадией является образование активного аниона.
 Электрофильный катализ заключается в активации реагента апро тонной кислотой, при этом получается активированная частица, которая при взаимодействии с другим реагентом превращается в продукт реакции с регенерацией катализатора. Катализаторами служат кислоты Льюиса – Al. Cl 3, Fe. Cl 3, Cu. Cl 2, Al. Br 3, BF 3. Роль кислот Льюиса как катализаторов – образование за счёт донорно акцепторной связи промежуточного соединения с одним реагентом, кото рое более легко вступает в реакцию с молекулами второго реагента.
Электрофильный катализ заключается в активации реагента апро тонной кислотой, при этом получается активированная частица, которая при взаимодействии с другим реагентом превращается в продукт реакции с регенерацией катализатора. Катализаторами служат кислоты Льюиса – Al. Cl 3, Fe. Cl 3, Cu. Cl 2, Al. Br 3, BF 3. Роль кислот Льюиса как катализаторов – образование за счёт донорно акцепторной связи промежуточного соединения с одним реагентом, кото рое более легко вступает в реакцию с молекулами второго реагента.
 Электрофильный катализ Пример: каталитическое хлорирование этилена в присутствии Fe. Cl 3 :
Электрофильный катализ Пример: каталитическое хлорирование этилена в присутствии Fe. Cl 3 :
 Металлокомплексный катализ Ионы металлов имеют ряд преимуществ перед протоном. Больший заряд ионов металлов позволяет им связываться не с одним, а с двумя и более донорными атомами молекул реагента и тем самым обеспечивать более высокую степень их поляризации. Кроме того, каталитические функции ионов металлов сохраняются в средах с очень низкой концентрацией протонов. Ещё одно их преимущество состоит в специфичности действия, обус ловленной особенностями электронной конфигурации, лигандным соста вом и структурой координационной сферы.
Металлокомплексный катализ Ионы металлов имеют ряд преимуществ перед протоном. Больший заряд ионов металлов позволяет им связываться не с одним, а с двумя и более донорными атомами молекул реагента и тем самым обеспечивать более высокую степень их поляризации. Кроме того, каталитические функции ионов металлов сохраняются в средах с очень низкой концентрацией протонов. Ещё одно их преимущество состоит в специфичности действия, обус ловленной особенностями электронной конфигурации, лигандным соста вом и структурой координационной сферы.
 Металлокомплексный катализ Особенности поведения ионов металлов явились основой для разработки нового класса гомогенных катализаторов – растворимых в реакционных сре дах соединений переходных металлов. Основная группа таких металлов имеет частично заполненные d орбитали. Эти орбитали выходят за периферию атомов или ионов, что способствует об разованию связей различной симметрии между металлом и его окружением. Среди них наиболее интересны соединения металлов, растворимые в ор ганических средах (комплексные соединения и соли).
Металлокомплексный катализ Особенности поведения ионов металлов явились основой для разработки нового класса гомогенных катализаторов – растворимых в реакционных сре дах соединений переходных металлов. Основная группа таких металлов имеет частично заполненные d орбитали. Эти орбитали выходят за периферию атомов или ионов, что способствует об разованию связей различной симметрии между металлом и его окружением. Среди них наиболее интересны соединения металлов, растворимые в ор ганических средах (комплексные соединения и соли).
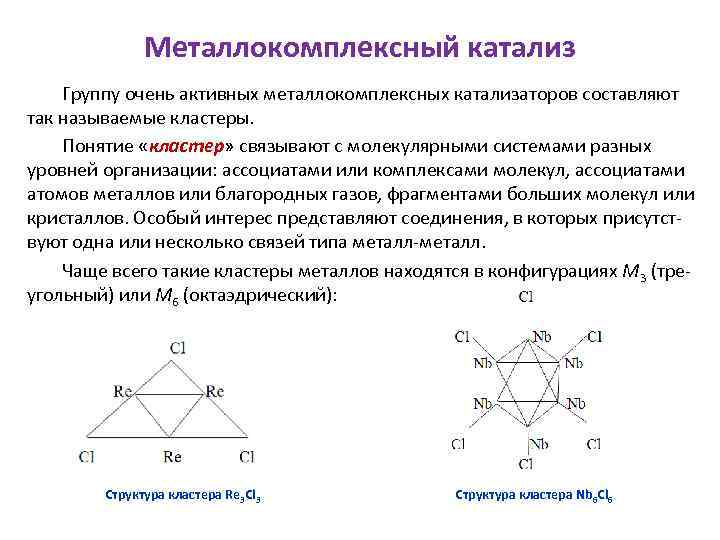 Металлокомплексный катализ Группу очень активных металлокомплексных катализаторов составляют так называемые кластеры. Понятие «кластер» связывают с молекулярными системами разных уровней организации: ассоциатами или комплексами молекул, ассоциатами атомов металлов или благородных газов, фрагментами больших молекул или кристаллов. Особый интерес представляют соединения, в которых присутст вуют одна или несколько связей типа металл. Чаще всего такие кластеры металлов находятся в конфигурациях М 3 (тре угольный) или М 6 (октаэдрический): Структура кластера Re 3 Cl 3 Структура кластера Nb 6 Cl 6
Металлокомплексный катализ Группу очень активных металлокомплексных катализаторов составляют так называемые кластеры. Понятие «кластер» связывают с молекулярными системами разных уровней организации: ассоциатами или комплексами молекул, ассоциатами атомов металлов или благородных газов, фрагментами больших молекул или кристаллов. Особый интерес представляют соединения, в которых присутст вуют одна или несколько связей типа металл. Чаще всего такие кластеры металлов находятся в конфигурациях М 3 (тре угольный) или М 6 (октаэдрический): Структура кластера Re 3 Cl 3 Структура кластера Nb 6 Cl 6
 Металлокомплексный катализ Высокая каталитическая активность кластеров обусловлена прежде всего многоточечным контактом атомов металла с молекулой субстрата и закреплением последнего в наиболее благоприятной для реакции кон формации, а также возможностью координации нескольких молекул дву мя соседними металлическими центрами и осуществления многоэлек тронных реакций, благодаря высокой проводимости металлической свя зи. По этим причинам кластеры проявляют во многих химических реак циях уникальные каталитические свойства, несвойственные одноядер ным частицам. Особый интерес в катализе представляют гетероядерные кластеры.
Металлокомплексный катализ Высокая каталитическая активность кластеров обусловлена прежде всего многоточечным контактом атомов металла с молекулой субстрата и закреплением последнего в наиболее благоприятной для реакции кон формации, а также возможностью координации нескольких молекул дву мя соседними металлическими центрами и осуществления многоэлек тронных реакций, благодаря высокой проводимости металлической свя зи. По этим причинам кластеры проявляют во многих химических реак циях уникальные каталитические свойства, несвойственные одноядер ным частицам. Особый интерес в катализе представляют гетероядерные кластеры.
 Металлокомплексный катализ При разработке технологии гомогенно каталитической реакции часто предпочтение отдают не отдельному катализатору, а каталитической сис теме, включающей собственно катализатор и один или несколько актива торов. Активатором называют вещество с собственной каталитической активностью или без неё, добавка которого в небольшом количестве к основному катализатору существенно повышает его активность. Применение активаторов в гомогенном катализе позволяет снизить себестоимость продукции за счёт увеличения скорости и селективности процесса, уменьшения давления и температуры синтеза.
Металлокомплексный катализ При разработке технологии гомогенно каталитической реакции часто предпочтение отдают не отдельному катализатору, а каталитической сис теме, включающей собственно катализатор и один или несколько актива торов. Активатором называют вещество с собственной каталитической активностью или без неё, добавка которого в небольшом количестве к основному катализатору существенно повышает его активность. Применение активаторов в гомогенном катализе позволяет снизить себестоимость продукции за счёт увеличения скорости и селективности процесса, уменьшения давления и температуры синтеза.
 Ферментативный катализ Катализ осуществляется с помощью ферментов – белковых образо ваний, в которых рабочей частью является активный центр, представля ющий собой гидрофильно гидрофобную полость ( «карман» ), образо ванную полипептидными фрагментами белковой молекулы и боковыми цепями остатков аминокислот. Около 30 % известных в настоящее время ферментов содержат в ка честве активного центра ионы металлов постоянной или переменной ва лентности, которые образуют с молекулами белка ряд комплексов, отли чающихся степенью лабильности. В качестве таких металлов могут присутствовать железо, цинк, медь, марганец, кальций, кобальт и другие. Ферменты обладают огромной активностью, превышающей на не сколько порядков активность известных катализаторов. При этом отме чено, что они обеспечивают протекание химических реакций в мягких условиях: практически при комнатной температуре и атмосферном дав лении.
Ферментативный катализ Катализ осуществляется с помощью ферментов – белковых образо ваний, в которых рабочей частью является активный центр, представля ющий собой гидрофильно гидрофобную полость ( «карман» ), образо ванную полипептидными фрагментами белковой молекулы и боковыми цепями остатков аминокислот. Около 30 % известных в настоящее время ферментов содержат в ка честве активного центра ионы металлов постоянной или переменной ва лентности, которые образуют с молекулами белка ряд комплексов, отли чающихся степенью лабильности. В качестве таких металлов могут присутствовать железо, цинк, медь, марганец, кальций, кобальт и другие. Ферменты обладают огромной активностью, превышающей на не сколько порядков активность известных катализаторов. При этом отме чено, что они обеспечивают протекание химических реакций в мягких условиях: практически при комнатной температуре и атмосферном дав лении.
 Ферментативный катализ •
Ферментативный катализ •
 Ферментативный катализ •
Ферментативный катализ •
 Ферментативный катализ Принципиальное отличие ферментов от других катализаторов связано прежде всего со специфичностью их действия. Различают четыре типа спе ци фичности ействия ферментов. д Абсолютная специфичность, когда фермент ускоряет превращение только одного вещества или одной пары субстратов (для бимолекулярной реакции) в соответствующие продукты. Без абсолютной специфичности большинства ферментов существующая форма жизни была бы невозможна, поскольку в клетке существуют различные функционально близкие суб страты, претерпевающие совершенно разные превращения. Абсолютно-групповая специфичность, когда фермент катализирует превращения определённой группы веществ.
Ферментативный катализ Принципиальное отличие ферментов от других катализаторов связано прежде всего со специфичностью их действия. Различают четыре типа спе ци фичности ействия ферментов. д Абсолютная специфичность, когда фермент ускоряет превращение только одного вещества или одной пары субстратов (для бимолекулярной реакции) в соответствующие продукты. Без абсолютной специфичности большинства ферментов существующая форма жизни была бы невозможна, поскольку в клетке существуют различные функционально близкие суб страты, претерпевающие совершенно разные превращения. Абсолютно-групповая специфичность, когда фермент катализирует превращения определённой группы веществ.
 Ферментативный катализ Относительная групповая специфичность, при которой каталитическое действие фермента проявляется не к группе веществ, а только к её части (на пример, пероксидазы специфичны только к пероксиду водорода, но не очень чувствительны к природе окисляемых субстратов, если они являются арома тическими полифенолами). Стереохимическая специфичность, когда фермент способен отличать свой субстрат от его оптического изомера. Тогда название фермента содержит буквы D или L. Такой фермент абсолютно стереоспецифичен. Это означает, что адсорбционный участок такого фермента строго комплиментарен избран ному субстрату. Важно отметить, что второй стереоизомер вообще не спосо бен соединяться с ферментом, либо, если такое связывание и происходит, он является конкурентным ингибитором. Это свойство ферментов называют так же энантиоселективностью, а молекулы, синтезируемые с помощью их, на зывают энантиомерами.
Ферментативный катализ Относительная групповая специфичность, при которой каталитическое действие фермента проявляется не к группе веществ, а только к её части (на пример, пероксидазы специфичны только к пероксиду водорода, но не очень чувствительны к природе окисляемых субстратов, если они являются арома тическими полифенолами). Стереохимическая специфичность, когда фермент способен отличать свой субстрат от его оптического изомера. Тогда название фермента содержит буквы D или L. Такой фермент абсолютно стереоспецифичен. Это означает, что адсорбционный участок такого фермента строго комплиментарен избран ному субстрату. Важно отметить, что второй стереоизомер вообще не спосо бен соединяться с ферментом, либо, если такое связывание и происходит, он является конкурентным ингибитором. Это свойство ферментов называют так же энантиоселективностью, а молекулы, синтезируемые с помощью их, на зывают энантиомерами.
 Ферментативный катализ Ø Ø Ø Причины высокой активности ферментативного катализа: сближение реагентов при сорбции их в активном центре, этот фактор эк вивалентен повышению концентрации реагирующих веществ; специфическая ориентация сорбированного в активном центре субстрата, благоприятная для взаимодействия с каталитическим участком активного центра; образование химических связей между субстратом и каталитическим участком активного центра, направляющее реакцию по энергетически наиболее лёгкому пути; осуществление всех основных химических превращений субстрата «вну тримолекулярно» – в составе фермент субстратного комплекса; исключительная гибкость молекулы фермента, позволяющая активному центру принимать на каждой стадии превращения фермент субстратного комплекса строение, способствующее достижению максимальной ско рости данной стадии реакции.
Ферментативный катализ Ø Ø Ø Причины высокой активности ферментативного катализа: сближение реагентов при сорбции их в активном центре, этот фактор эк вивалентен повышению концентрации реагирующих веществ; специфическая ориентация сорбированного в активном центре субстрата, благоприятная для взаимодействия с каталитическим участком активного центра; образование химических связей между субстратом и каталитическим участком активного центра, направляющее реакцию по энергетически наиболее лёгкому пути; осуществление всех основных химических превращений субстрата «вну тримолекулярно» – в составе фермент субстратного комплекса; исключительная гибкость молекулы фермента, позволяющая активному центру принимать на каждой стадии превращения фермент субстратного комплекса строение, способствующее достижению максимальной ско рости данной стадии реакции.
 Ферментативный катализ Иногда течение ферментативной реакции осложняется присутствием ингибиторов – веществ, способных образовывать комплексы с ферментом или фермент субстратным комплексом. Различают конкурентное, неконкурентное и смешанное ингибиро вание.
Ферментативный катализ Иногда течение ферментативной реакции осложняется присутствием ингибиторов – веществ, способных образовывать комплексы с ферментом или фермент субстратным комплексом. Различают конкурентное, неконкурентное и смешанное ингибиро вание.
 Ферментативный катализ •
Ферментативный катализ •
 Ферментативный катализ •
Ферментативный катализ •
 Ферментативный катализ •
Ферментативный катализ •
 Ферментативный катализ • Смешанное ингибирование описывается более сложными кинетически ми схемами. При смешанном ингибировании изменяются и константа Ми хаэлиса, и максимальная скорость ферментативной реакции.
Ферментативный катализ • Смешанное ингибирование описывается более сложными кинетически ми схемами. При смешанном ингибировании изменяются и константа Ми хаэлиса, и максимальная скорость ферментативной реакции.
 Ферментативный катализ Ферменты широко применяются в биосинтезе для создания ряда про дуктов с разнообразным спектром потребительских свойств: Ø медикаментов – инсулина, интерферона, витаминов, гормональных препаратов, антибиотиков; Ø пищевых добавок – кормового и пищевого белков, простейших сахаров, глюкозы, фруктозы, антиоксидантов, ароматизаторов; Ø биоэнергетиков – спирта, водорода, биогенных углеводородов, фер ментных электродов; Ø биополимеров – полимеров, способных разлагаться под воздействием природных микроорганизмов, приближающихся по свойствам к полу ченным обычным химическим путем.
Ферментативный катализ Ферменты широко применяются в биосинтезе для создания ряда про дуктов с разнообразным спектром потребительских свойств: Ø медикаментов – инсулина, интерферона, витаминов, гормональных препаратов, антибиотиков; Ø пищевых добавок – кормового и пищевого белков, простейших сахаров, глюкозы, фруктозы, антиоксидантов, ароматизаторов; Ø биоэнергетиков – спирта, водорода, биогенных углеводородов, фер ментных электродов; Ø биополимеров – полимеров, способных разлагаться под воздействием природных микроорганизмов, приближающихся по свойствам к полу ченным обычным химическим путем.


