Гидролиз солей.ppt
- Количество слайдов: 20

Гидролиз солей
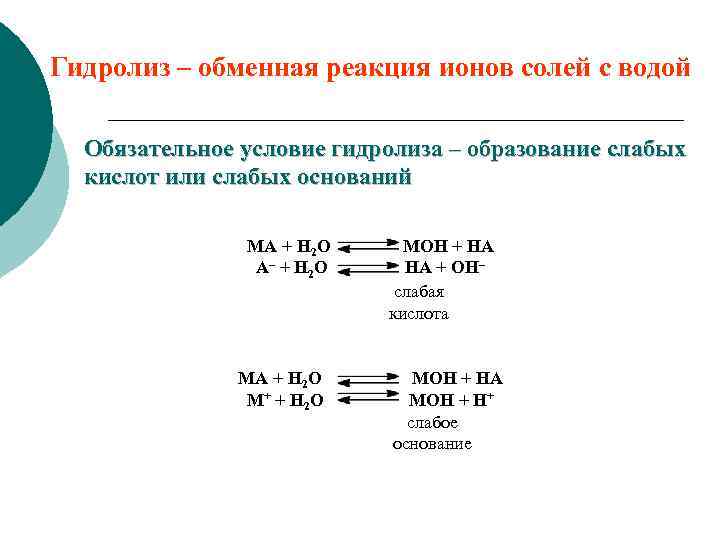
Гидролиз – обменная реакция ионов солей с водой Обязательное условие гидролиза – образование слабых кислот или слабых оснований MA + H 2 O A– + H 2 O MA + H 2 O M+ + H 2 O MOH + HA HA + OH– слабая кислота MOH + HA MOH + H+ слабое основание

Типы гидролиза Гидролиз по катиону ¡ Гидролиз по аниону ¡ Гидролиз и по аниону и по катиону ¡
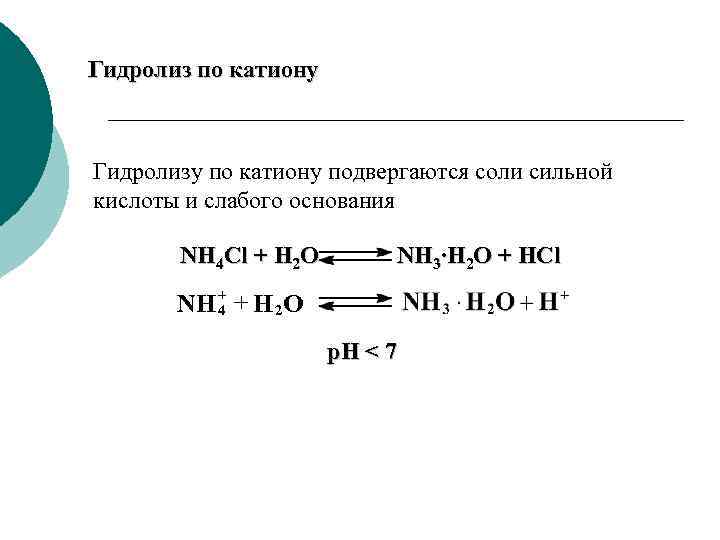
Гидролиз по катиону Гидролизу по катиону подвергаются соли сильной кислоты и слабого основания NH 4 Cl + H 2 O NH 3∙H 2 O + HCl + NH 4 + H 2 O p. H < 7

Гидролиз по аниону Гидролизу по аниону подвергаются соли слабой кислоты и сильного основания Na 3 PO 4 + H 2 O Na. H 2 PO 4 + Na. OH p. H > 7

Гидролиз и по катиону и по аниону Гидролизу и по катиону и по аниону подвергаются соли, образованные слабыми кислотами и основаниями ¡ Гидролиз таких солей протекает глубже, чем при гидролизе соли только по катиону или только по аниону ¡

Гидролиз и по катиону и по аниону (NH 4)2 S + H 2 O NH 3∙H 2 O + NH 4 HS p. Ka(HS-) = 14. 7; p. Kb(NH 3∙H 2 O) = 4. 75 p. H > 7 Чем слабее кислота или основание, тем сильнее гидролизуются их соли

Гидролиз и по катиону и по аниону Необратимый гидролиз – частный случай гидролиза и по катиону и по аниону (наблюдается редко) Al 2 S 3 + 6 H 2 O 2 Al(OH)3↓ + 3 H 2 S↑ Cr 2 S 3 + 6 H 2 O 2 Cr(OH)3 ↓ + 3 H 2 S↑

Совместный гидролиз Одна из солей гидролизуется по катиону, а другая ― по аниону. ¡ Совместному гидролизу подвергаются соли металлов со степенями окисления +II или +III. ¡ Совместный гидролиз практически необратим, так как образующиеся при этом ионы H+ и OH– превращаются в молекулы слабого электролита ― воды. ¡

Примеры совместного гидролиза M+ + H 2 O MOH + H+ A – + H 2 O HA + OH– H+ + OH– H 2 O 2 Cr. Cl 3 + 3 Na 2 CO 3 + 3 H 2 O = 2 Cr(OH)3 + 3 CO 2 + 6 Na. Cl 2 Al. Cl 3 + 3 Na 2 S + 6 H 2 O = 2 Al(OH)3 + 3 H 2 S + 6 Na. Cl 2 Cu. Cl 2 + 2 Na 2 CO 3 + H 2 O = (Cu. OH)2 CO 3 + CO 2 + 4 Na. Cl

Количественные характеристики гидролиза Степень гидролиза ¡ Константа гидролиза ¡

Степень гидролиза Nh ― число ионов, подвергшихся гидролизу; N ― число ионов, способных к гидролизу αh = 0 ÷ 1 В большинстве случаев степень гидролиза мала. Так, при молярной концентрации NH 4 Cl 0, 01% αh < 0, 01%
![Константа гидролиза по аниону CN– + H 2 O [H 2 O] = 55, Константа гидролиза по аниону CN– + H 2 O [H 2 O] = 55,](https://present5.com/presentation/3/138190540_138046187.pdf-img/138190540_138046187.pdf-13.jpg)
Константа гидролиза по аниону CN– + H 2 O [H 2 O] = 55, 5 моль/л HCN + OH–

Константа гидролиза по катиону NH 4+ + H 2 O NH 3∙H 2 O + H+

Константа гидролиза по катиону и аниону

Степень гидролиза и константа гидролиза c(MA) – аналитическая концентрация соли, моль/л

Степень гидролиза и константа гидролиза Если αh << 1, то Тогда

Степень гидролиза и константа гидролиза При гидролизе соли по аниону При гидролизе соли по катиону При гидролизе соли по аниону и катиону

Факторы, влияющие на степень гидролиза соли С увеличением Ka (Kb) степень гидролиза соли уменьшается ¡ С увеличением концентрации соли в растворе степень гидролиза соли уменьшается ¡ С увеличением температуры степень гидролиза соли увеличивается (увеличивается Kw) ¡

Факторы, влияющие на степень гидролиза соли Добавки кислот ¡ Добавки щелочей ¡ Добавки солей ¡
Гидролиз солей.ppt