12_Гетерофункциональные соединения.pptx
- Количество слайдов: 31
 Гетерофункциональные соединения
Гетерофункциональные соединения
 1. Гидроксикислоты (OH + COOH) 2. Оксокислоты (C=O + COOH) 3. Аминокислоты (NH 2 + COOH) 4. Гидроксиальдегиды и гидроксикетоны (OH + C=O) 2
1. Гидроксикислоты (OH + COOH) 2. Оксокислоты (C=O + COOH) 3. Аминокислоты (NH 2 + COOH) 4. Гидроксиальдегиды и гидроксикетоны (OH + C=O) 2
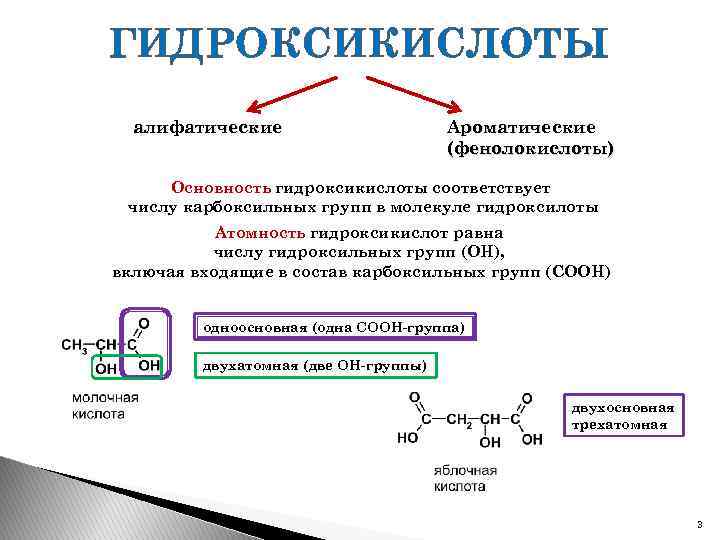 ГИДРОКСИКИСЛОТЫ алифатические Ароматические (фенолокислоты) Основность гидроксикислоты соответствует числу карбоксильных групп в молекуле гидроксилоты Атомность гидроксикислот равна числу гидроксильных групп (ОН), включая входящие в состав карбоксильных групп (СООН) одноосновная (одна СООН-группа) двухатомная (две ОН-группы) двухосновная трехатомная 3
ГИДРОКСИКИСЛОТЫ алифатические Ароматические (фенолокислоты) Основность гидроксикислоты соответствует числу карбоксильных групп в молекуле гидроксилоты Атомность гидроксикислот равна числу гидроксильных групп (ОН), включая входящие в состав карбоксильных групп (СООН) одноосновная (одна СООН-группа) двухатомная (две ОН-группы) двухосновная трехатомная 3
 По взаимному расположению функциональных групп различают: -α-гидроксикислоты; -β-гидроксикислоты; -γ - и δ-гидроксикислоты. 4
По взаимному расположению функциональных групп различают: -α-гидроксикислоты; -β-гидроксикислоты; -γ - и δ-гидроксикислоты. 4
 Изомерия - Структурная (изомерия УВ скелета, изомерия положения функциональной группы) - Стереоизомерия - энантиомерия 5
Изомерия - Структурная (изомерия УВ скелета, изомерия положения функциональной группы) - Стереоизомерия - энантиомерия 5
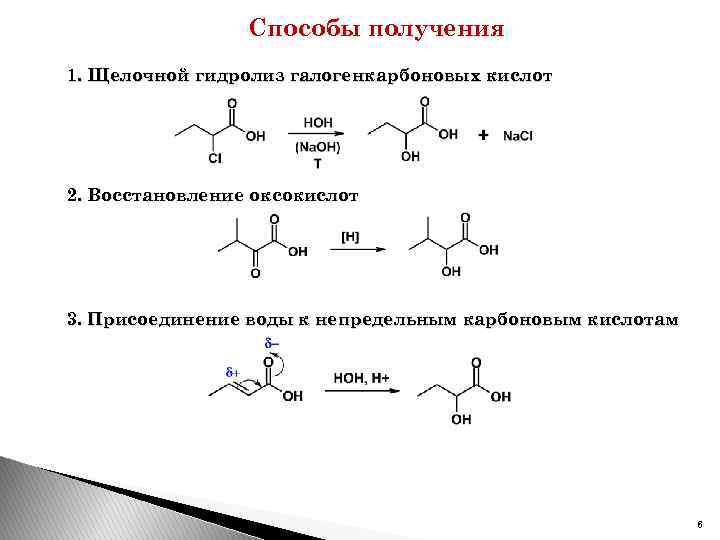 Способы получения 1. Щелочной гидролиз галогенкарбоновых кислот 2. Восстановление оксокислот 3. Присоединение воды к непредельным карбоновым кислотам 6
Способы получения 1. Щелочной гидролиз галогенкарбоновых кислот 2. Восстановление оксокислот 3. Присоединение воды к непредельным карбоновым кислотам 6
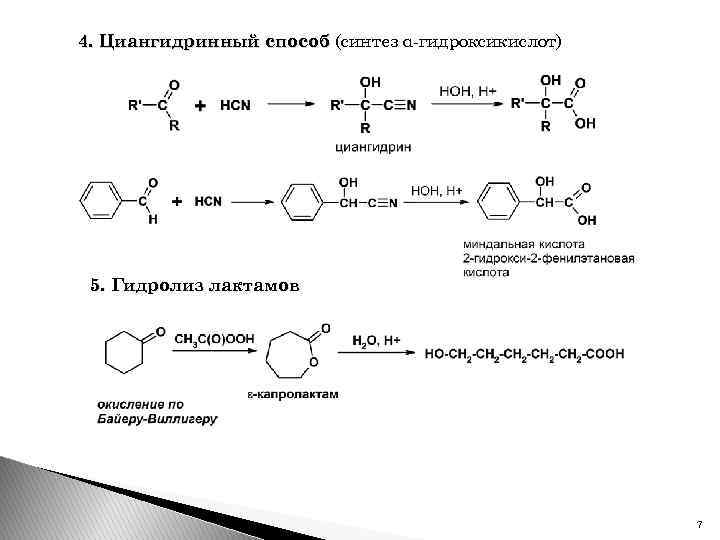 4. Циангидринный способ (синтез α-гидроксикислот) 5. Гидролиз лактамов 7
4. Циангидринный способ (синтез α-гидроксикислот) 5. Гидролиз лактамов 7
 Химические свойства 1. Реакции по гидроксильной группе 2. Реакции с участием карбоксильной группы 3. Специфические реакции гидроксикислот 8
Химические свойства 1. Реакции по гидроксильной группе 2. Реакции с участием карбоксильной группы 3. Специфические реакции гидроксикислот 8
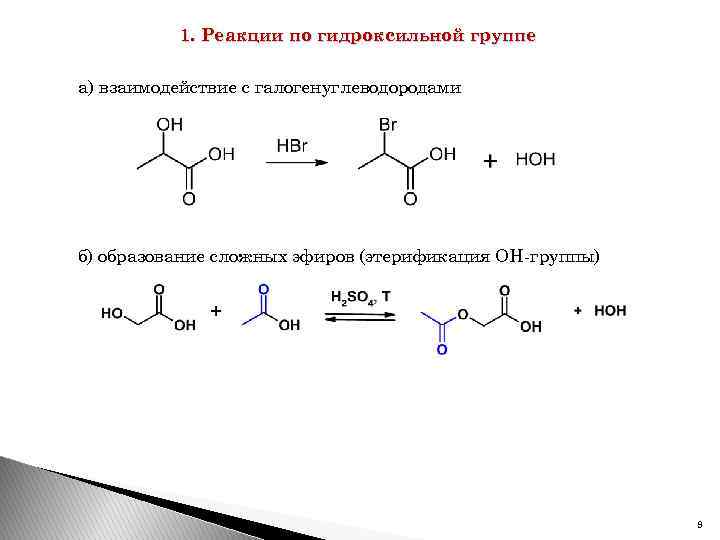 1. Реакции по гидроксильной группе а) взаимодействие с галогенуглеводородами б) образование сложных эфиров (этерификация ОН-группы) 9
1. Реакции по гидроксильной группе а) взаимодействие с галогенуглеводородами б) образование сложных эфиров (этерификация ОН-группы) 9
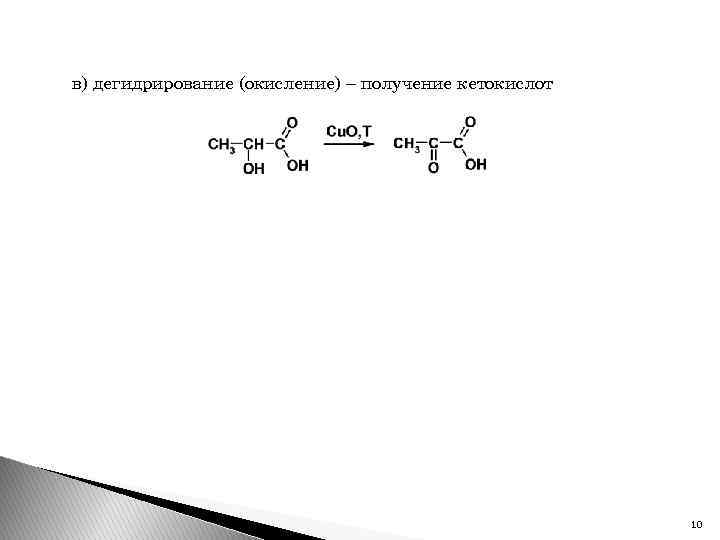 в) дегидрирование (окисление) – получение кетокислот 10
в) дегидрирование (окисление) – получение кетокислот 10
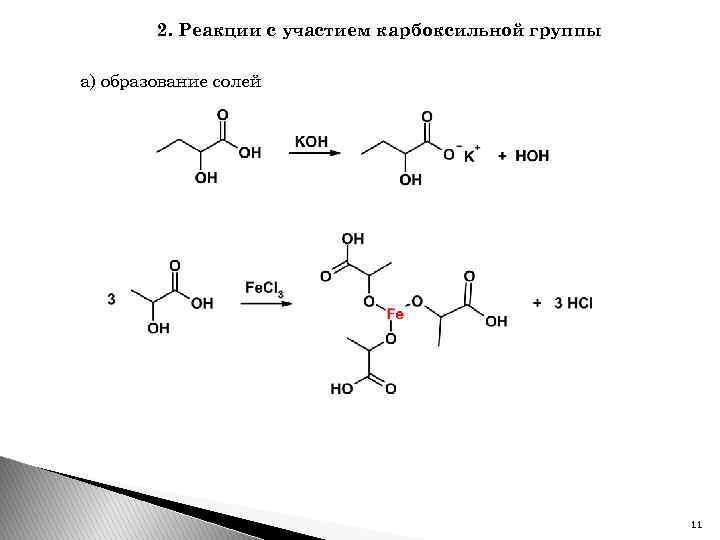 2. Реакции с участием карбоксильной группы а) образование солей 11
2. Реакции с участием карбоксильной группы а) образование солей 11
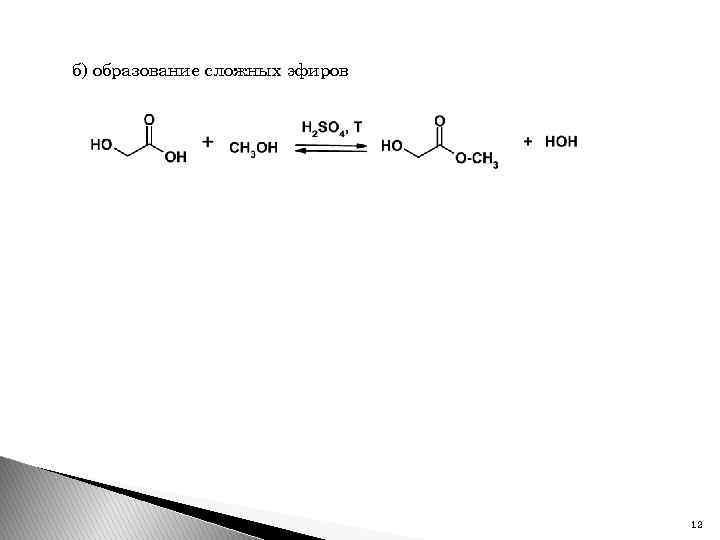 б) образование сложных эфиров 12
б) образование сложных эфиров 12
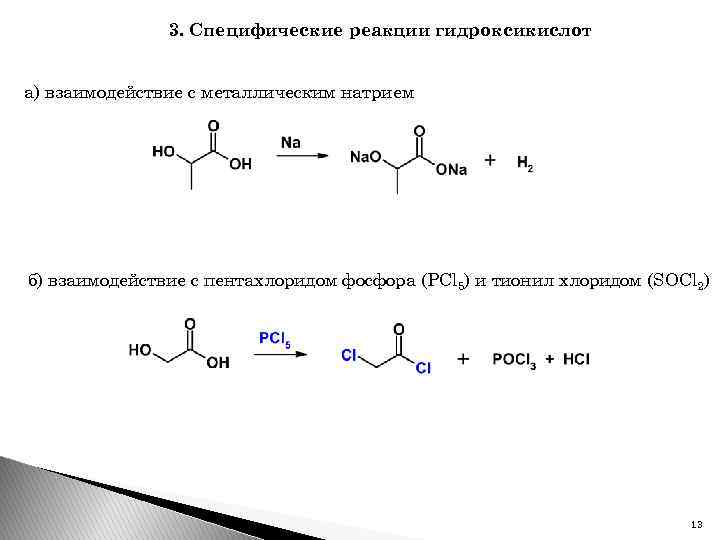 3. Специфические реакции гидроксикислот а) взаимодействие с металлическим натрием б) взаимодействие с пентахлоридом фосфора (PCl 5) и тионил хлоридом (SOCl 2) 13
3. Специфические реакции гидроксикислот а) взаимодействие с металлическим натрием б) взаимодействие с пентахлоридом фосфора (PCl 5) и тионил хлоридом (SOCl 2) 13
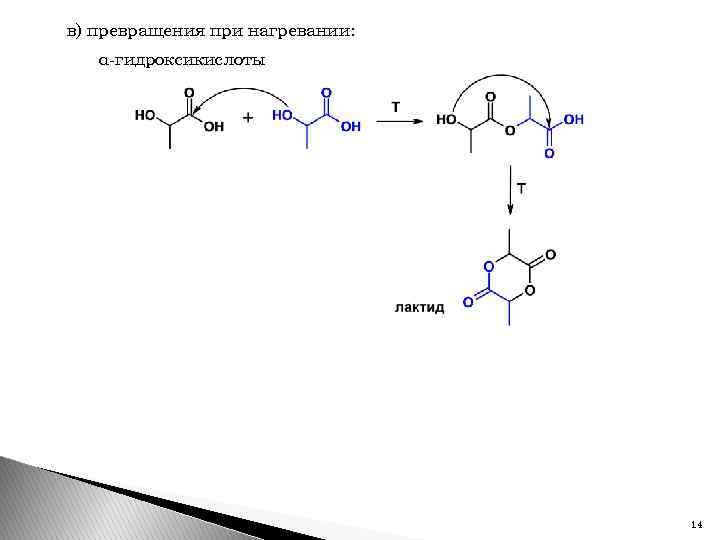 в) превращения при нагревании: α-гидроксикислоты 14
в) превращения при нагревании: α-гидроксикислоты 14
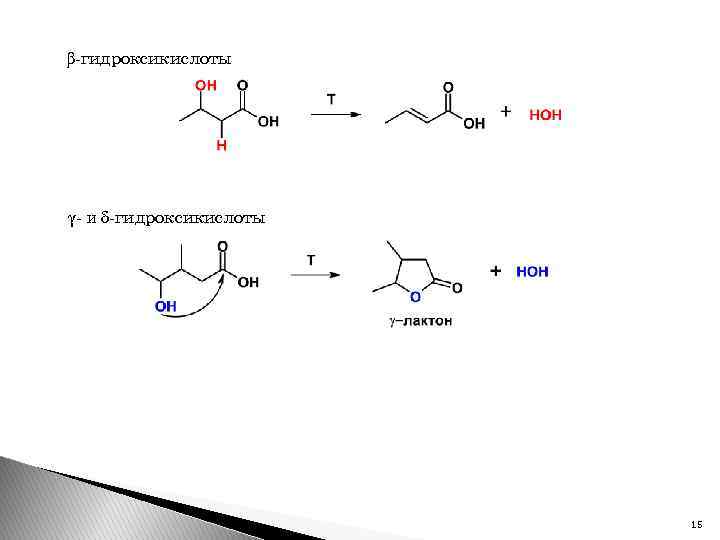 β-гидроксикислоты γ- и δ-гидроксикислоты 15
β-гидроксикислоты γ- и δ-гидроксикислоты 15
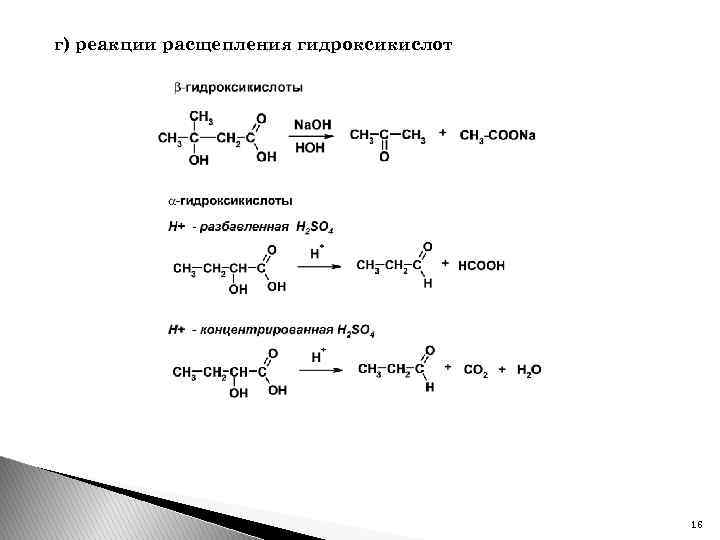 г) реакции расщепления гидроксикислот 16
г) реакции расщепления гидроксикислот 16
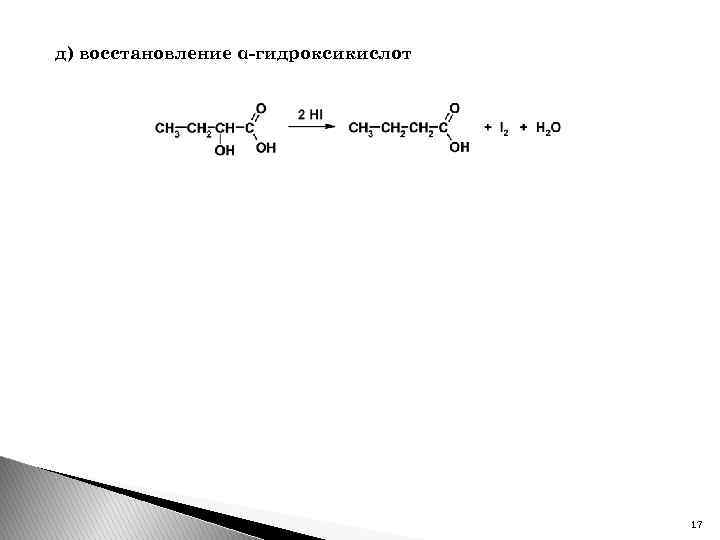 д) восстановление α-гидроксикислот 17
д) восстановление α-гидроксикислот 17
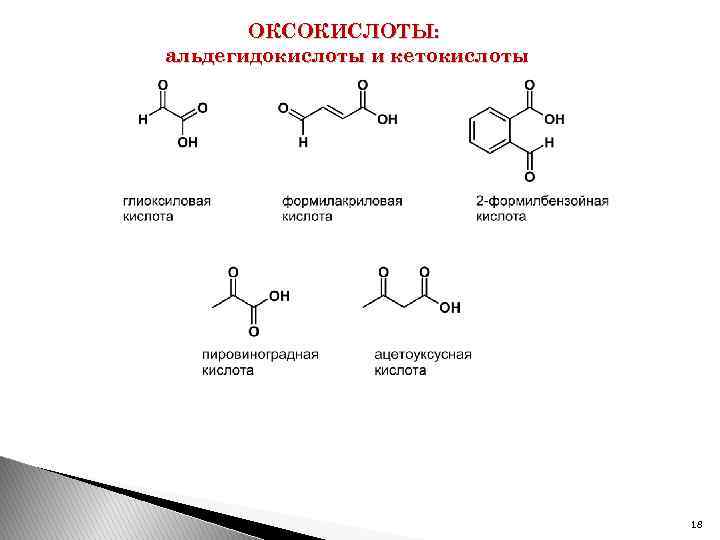 ОКСОКИСЛОТЫ: альдегидокислоты и кетокислоты 18
ОКСОКИСЛОТЫ: альдегидокислоты и кетокислоты 18
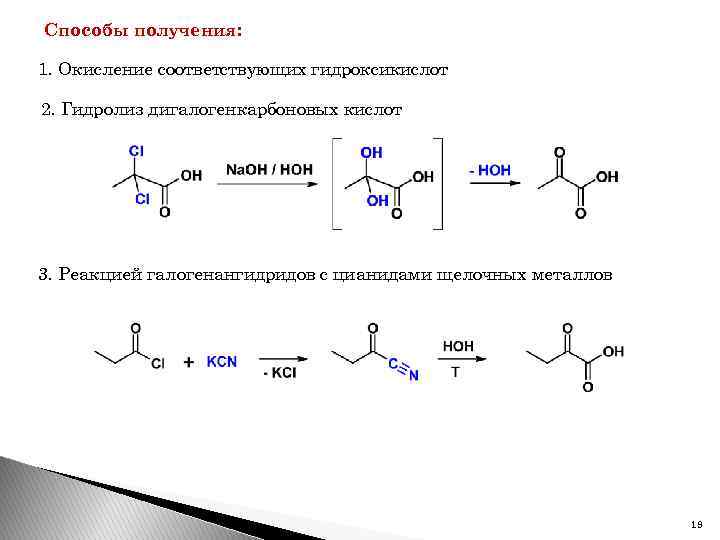 Способы получения: 1. Окисление соответствующих гидроксикислот 2. Гидролиз дигалогенкарбоновых кислот 3. Реакцией галогенангидридов с цианидами щелочных металлов 19
Способы получения: 1. Окисление соответствующих гидроксикислот 2. Гидролиз дигалогенкарбоновых кислот 3. Реакцией галогенангидридов с цианидами щелочных металлов 19
 Химические свойства - Реакции по карбоксильной группе: образование солей, сложных эфиров; - Реакции по карбонильной группе: взаимодействие с HCN, фенилгидразином, гидроксиламином, восстановление 20
Химические свойства - Реакции по карбоксильной группе: образование солей, сложных эфиров; - Реакции по карбонильной группе: взаимодействие с HCN, фенилгидразином, гидроксиламином, восстановление 20
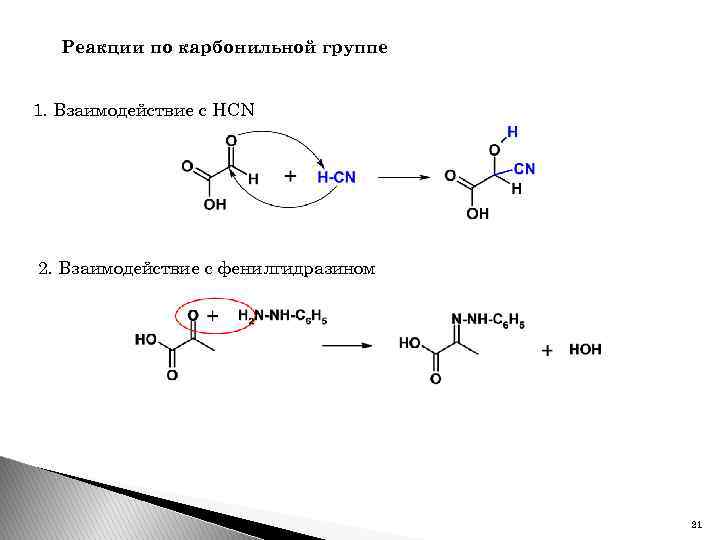 Реакции по карбонильной группе 1. Взаимодействие с HCN 2. Взаимодействие с фенилгидразином 21
Реакции по карбонильной группе 1. Взаимодействие с HCN 2. Взаимодействие с фенилгидразином 21
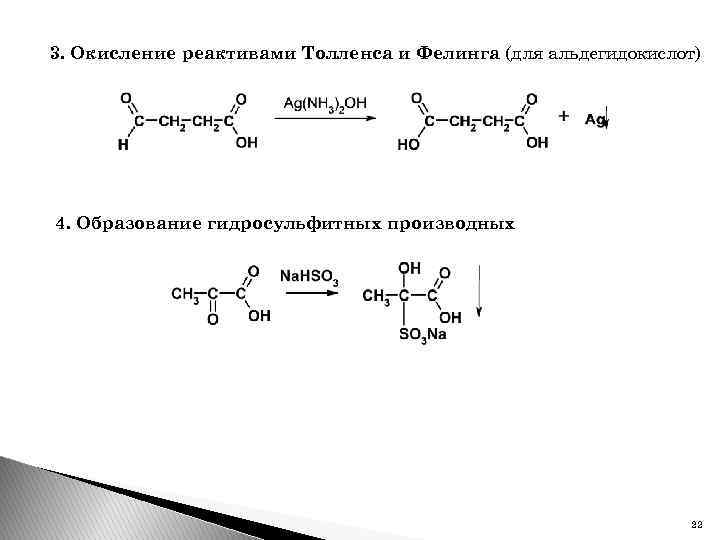 3. Окисление реактивами Толленса и Фелинга (для альдегидокислот) 4. Образование гидросульфитных производных 22
3. Окисление реактивами Толленса и Фелинга (для альдегидокислот) 4. Образование гидросульфитных производных 22
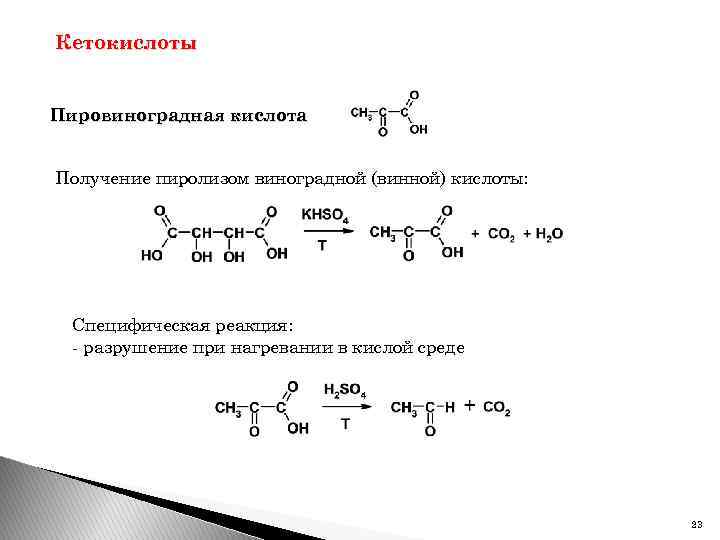 Кетокислоты Пировиноградная кислота Получение пиролизом виноградной (винной) кислоты: Специфическая реакция: - разрушение при нагревании в кислой среде 23
Кетокислоты Пировиноградная кислота Получение пиролизом виноградной (винной) кислоты: Специфическая реакция: - разрушение при нагревании в кислой среде 23
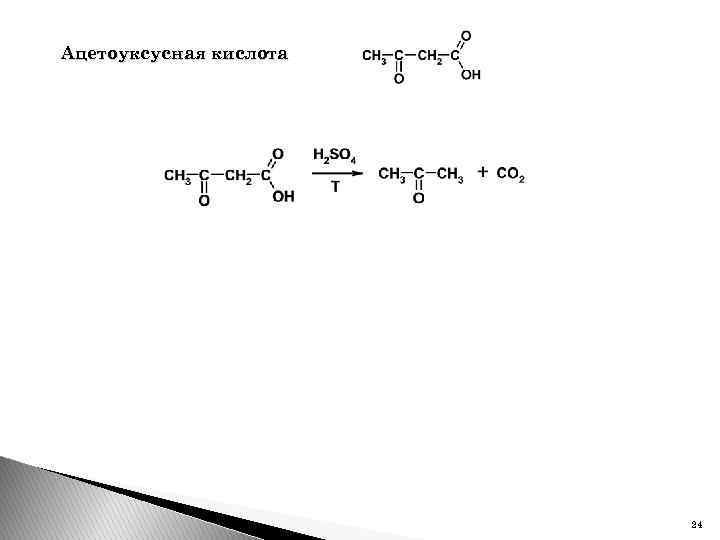 Ацетоуксусная кислота 24
Ацетоуксусная кислота 24
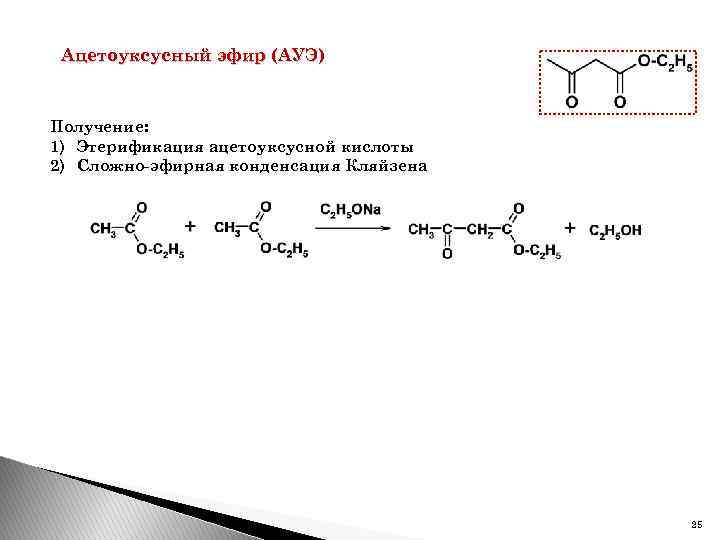 Ацетоуксусный эфир (АУЭ) Получение: 1) Этерификация ацетоуксусной кислоты 2) Сложно-эфирная конденсация Кляйзена 25
Ацетоуксусный эфир (АУЭ) Получение: 1) Этерификация ацетоуксусной кислоты 2) Сложно-эфирная конденсация Кляйзена 25
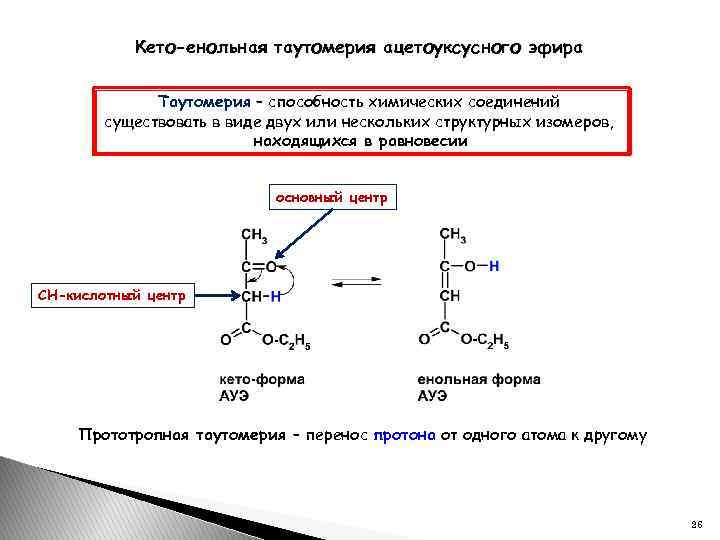 Кето-енольная таутомерия ацетоуксусного эфира Таутомерия – способность химических соединений существовать в виде двух или нескольких структурных изомеров, находящихся в равновесии основный центр СН-кислотный центр Прототропная таутомерия – перенос протона от одного атома к другому 26
Кето-енольная таутомерия ацетоуксусного эфира Таутомерия – способность химических соединений существовать в виде двух или нескольких структурных изомеров, находящихся в равновесии основный центр СН-кислотный центр Прототропная таутомерия – перенос протона от одного атома к другому 26
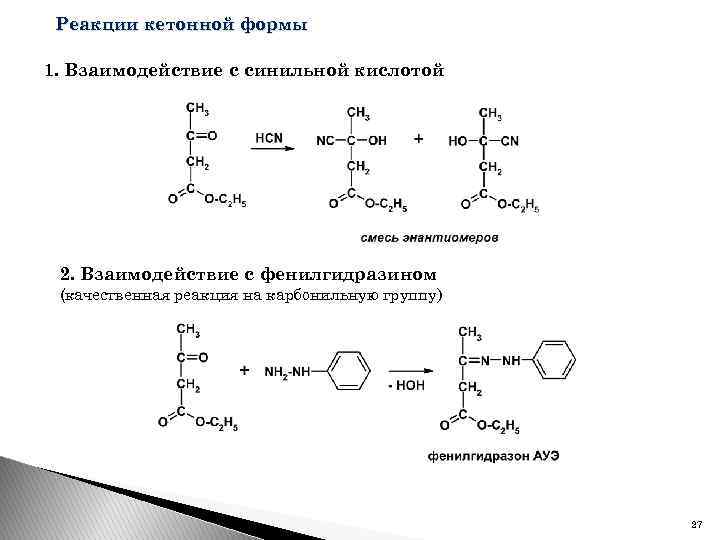 Реакции кетонной формы 1. Взаимодействие с синильной кислотой 2. Взаимодействие с фенилгидразином (качественная реакция на карбонильную группу) 27
Реакции кетонной формы 1. Взаимодействие с синильной кислотой 2. Взаимодействие с фенилгидразином (качественная реакция на карбонильную группу) 27
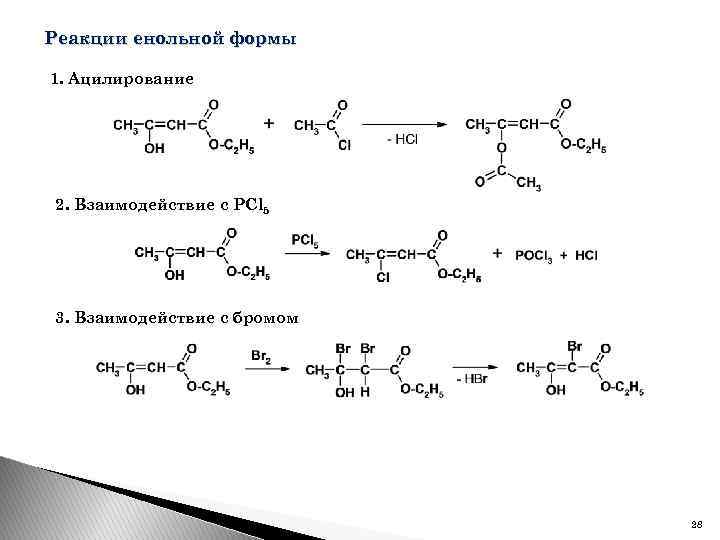 Реакции енольной формы 1. Ацилирование 2. Взаимодействие с PCl 5 3. Взаимодействие с бромом 28
Реакции енольной формы 1. Ацилирование 2. Взаимодействие с PCl 5 3. Взаимодействие с бромом 28
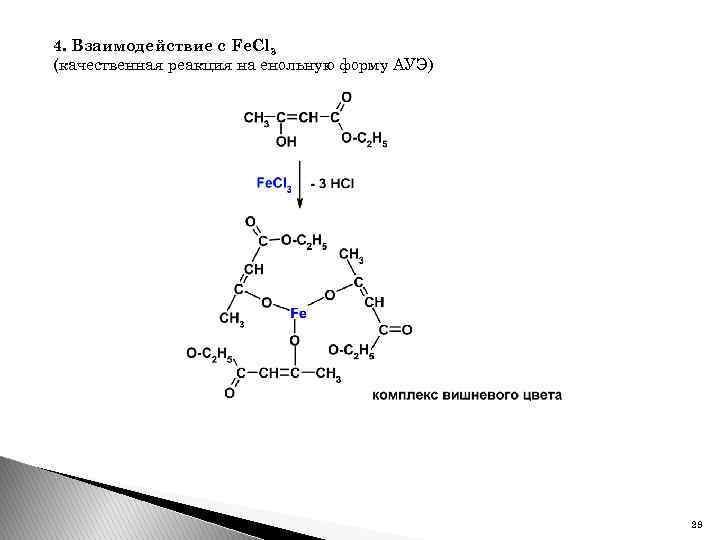 4. Взаимодействие с Fe. Cl 3 (качественная реакция на енольную форму АУЭ) 29
4. Взаимодействие с Fe. Cl 3 (качественная реакция на енольную форму АУЭ) 29
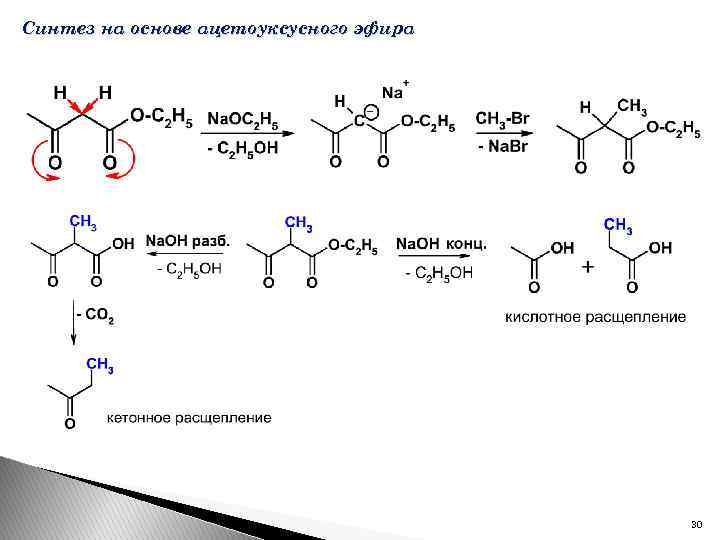 Синтез на основе ацетоуксусного эфира 30
Синтез на основе ацетоуксусного эфира 30
 31
31


