9 гетероциклы ТПМ-8-19.ppt
- Количество слайдов: 63
 ГЕТЕРОЦИКЛИЧ. СОЕД-НИЯ иклич. соед. , содерж. в составе наряду с ат. С иные, другие элементы (гетероатомы). Наиболее распрост-ны: О, N, S. КЛАССИФ-ЦИЯ От разм. цикла: 3 х, 4 х, 5, 6 -член. циклы. Наиб. распростр: 5 -, 6 - чл. циклы От кол-ва гетероатом. : моно-, ди-, три- … гетероат. кольца От степени насыщенти. : насыщен. ; ненасыщ. ; ароматич.
ГЕТЕРОЦИКЛИЧ. СОЕД-НИЯ иклич. соед. , содерж. в составе наряду с ат. С иные, другие элементы (гетероатомы). Наиболее распрост-ны: О, N, S. КЛАССИФ-ЦИЯ От разм. цикла: 3 х, 4 х, 5, 6 -член. циклы. Наиб. распростр: 5 -, 6 - чл. циклы От кол-ва гетероатом. : моно-, ди-, три- … гетероат. кольца От степени насыщенти. : насыщен. ; ненасыщ. ; ароматич.
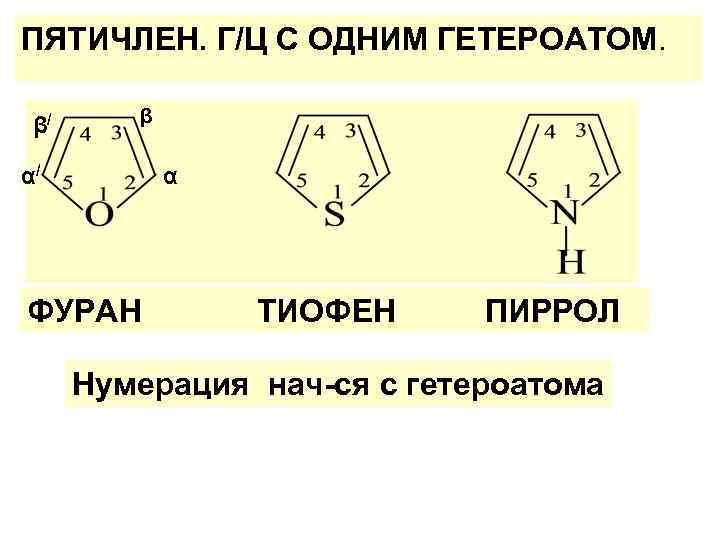 ПЯТИЧЛЕН. Г/Ц С ОДНИМ ГЕТЕРОАТОМ. β/ β α/ α ФУРАН ТИОФЕН ПИРРОЛ Нумерация нач-ся с гетероатома
ПЯТИЧЛЕН. Г/Ц С ОДНИМ ГЕТЕРОАТОМ. β/ β α/ α ФУРАН ТИОФЕН ПИРРОЛ Нумерация нач-ся с гетероатома
 П/чл. г/ц ароматичны по Хюккелю. Аром. секстет электр. (6) образован: четырьмя электр. от С-атом. и двумя - от гетероатома (O, N, S). В связи с тем, что электроотриц. г/а неодинакова: O>N>S, аромат-сть фурана, тиофена и пиррола тоже отличается.
П/чл. г/ц ароматичны по Хюккелю. Аром. секстет электр. (6) образован: четырьмя электр. от С-атом. и двумя - от гетероатома (O, N, S). В связи с тем, что электроотриц. г/а неодинакова: O>N>S, аромат-сть фурана, тиофена и пиррола тоже отличается.
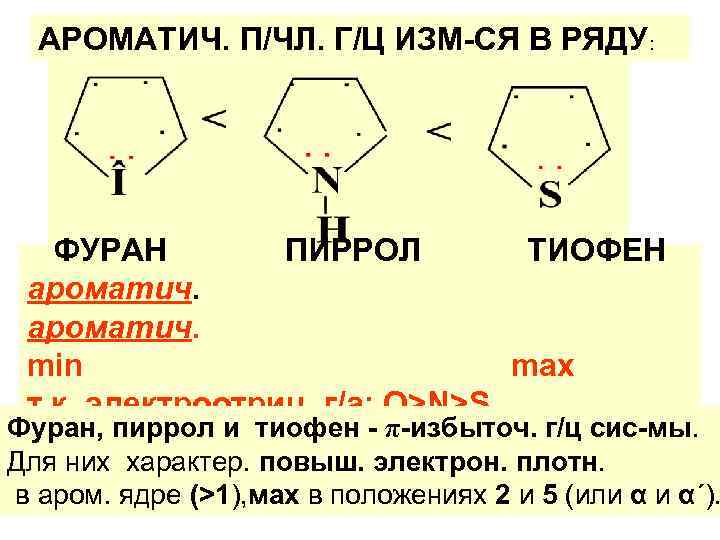 АРОМАТИЧ. П/ЧЛ. Г/Ц ИЗМ-СЯ В РЯДУ: ФУРАН ПИРРОЛ ТИОФЕН ароматич. min max т. к. электроотриц. г/а: О>N>S Фуран, пиррол и тиофен - π-избыточ. г/ц сис-мы. Для них характер. повыш. электрон. плотн. в аром. ядре (>1), мах в положениях 2 и 5 (или α и α΄).
АРОМАТИЧ. П/ЧЛ. Г/Ц ИЗМ-СЯ В РЯДУ: ФУРАН ПИРРОЛ ТИОФЕН ароматич. min max т. к. электроотриц. г/а: О>N>S Фуран, пиррол и тиофен - π-избыточ. г/ц сис-мы. Для них характер. повыш. электрон. плотн. в аром. ядре (>1), мах в положениях 2 и 5 (или α и α΄).
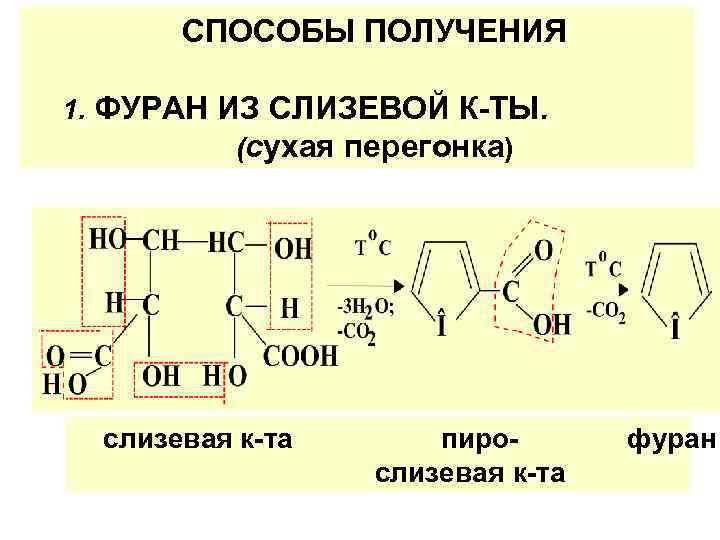 СПОСОБЫ ПОЛУЧЕНИЯ 1. ФУРАН ИЗ СЛИЗЕВОЙ К-ТЫ. (сухая перегонка) слизевая к-та пирослизевая к-та фуран
СПОСОБЫ ПОЛУЧЕНИЯ 1. ФУРАН ИЗ СЛИЗЕВОЙ К-ТЫ. (сухая перегонка) слизевая к-та пирослизевая к-та фуран
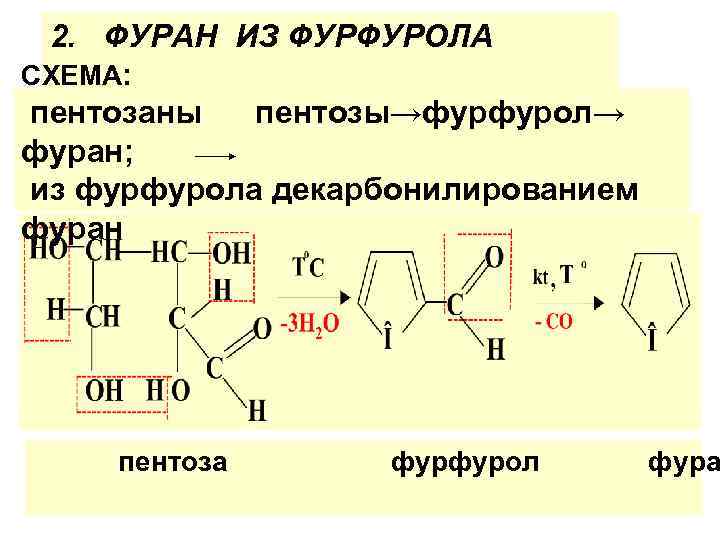 2. ФУРАН ИЗ ФУРФУРОЛА СХЕМА: пентозаны пентозы→фурфурол→ фуран; из фурфурола декарбонилированием фуран пентоза фурфурол фура
2. ФУРАН ИЗ ФУРФУРОЛА СХЕМА: пентозаны пентозы→фурфурол→ фуран; из фурфурола декарбонилированием фуран пентоза фурфурол фура
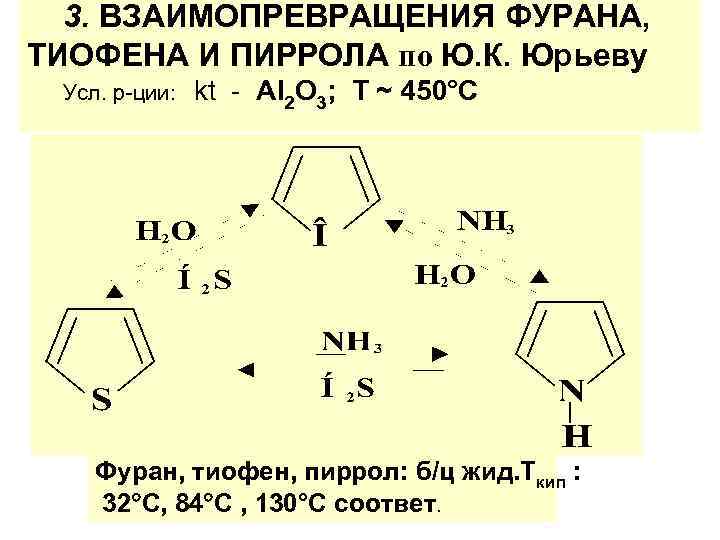 3. ВЗАИМОПРЕВРАЩЕНИЯ ФУРАНА, ТИОФЕНА И ПИРРОЛА по Ю. К. Юрьеву Усл. р-ции: kt - Al 2 O 3; T ~ 450°C Фуран, тиофен, пиррол: б/ц жид. Ткип : 32 С, 84 С , 130°С соответ.
3. ВЗАИМОПРЕВРАЩЕНИЯ ФУРАНА, ТИОФЕНА И ПИРРОЛА по Ю. К. Юрьеву Усл. р-ции: kt - Al 2 O 3; T ~ 450°C Фуран, тиофен, пиррол: б/ц жид. Ткип : 32 С, 84 С , 130°С соответ.
 ХИМ. СВ-ВА обусл. особен. строения Конкурир. структ-ры: • ароматичность; • диены; • кислотность-основность. Р-ции пятичленных г/ц: 1. Р-ции SЕ; 2. Р-ции А; 3. Кислотно-основн. св-ва; 4. Взаимные превращения по Юрьеву
ХИМ. СВ-ВА обусл. особен. строения Конкурир. структ-ры: • ароматичность; • диены; • кислотность-основность. Р-ции пятичленных г/ц: 1. Р-ции SЕ; 2. Р-ции А; 3. Кислотно-основн. св-ва; 4. Взаимные превращения по Юрьеву
 l. Р-ции SЕ: галоген. , сульфир. , нитров. и др. В р-циях SЕ пятичл. г/ц активнее бензола, а в некот. р-циях иллюстр. СУПЕРАРОМАТИЧНОСТЬ. Причина – повыш. электр. плотн. в аром. ядре (> 1). Мах электр. плотн. на С-2 и С-5 атом. аром. ядра, где и наблюд. SE.
l. Р-ции SЕ: галоген. , сульфир. , нитров. и др. В р-циях SЕ пятичл. г/ц активнее бензола, а в некот. р-циях иллюстр. СУПЕРАРОМАТИЧНОСТЬ. Причина – повыш. электр. плотн. в аром. ядре (> 1). Мах электр. плотн. на С-2 и С-5 атом. аром. ядра, где и наблюд. SE.
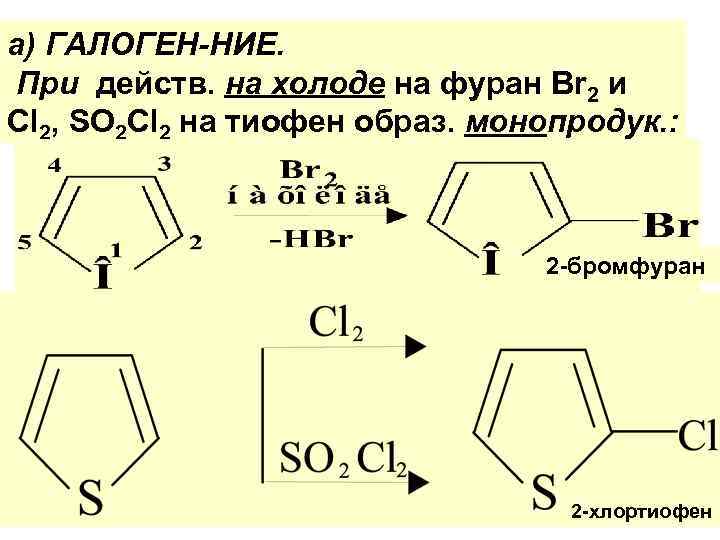 а) ГАЛОГЕН-НИЕ. При действ. на холоде на фуран Br 2 и Cl 2, SO 2 Cl 2 на тиофен образ. монопродук. : 2 -бромфуран 2 -хлортиофен
а) ГАЛОГЕН-НИЕ. При действ. на холоде на фуран Br 2 и Cl 2, SO 2 Cl 2 на тиофен образ. монопродук. : 2 -бромфуран 2 -хлортиофен
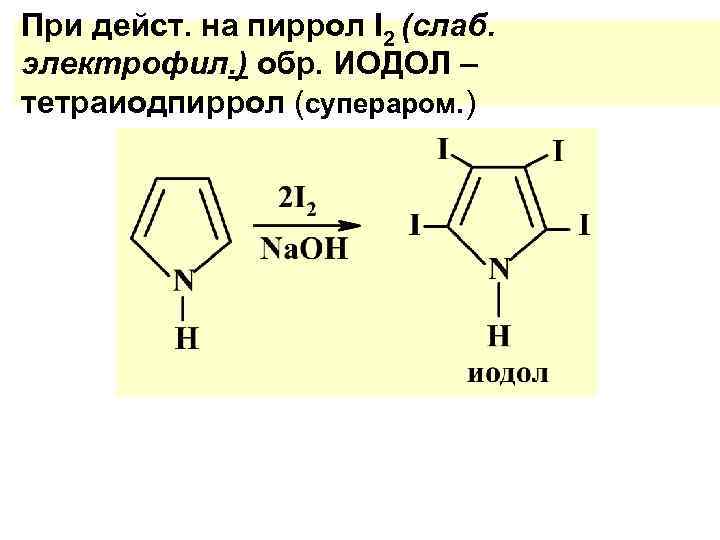 При дейст. на пиррол I 2 (слаб. электрофил. ) обр. ИОДОЛ – тетраиодпиррол (супераром. )
При дейст. на пиррол I 2 (слаб. электрофил. ) обр. ИОДОЛ – тетраиодпиррол (супераром. )
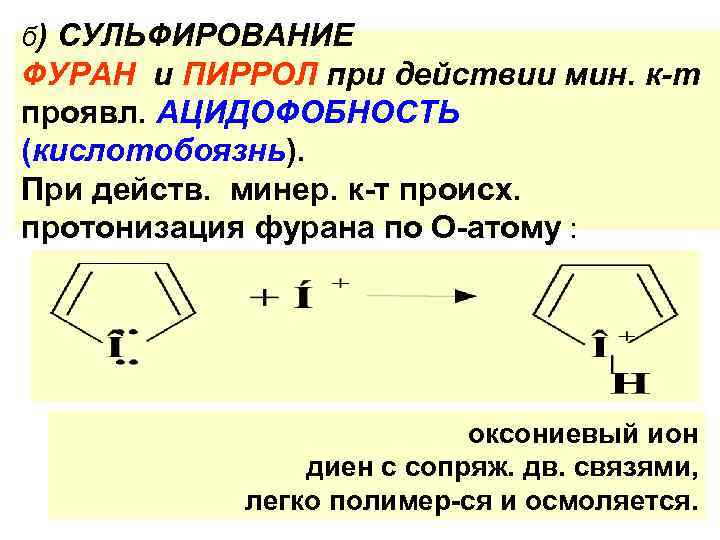 б) СУЛЬФИРОВАНИЕ ФУРАН и ПИРРОЛ при действии мин. к-т проявл. АЦИДОФОБНОСТЬ (кислотобоязнь). При действ. минер. к-т происх. протонизация фурана по О-атому : оксониевый ион диен с сопряж. дв. связями, легко полимер-ся и осмоляется.
б) СУЛЬФИРОВАНИЕ ФУРАН и ПИРРОЛ при действии мин. к-т проявл. АЦИДОФОБНОСТЬ (кислотобоязнь). При действ. минер. к-т происх. протонизация фурана по О-атому : оксониевый ион диен с сопряж. дв. связями, легко полимер-ся и осмоляется.
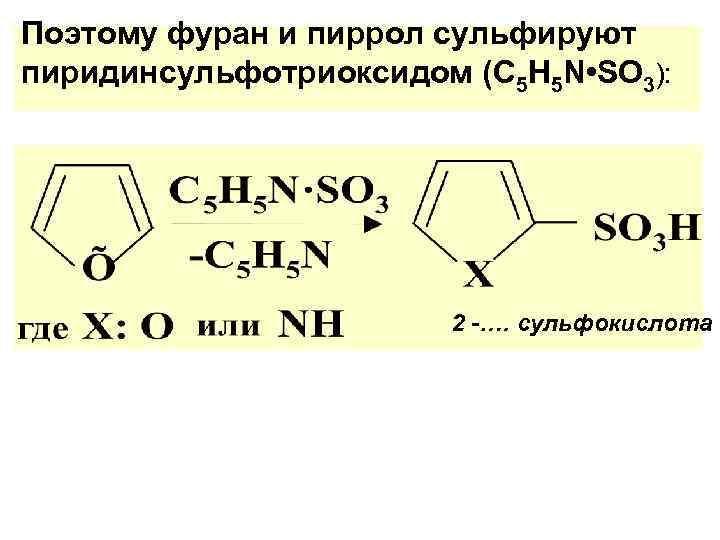 Поэтому фуран и пиррол сульфируют пиридинсульфотриоксидом (С 5 Н 5 N • SO 3): 2 -…. сульфокислота
Поэтому фуран и пиррол сульфируют пиридинсульфотриоксидом (С 5 Н 5 N • SO 3): 2 -…. сульфокислота
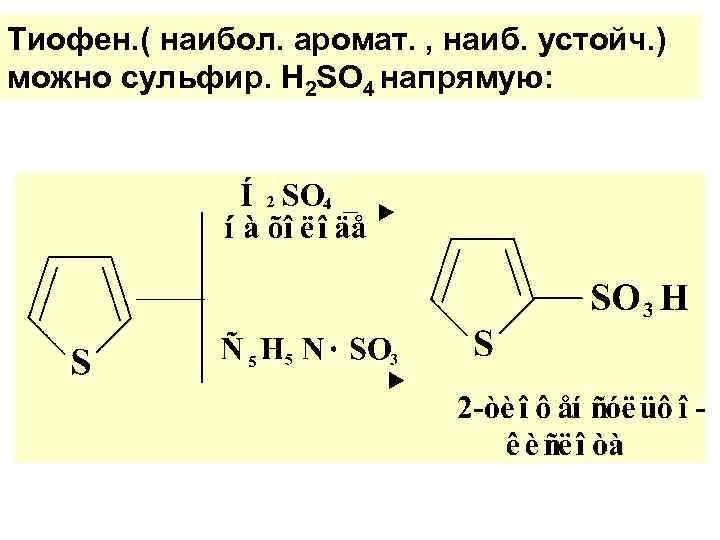 Тиофен. ( наибол. аромат. , наиб. устойч. ) можно сульфир. H 2 SO 4 напрямую:
Тиофен. ( наибол. аромат. , наиб. устойч. ) можно сульфир. H 2 SO 4 напрямую:
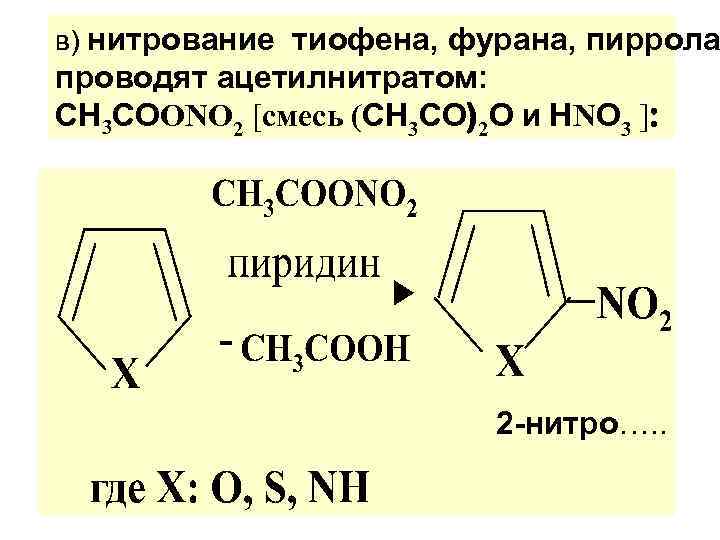 в) нитрование тиофена, фурана, пиррола проводят ацетилнитратом: СН 3 СОONO 2 [смесь (СН 3 СО)2 О и НNО 3 ]: 2 -нитро…. .
в) нитрование тиофена, фурана, пиррола проводят ацетилнитратом: СН 3 СОONO 2 [смесь (СН 3 СО)2 О и НNО 3 ]: 2 -нитро…. .
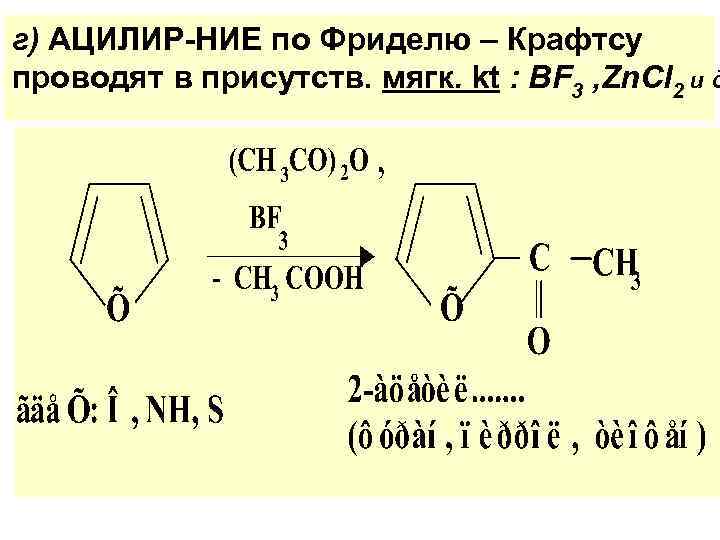 г) АЦИЛИР-НИЕ по Фриделю – Крафтсу проводят в присутств. мягк. kt : BF 3 , Zn. Cl 2 и д
г) АЦИЛИР-НИЕ по Фриделю – Крафтсу проводят в присутств. мягк. kt : BF 3 , Zn. Cl 2 и д
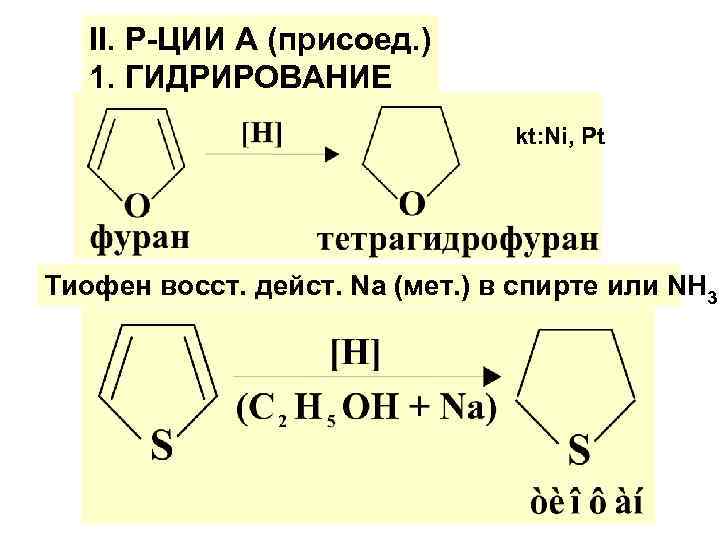 ΙΙ. Р-ЦИИ А (присоед. ) 1. ГИДРИРОВАНИЕ kt: Ni, Pt Тиофен восст. дейст. Na (мет. ) в спирте или ΝΗ 3:
ΙΙ. Р-ЦИИ А (присоед. ) 1. ГИДРИРОВАНИЕ kt: Ni, Pt Тиофен восст. дейст. Na (мет. ) в спирте или ΝΗ 3:
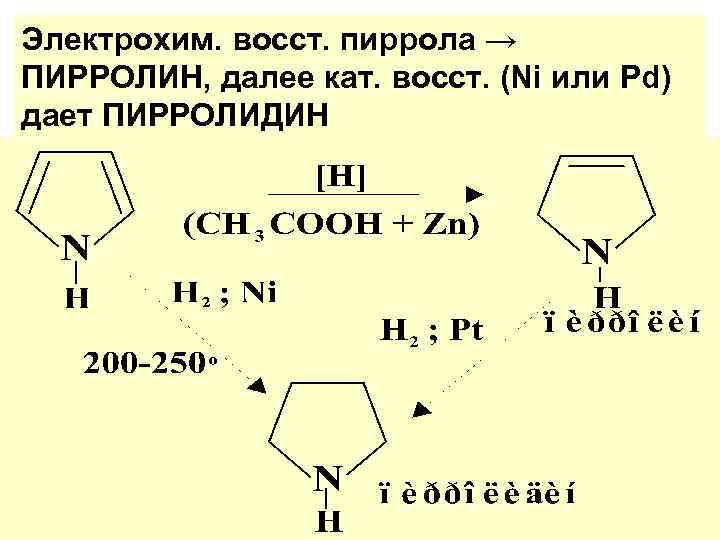 Электрохим. восст. пиррола → ПИРРОЛИН, далее кат. восст. (Ni или Pd) дает ПИРРОЛИДИН
Электрохим. восст. пиррола → ПИРРОЛИН, далее кат. восст. (Ni или Pd) дает ПИРРОЛИДИН
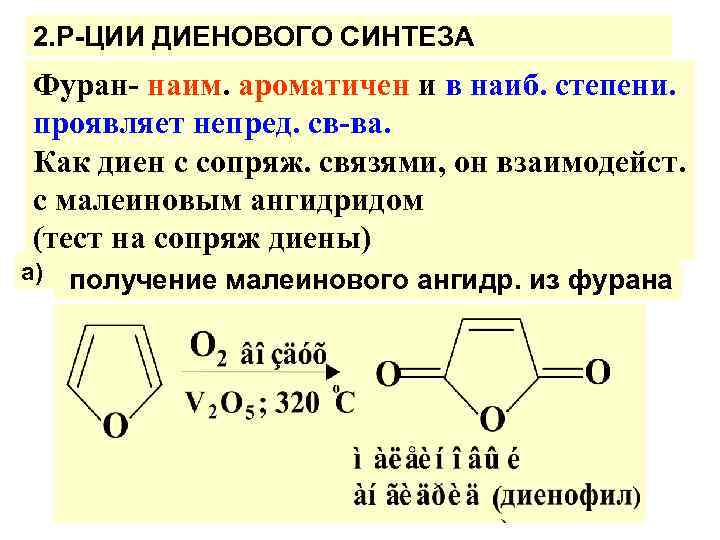 2. Р-ЦИИ ДИЕНОВОГО СИНТЕЗА Фуран- наим. ароматичен и в наиб. степени. проявляет непред. св-ва. Как диен с сопряж. связями, он взаимодейст. с малеиновым ангидридом (тест на сопряж диены) а) получение малеинового ангидр. из фурана
2. Р-ЦИИ ДИЕНОВОГО СИНТЕЗА Фуран- наим. ароматичен и в наиб. степени. проявляет непред. св-ва. Как диен с сопряж. связями, он взаимодейст. с малеиновым ангидридом (тест на сопряж диены) а) получение малеинового ангидр. из фурана
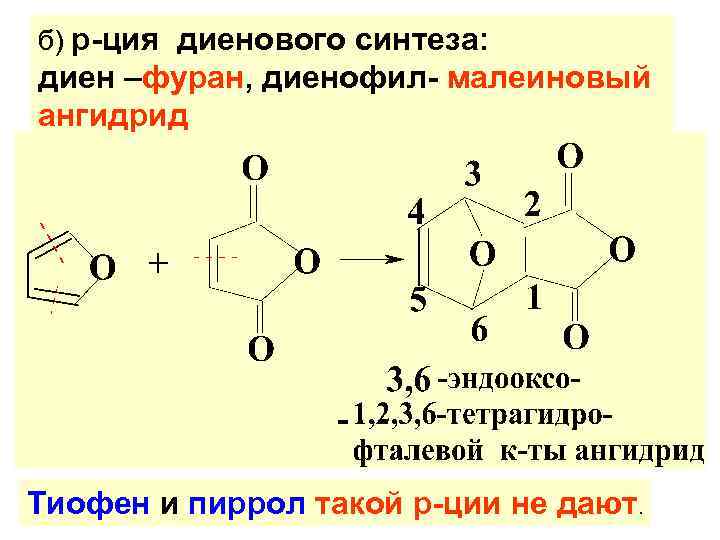 б) р-ция диенового синтеза: диен –фуран, диенофил- малеиновый ангидрид Тиофен и пиррол такой р-ции не дают.
б) р-ция диенового синтеза: диен –фуран, диенофил- малеиновый ангидрид Тиофен и пиррол такой р-ции не дают.
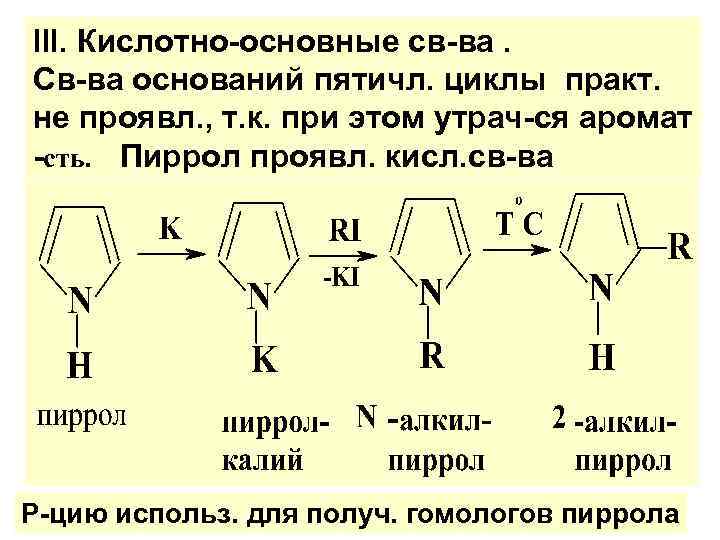 lll. Кислотно-основные св-ва. Св-ва оснований пятичл. циклы практ. не проявл. , т. к. при этом утрач-ся аромат -сть. Пиррол проявл. кисл. св-ва Р-цию использ. для получ. гомологов пиррола
lll. Кислотно-основные св-ва. Св-ва оснований пятичл. циклы практ. не проявл. , т. к. при этом утрач-ся аромат -сть. Пиррол проявл. кисл. св-ва Р-цию использ. для получ. гомологов пиррола
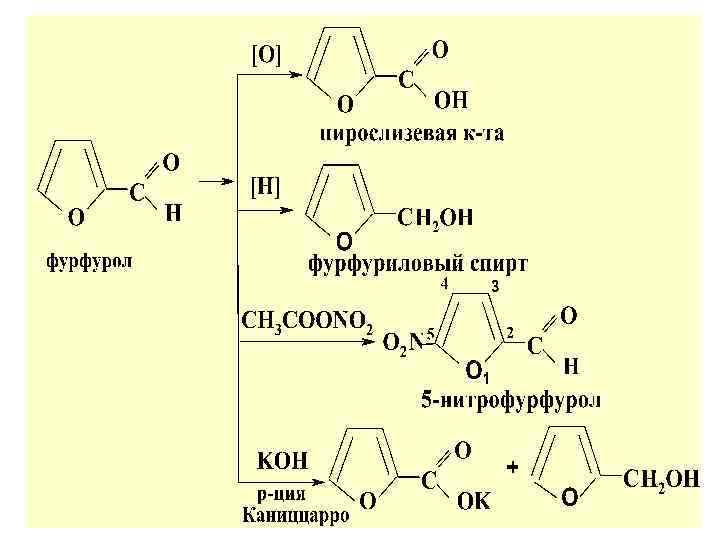
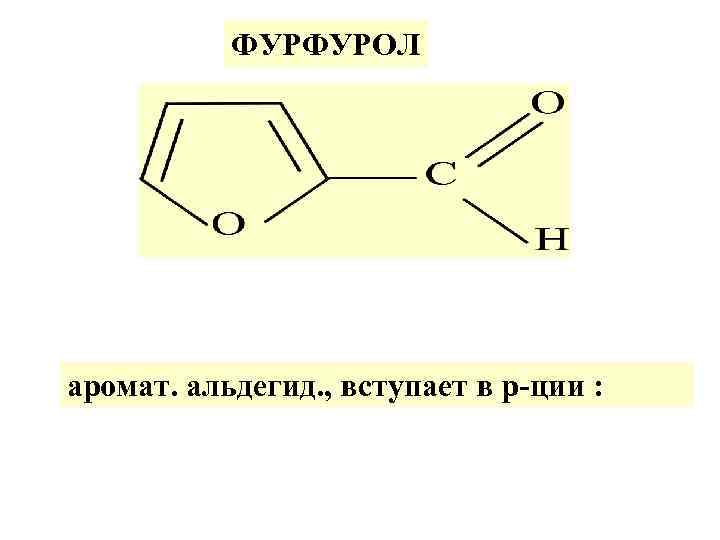 ФУРФУРОЛ аромат. альдегид. , вступает в р-ции :
ФУРФУРОЛ аромат. альдегид. , вступает в р-ции :
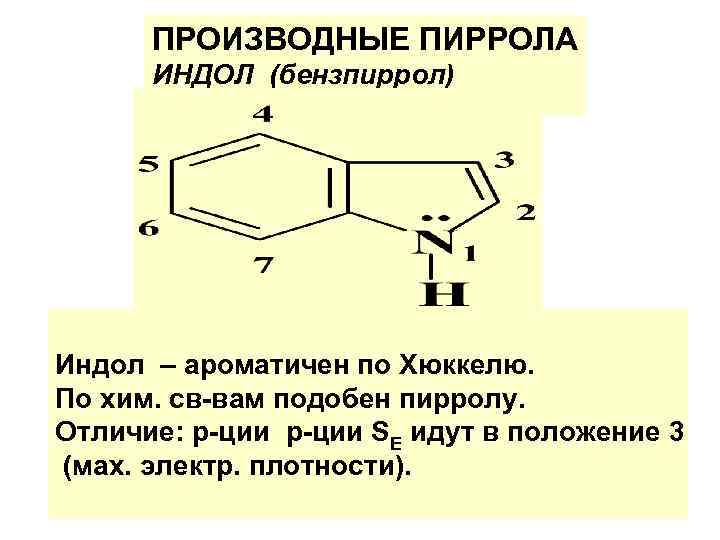 ПРОИЗВОДНЫЕ ПИРРОЛА ИНДОЛ (бензпиррол) Индол – ароматичен по Хюккелю. По хим. св-вам подобен пирролу. Отличие: р-ции SE идут в положение 3 (мах. электр. плотности).
ПРОИЗВОДНЫЕ ПИРРОЛА ИНДОЛ (бензпиррол) Индол – ароматичен по Хюккелю. По хим. св-вам подобен пирролу. Отличие: р-ции SE идут в положение 3 (мах. электр. плотности).
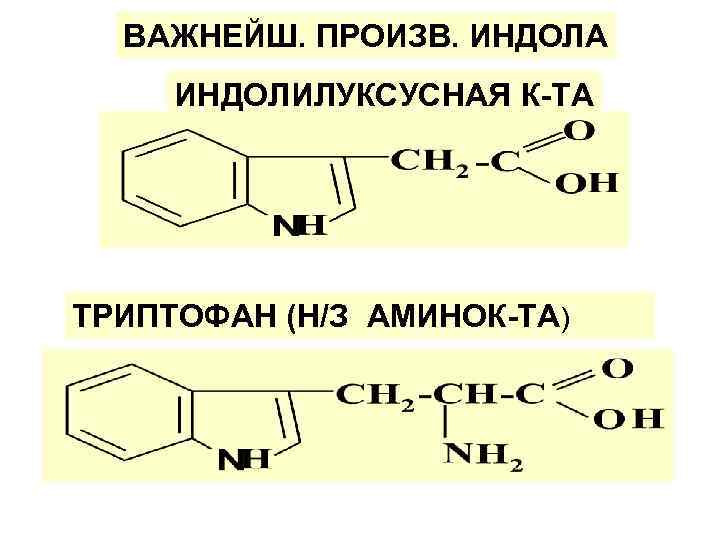 ВАЖНЕЙШ. ПРОИЗВ. ИНДОЛА ИНДОЛИЛУКСУСНАЯ К-ТА ТРИПТОФАН (Н/З АМИНОК-ТА)
ВАЖНЕЙШ. ПРОИЗВ. ИНДОЛА ИНДОЛИЛУКСУСНАЯ К-ТА ТРИПТОФАН (Н/З АМИНОК-ТА)
 ПИРРОЛОВЫЕ КРАСИТЕЛИ ХЛОРОФИЛЛЫ и ГЕМИН (кровь) – пирроловые красители. В основе - ядро порфина ( аромат. по Хюккелю): 4 пиррольных кольца, соедин. по , /-полож. метиленовыми связями ( –СН= ). Порфирин – алкилирован по полож. , / ядро порфина. В центре - комплексообразователь: Mg – в хлорофилле; Fе – в гемине.
ПИРРОЛОВЫЕ КРАСИТЕЛИ ХЛОРОФИЛЛЫ и ГЕМИН (кровь) – пирроловые красители. В основе - ядро порфина ( аромат. по Хюккелю): 4 пиррольных кольца, соедин. по , /-полож. метиленовыми связями ( –СН= ). Порфирин – алкилирован по полож. , / ядро порфина. В центре - комплексообразователь: Mg – в хлорофилле; Fе – в гемине.
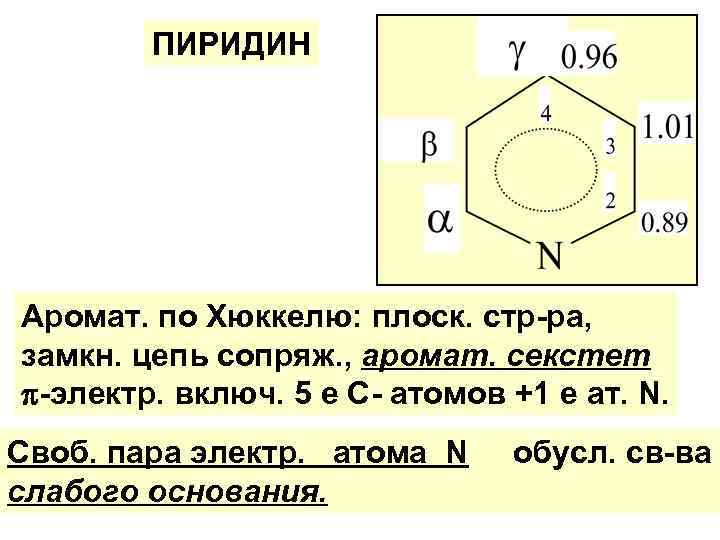 ПИРИДИН Аромат. по Хюккелю: плоск. стр-ра, замкн. цепь сопряж. , аромат. секстет -электр. включ. 5 е С- атомов +1 е ат. N. Своб. пара электр. атома N слабого основания. обусл. св-ва
ПИРИДИН Аромат. по Хюккелю: плоск. стр-ра, замкн. цепь сопряж. , аромат. секстет -электр. включ. 5 е С- атомов +1 е ат. N. Своб. пара электр. атома N слабого основания. обусл. св-ва
 ХИМ. СВ-ВА Аромат. харак. пиридина выраж. очень ярко: не разруш. К 2 Cr 2 O 7 и НNO 3; термич. устойч. Система -дефиц. , т. к. электр. плотн. в ядре пиридина понижена, вследствие электоотриц. N. Р-ции SN в -дефиц. г/ц идут легче, чем SE. В целом, для пиридина, характ-ны р-ции: • SE ( -полож); • SN ( - и - полож); • иллюстр. основность; • восстановл
ХИМ. СВ-ВА Аромат. харак. пиридина выраж. очень ярко: не разруш. К 2 Cr 2 O 7 и НNO 3; термич. устойч. Система -дефиц. , т. к. электр. плотн. в ядре пиридина понижена, вследствие электоотриц. N. Р-ции SN в -дефиц. г/ц идут легче, чем SE. В целом, для пиридина, характ-ны р-ции: • SE ( -полож); • SN ( - и - полож); • иллюстр. основность; • восстановл
 Р-ЦИИ ПИРИДИНА Ι. Р-ЦИИ SE Пиридин труд. вступает в р-ции SE по сравн. с бензолом. Сильные электрофилы (NO 2+; SO 3 H+) действ. в кислой среде. При этом пиридин превращ. в соль, атом N станов-ся полож. заряж. Это еще более затрудн. р-ции SE. Р-ции SE идут в полож. 3 - наибол. электр. плот. после ат. N
Р-ЦИИ ПИРИДИНА Ι. Р-ЦИИ SE Пиридин труд. вступает в р-ции SE по сравн. с бензолом. Сильные электрофилы (NO 2+; SO 3 H+) действ. в кислой среде. При этом пиридин превращ. в соль, атом N станов-ся полож. заряж. Это еще более затрудн. р-ции SE. Р-ции SE идут в полож. 3 - наибол. электр. плот. после ат. N
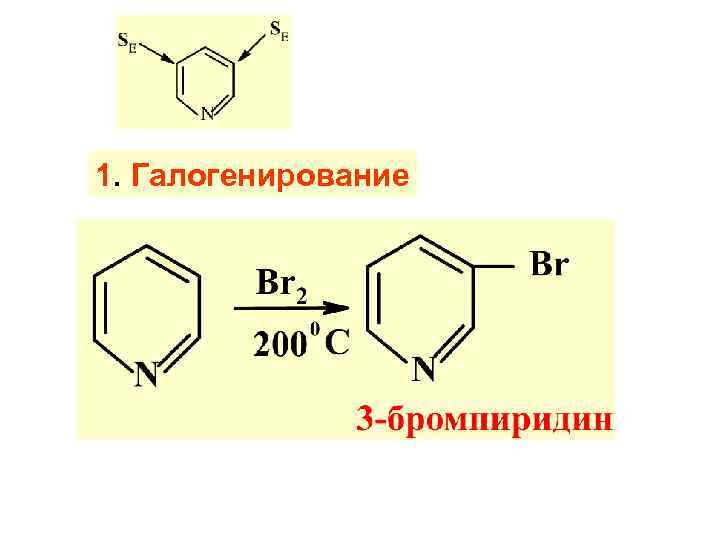 1. Галогенирование
1. Галогенирование
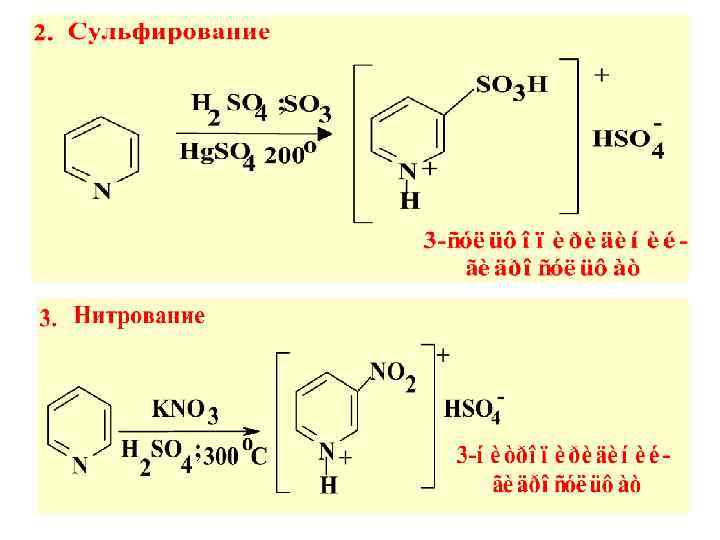
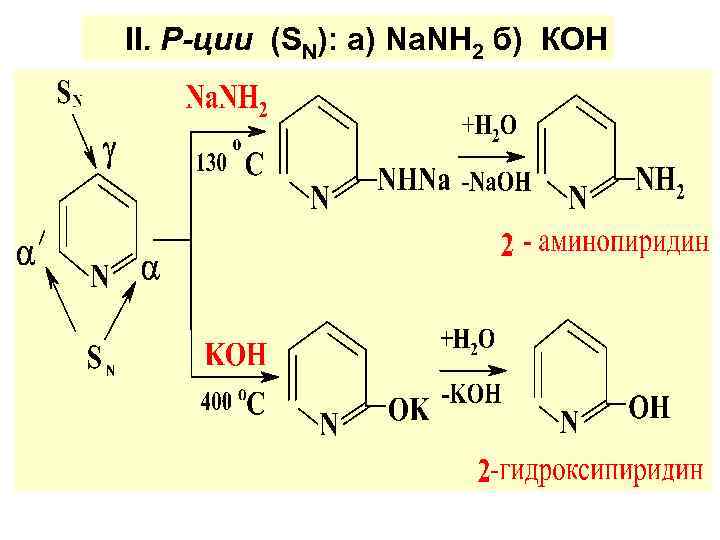 ΙΙ. Р-ции (SN): а) Na. NH 2 б) КОН
ΙΙ. Р-ции (SN): а) Na. NH 2 б) КОН
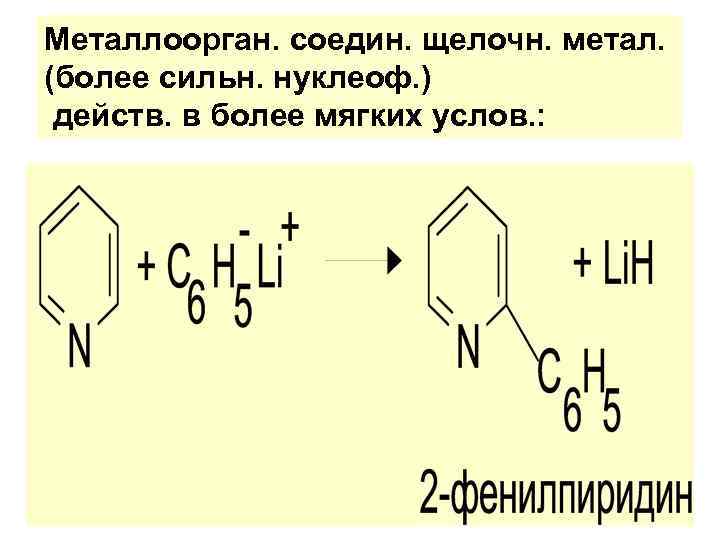 Металлоорган. соедин. щелочн. метал. (более сильн. нуклеоф. ) действ. в более мягких услов. :
Металлоорган. соедин. щелочн. метал. (более сильн. нуклеоф. ) действ. в более мягких услов. :
 lll. ОСНОВНОСТЬ Основность пиридина обусл. своб. электр. парой N. Основание- слабое. С сильн. мин. кислот. пиридин дает соли: пиридинийхлорид пиридинсульфотриоксид
lll. ОСНОВНОСТЬ Основность пиридина обусл. своб. электр. парой N. Основание- слабое. С сильн. мин. кислот. пиридин дает соли: пиридинийхлорид пиридинсульфотриоксид
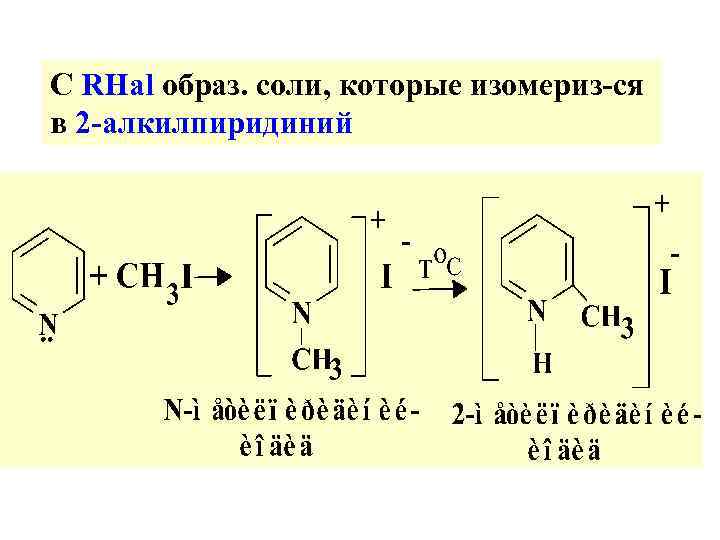 С RHal образ. соли, которые изомериз-ся в 2 -алкилпиридиний
С RHal образ. соли, которые изомериз-ся в 2 -алкилпиридиний
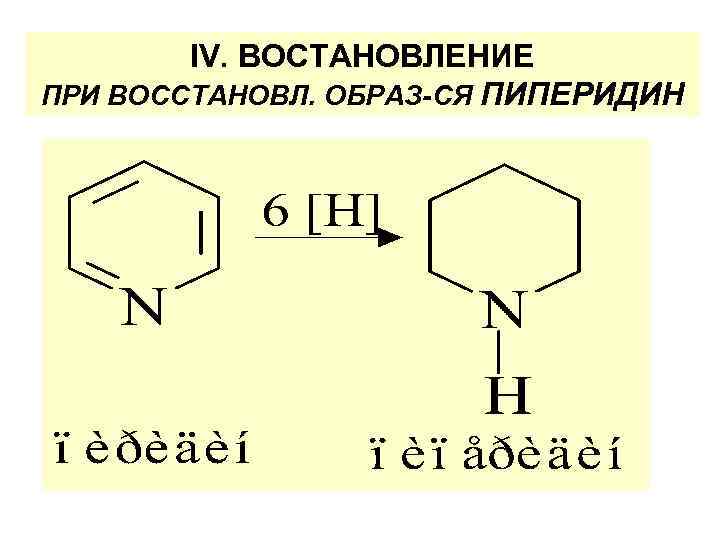 ΙV. ВОСТАНОВЛЕНИЕ ПРИ ВОССТАНОВЛ. ОБРАЗ-СЯ ПИПЕРИДИН
ΙV. ВОСТАНОВЛЕНИЕ ПРИ ВОССТАНОВЛ. ОБРАЗ-СЯ ПИПЕРИДИН
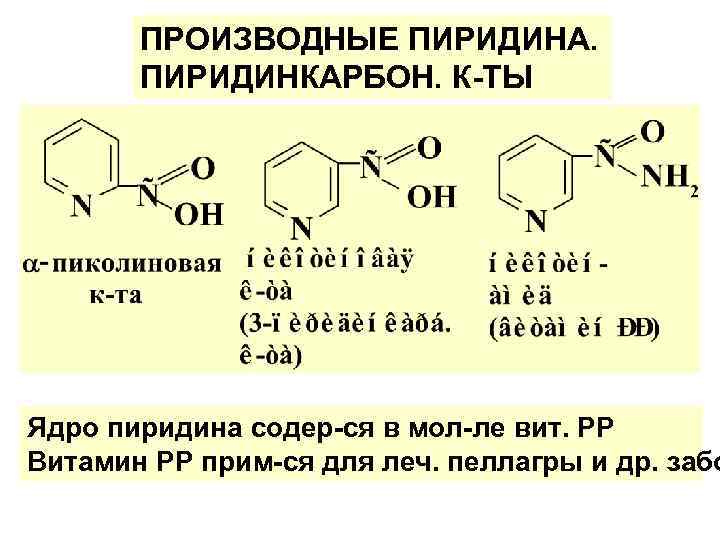 ПРОИЗВОДНЫЕ ПИРИДИНА. ПИРИДИНКАРБОН. К-ТЫ Ядро пиридина содер-ся в мол-ле вит. РР Витамин РР прим-ся для леч. пеллагры и др. забо
ПРОИЗВОДНЫЕ ПИРИДИНА. ПИРИДИНКАРБОН. К-ТЫ Ядро пиридина содер-ся в мол-ле вит. РР Витамин РР прим-ся для леч. пеллагры и др. забо
 ПОНЯТИЕ ОБ АЛКАЛОИДАХ АЛКАЛОИДЫ – груп. азотистых соед. , обладающих св-ми оснований , встреч-ся, преимущ. , в раст. Алкалоиды облад. сильным физиолог. или фармаколог. действ. . Классиф. по виду раст. или типу г/ц. Ряд алк-дов содерж. ядро пиридина и пиперидина: никотин, анабазин и др. Никотин до 3% содер-ся в табаке. Ядовит: 40 мг никотина –летальная доза для человека.
ПОНЯТИЕ ОБ АЛКАЛОИДАХ АЛКАЛОИДЫ – груп. азотистых соед. , обладающих св-ми оснований , встреч-ся, преимущ. , в раст. Алкалоиды облад. сильным физиолог. или фармаколог. действ. . Классиф. по виду раст. или типу г/ц. Ряд алк-дов содерж. ядро пиридина и пиперидина: никотин, анабазин и др. Никотин до 3% содер-ся в табаке. Ядовит: 40 мг никотина –летальная доза для человека.
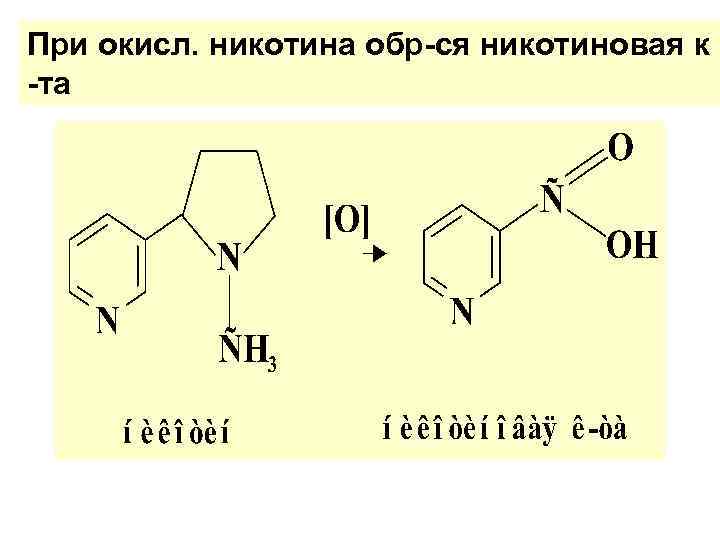 При окисл. никотина обр-ся никотиновая к -та
При окисл. никотина обр-ся никотиновая к -та
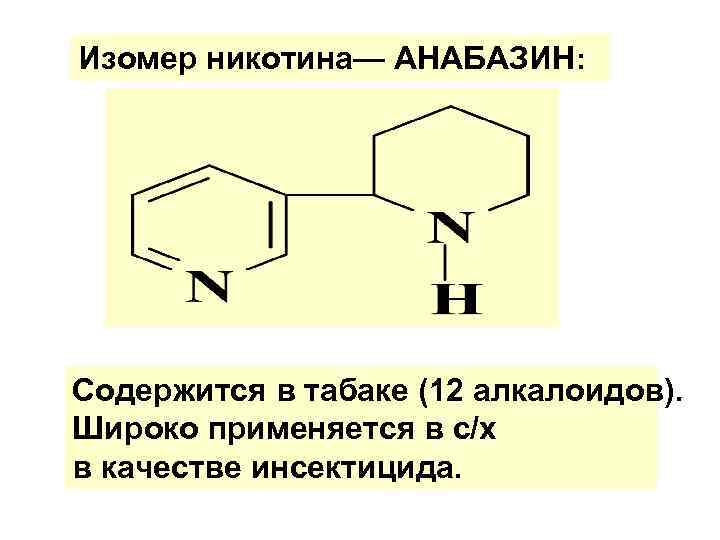 Изомер никотина— АНАБАЗИН: Содержится в табаке (12 алкалоидов). Широко применяется в с/х в качестве инсектицида.
Изомер никотина— АНАБАЗИН: Содержится в табаке (12 алкалоидов). Широко применяется в с/х в качестве инсектицида.
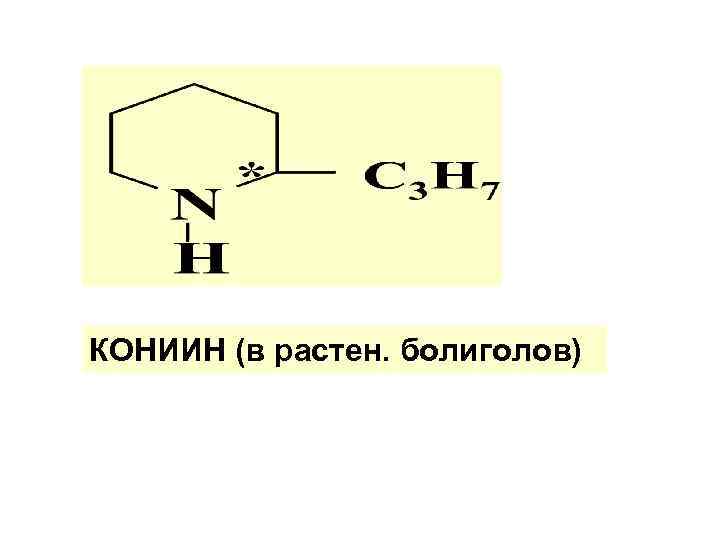 КОНИИН (в растен. болиголов)
КОНИИН (в растен. болиголов)
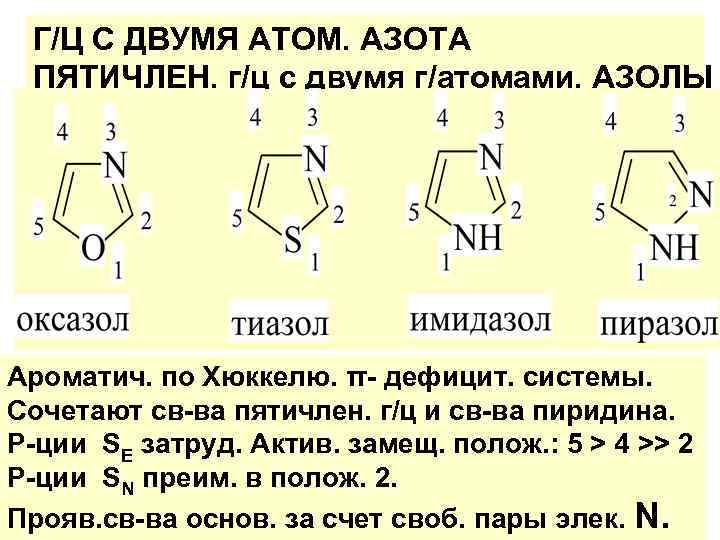 Г/Ц С ДВУМЯ АТОМ. АЗОТА ПЯТИЧЛЕН. г/ц с двумя г/атомами. АЗОЛЫ Ароматич. по Хюккелю. π- дефицит. системы. Сочетают св-ва пятичлен. г/ц и св-ва пиридина. Р-ции SE затруд. Актив. замещ. полож. : 5 > 4 >> 2 Р-ции SΝ преим. в полож. 2. Прояв. св-ва основ. за счет своб. пары элек. Ν.
Г/Ц С ДВУМЯ АТОМ. АЗОТА ПЯТИЧЛЕН. г/ц с двумя г/атомами. АЗОЛЫ Ароматич. по Хюккелю. π- дефицит. системы. Сочетают св-ва пятичлен. г/ц и св-ва пиридина. Р-ции SE затруд. Актив. замещ. полож. : 5 > 4 >> 2 Р-ции SΝ преим. в полож. 2. Прояв. св-ва основ. за счет своб. пары элек. Ν.
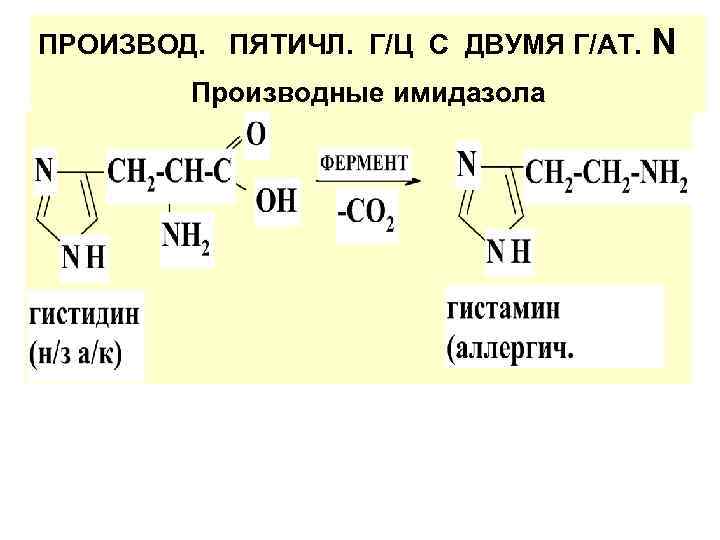 ПРОИЗВОД. ПЯТИЧЛ. Г/Ц С ДВУМЯ Г/АТ. Производные имидазола N
ПРОИЗВОД. ПЯТИЧЛ. Г/Ц С ДВУМЯ Г/АТ. Производные имидазола N
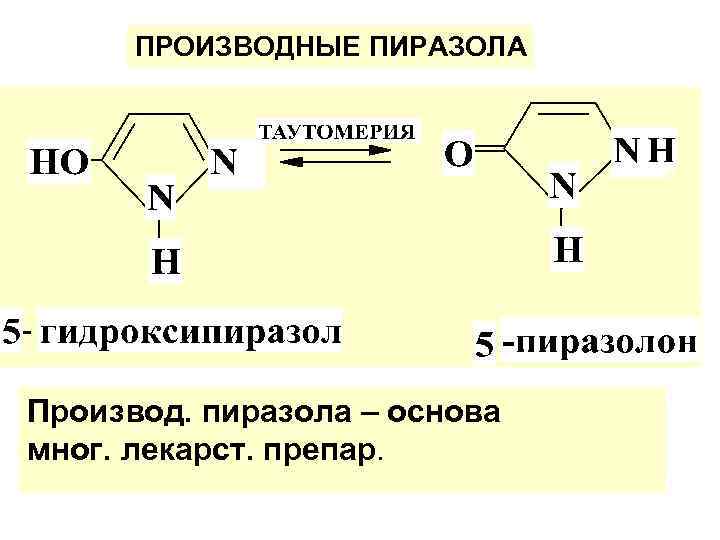 ПРОИЗВОДНЫЕ ПИРАЗОЛА Производ. пиразола – основа мног. лекарст. препар.
ПРОИЗВОДНЫЕ ПИРАЗОЛА Производ. пиразола – основа мног. лекарст. препар.
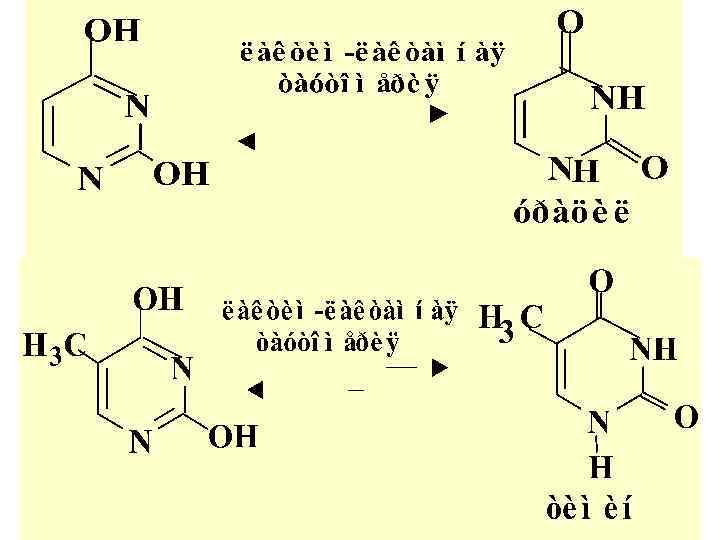
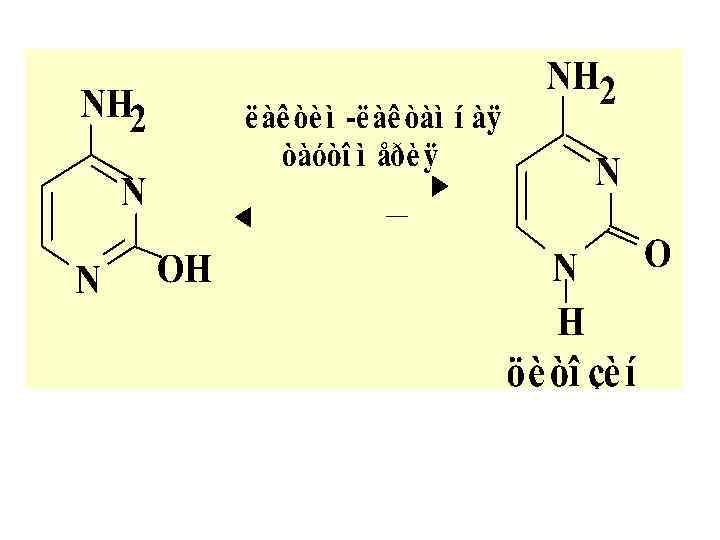
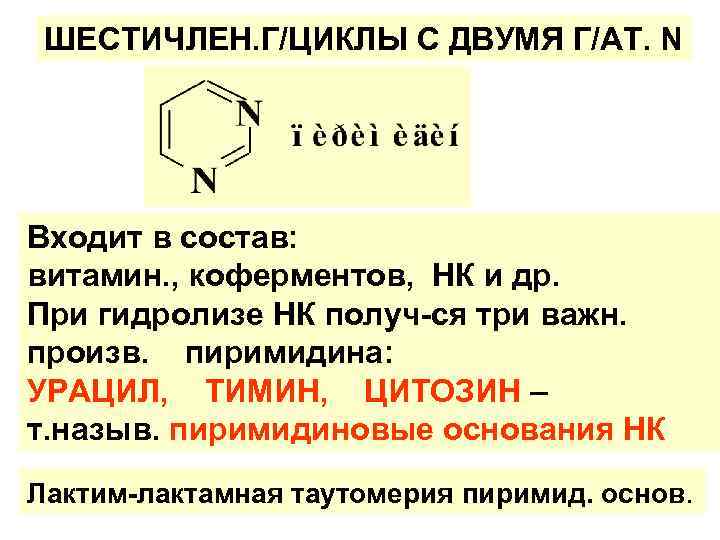 ШЕСТИЧЛЕН. Г/ЦИКЛЫ С ДВУМЯ Г/АТ. N Входит в состав: витамин. , коферментов, НК и др. При гидролизе НК получ-ся три важн. произв. пиримидина: УРАЦИЛ, ТИМИН, ЦИТОЗИН – т. назыв. пиримидиновые основания НК Лактим-лактамная таутомерия пиримид. основ.
ШЕСТИЧЛЕН. Г/ЦИКЛЫ С ДВУМЯ Г/АТ. N Входит в состав: витамин. , коферментов, НК и др. При гидролизе НК получ-ся три важн. произв. пиримидина: УРАЦИЛ, ТИМИН, ЦИТОЗИН – т. назыв. пиримидиновые основания НК Лактим-лактамная таутомерия пиримид. основ.
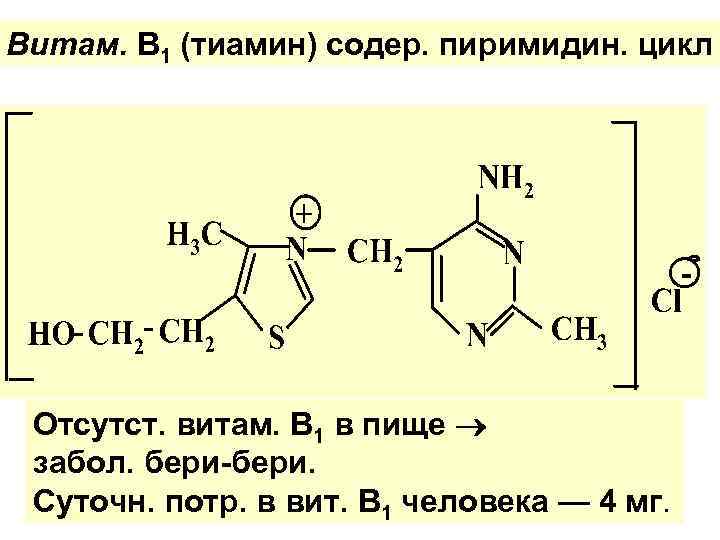 Витам. В 1 (тиамин) содер. пиримидин. цикл Отсутст. витам. В 1 в пище забол. бери-бери. Суточн. потр. в вит. В 1 человека — 4 мг.
Витам. В 1 (тиамин) содер. пиримидин. цикл Отсутст. витам. В 1 в пище забол. бери-бери. Суточн. потр. в вит. В 1 человека — 4 мг.
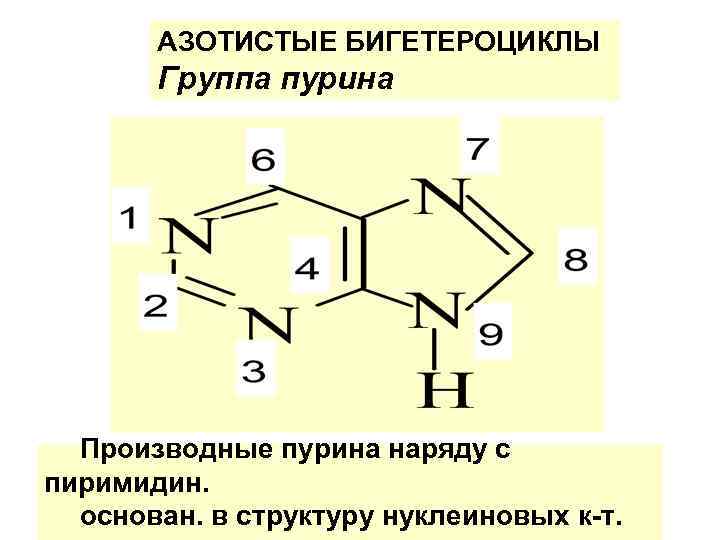 АЗОТИСТЫЕ БИГЕТЕРОЦИКЛЫ Группа пурина Производные пурина наряду с пиримидин. основан. в структуру нуклеиновых к-т.
АЗОТИСТЫЕ БИГЕТЕРОЦИКЛЫ Группа пурина Производные пурина наряду с пиримидин. основан. в структуру нуклеиновых к-т.
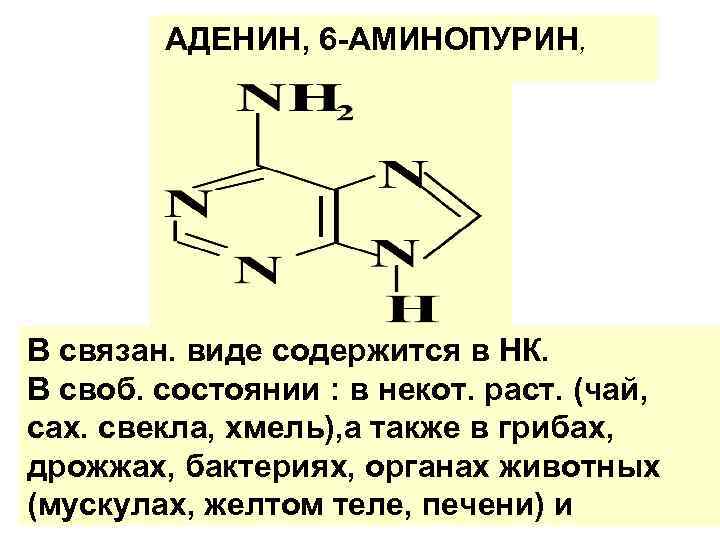 АДЕНИН, 6 -АМИНОПУРИН, В связан. виде содержится в НК. В своб. состоянии : в некот. раст. (чай, сах. свекла, хмель), а также в грибах, дрожжах, бактериях, органах животных (мускулах, желтом теле, печени) и
АДЕНИН, 6 -АМИНОПУРИН, В связан. виде содержится в НК. В своб. состоянии : в некот. раст. (чай, сах. свекла, хмель), а также в грибах, дрожжах, бактериях, органах животных (мускулах, желтом теле, печени) и
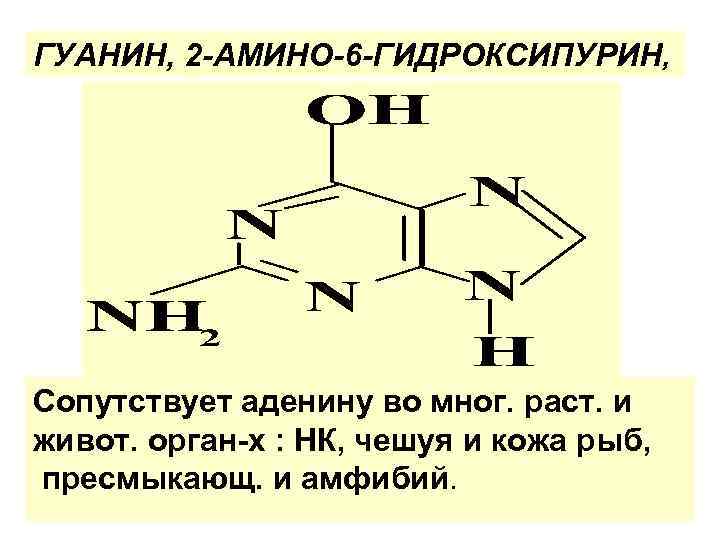 ГУАНИН, 2 -АМИНО-6 -ГИДРОКСИПУРИН, Сопутствует аденину во мног. раст. и живот. орган-х : НК, чешуя и кожа рыб, пресмыкающ. и амфибий.
ГУАНИН, 2 -АМИНО-6 -ГИДРОКСИПУРИН, Сопутствует аденину во мног. раст. и живот. орган-х : НК, чешуя и кожа рыб, пресмыкающ. и амфибий.
 ПОНЯТИЕ О СТРОЕНИИ НУКЛ. К-Т (НК) НК – БИОПОЛИМЕРЫ. Построены из мономеров -нуклеотидов, поэтому НК наз. полинуклеотидами. Нуклеотид включает: • г/ц основания, • углеводный остаток • фосфатную гр. У/водные комп-ты - пентозы : D-РИБОЗА и 2 - D-ДЕЗОКСИРИБОЗА. Отсюда НК подразд-ся на РНК, включ. рибозу и ДНК, содержащие дезоксирибозу.
ПОНЯТИЕ О СТРОЕНИИ НУКЛ. К-Т (НК) НК – БИОПОЛИМЕРЫ. Построены из мономеров -нуклеотидов, поэтому НК наз. полинуклеотидами. Нуклеотид включает: • г/ц основания, • углеводный остаток • фосфатную гр. У/водные комп-ты - пентозы : D-РИБОЗА и 2 - D-ДЕЗОКСИРИБОЗА. Отсюда НК подразд-ся на РНК, включ. рибозу и ДНК, содержащие дезоксирибозу.
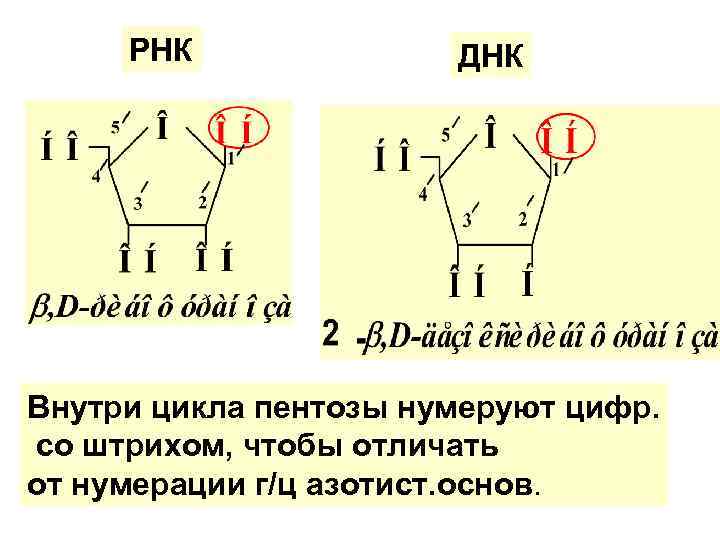 РНК ДНК Внутри цикла пентозы нумеруют цифр. со штрихом, чтобы отличать от нумерации г/ц азотист. основ.
РНК ДНК Внутри цикла пентозы нумеруют цифр. со штрихом, чтобы отличать от нумерации г/ц азотист. основ.
 Отличие в составе г/ц основ. , входящ. в состав РНК И ДНК: РНК УРАЦИЛ Цитозин Аденин Гуанин ДНК ТИМИН Цитозин Аденин Гуанин
Отличие в составе г/ц основ. , входящ. в состав РНК И ДНК: РНК УРАЦИЛ Цитозин Аденин Гуанин ДНК ТИМИН Цитозин Аденин Гуанин
 Схема мягк. кисл. или ферм. гидролиза НК: НК →нуклеотид → нуклеозид + Н 3 РО 4 НУКЛЕОЗИДЫ это N-гликозиды – природн. гликозиды пиримид. и пурин. основан. , соедин. с пентозами через атом N. В зав-ти от строения пентоз разл. : РИБОНУКЛЕОЗИДЫ и ДЕЗОКСИРИБОНУКЛЕОЗИДЫ.
Схема мягк. кисл. или ферм. гидролиза НК: НК →нуклеотид → нуклеозид + Н 3 РО 4 НУКЛЕОЗИДЫ это N-гликозиды – природн. гликозиды пиримид. и пурин. основан. , соедин. с пентозами через атом N. В зав-ти от строения пентоз разл. : РИБОНУКЛЕОЗИДЫ и ДЕЗОКСИРИБОНУКЛЕОЗИДЫ.
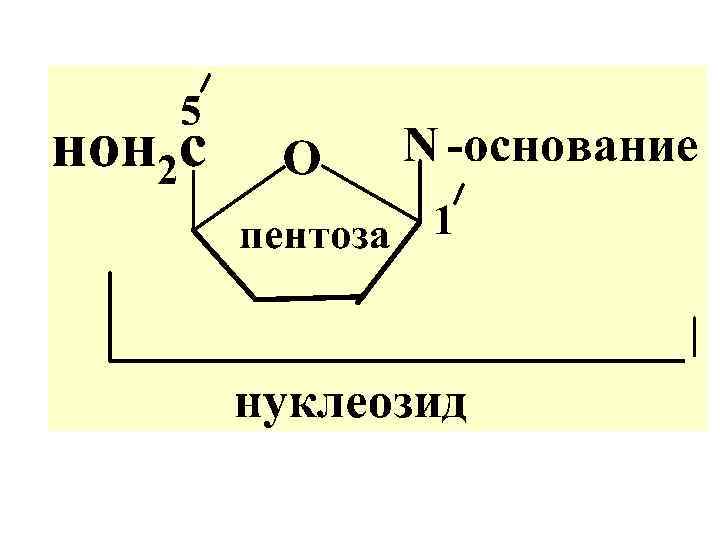
 НАЗВ. НУКЛЕОЗИДОВ Для пиримидиновых нуклеоз. : трив. назв. азот. основ + суфф. идин; Для пуриновых нуклеозидов: трив. назв. азот. основ. +суфф. озин Например: аденин + рибоза рибоаденозин цитозин + рибоза рибоцитидин
НАЗВ. НУКЛЕОЗИДОВ Для пиримидиновых нуклеоз. : трив. назв. азот. основ + суфф. идин; Для пуриновых нуклеозидов: трив. назв. азот. основ. +суфф. озин Например: аденин + рибоза рибоаденозин цитозин + рибоза рибоцитидин
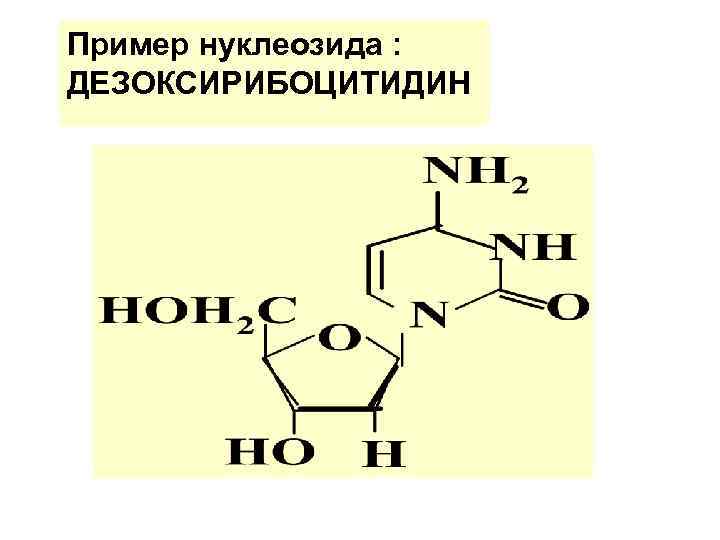 Пример нуклеозида : ДЕЗОКСИРИБОЦИТИДИН
Пример нуклеозида : ДЕЗОКСИРИБОЦИТИДИН
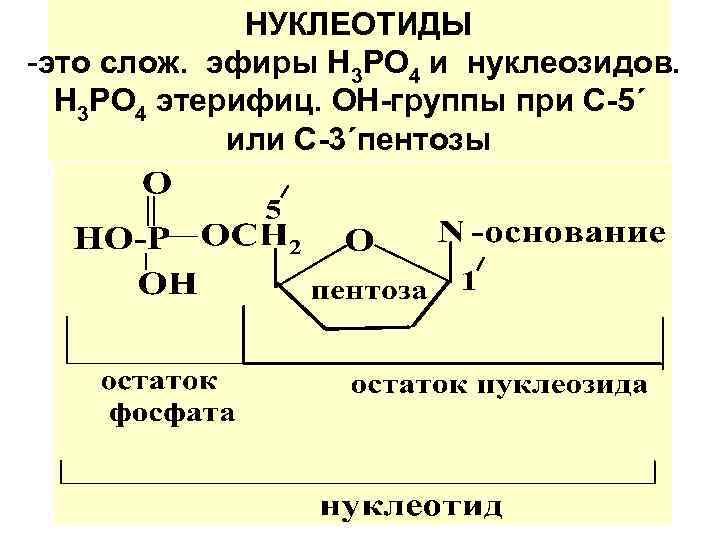 НУКЛЕОТИДЫ -это слож. эфиры Н 3 РО 4 и нуклеозидов. Н 3 РО 4 этерифиц. ОН-группы при С-5´ или С-3´пентозы
НУКЛЕОТИДЫ -это слож. эфиры Н 3 РО 4 и нуклеозидов. Н 3 РО 4 этерифиц. ОН-группы при С-5´ или С-3´пентозы
 Нуклеотиды называют : а) как соответствующие к-ты ; б)как эфиры (монофосф-ты) с указ. полож. фосф. ост-к Названия нуклеотидов КАК КИСЛОТ: 5´-адениловая к-та 3´-цитидиловая к-т КАК ЭФИРОВ: аденозин-5´- монофосфат цитидин-3´-монофосфат
Нуклеотиды называют : а) как соответствующие к-ты ; б)как эфиры (монофосф-ты) с указ. полож. фосф. ост-к Названия нуклеотидов КАК КИСЛОТ: 5´-адениловая к-та 3´-цитидиловая к-т КАК ЭФИРОВ: аденозин-5´- монофосфат цитидин-3´-монофосфат
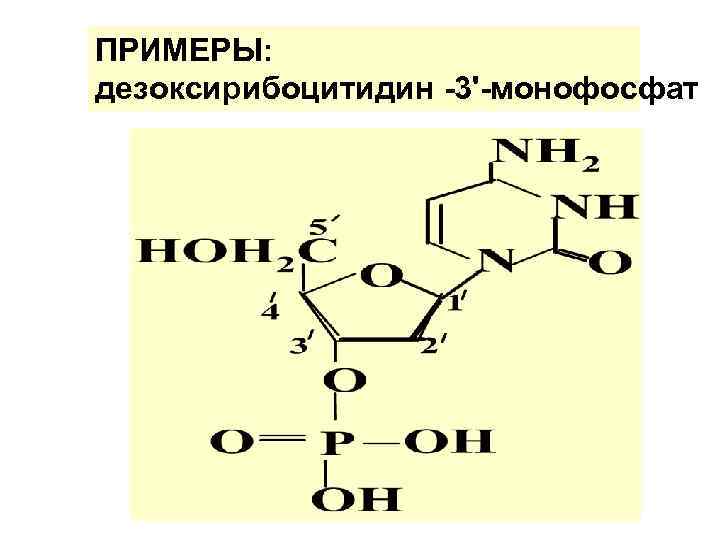 ПРИМЕРЫ: дезоксирибоцитидин -3'-монофосфат
ПРИМЕРЫ: дезоксирибоцитидин -3'-монофосфат
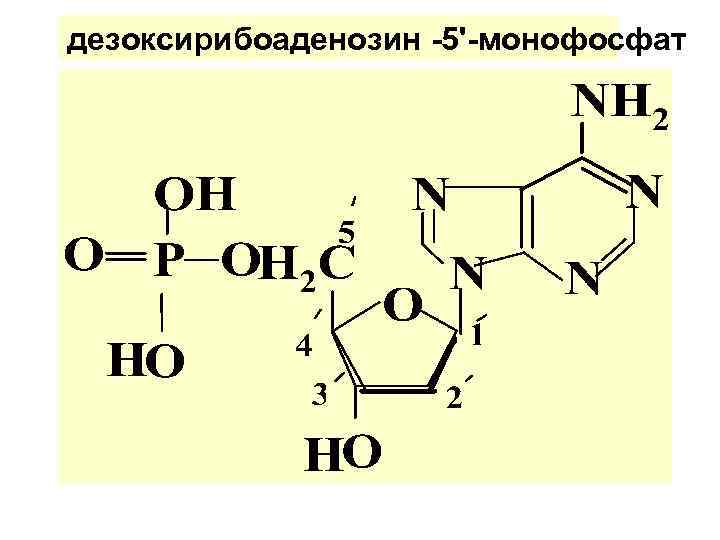 дезоксирибоаденозин -5'-монофосфат
дезоксирибоаденозин -5'-монофосфат
 НК выпол. гл. роль в передаче наследст. призн. и управл. биосинтез. белка. Комплементарные пары - пары , состоящие из пиримидин. и пуринов. основан. , определ. образом ориентир. в прост -ве и соедин. водород-ми связями. Комплементарные пары в ДНК: АДЕНИН –ТИМИН и ГУАНИН –ЦИТОЗИН. Комплементарность цепей и последов. звеньев - хим. основа важн. функций НК: ДНК- хран. и передача наследст. информации, а РНК – непосред. участие в биосинтезе белка.
НК выпол. гл. роль в передаче наследст. призн. и управл. биосинтез. белка. Комплементарные пары - пары , состоящие из пиримидин. и пуринов. основан. , определ. образом ориентир. в прост -ве и соедин. водород-ми связями. Комплементарные пары в ДНК: АДЕНИН –ТИМИН и ГУАНИН –ЦИТОЗИН. Комплементарность цепей и последов. звеньев - хим. основа важн. функций НК: ДНК- хран. и передача наследст. информации, а РНК – непосред. участие в биосинтезе белка.


