Фотосинтез. История изучения вопроса. Строение фотосинтетического аппараты























Лекция 7. История изучений фс. Пигменты.ppt
- Количество слайдов: 26
 Фотосинтез. История изучения вопроса. Строение фотосинтетического аппараты высших растений
Фотосинтез. История изучения вопроса. Строение фотосинтетического аппараты высших растений
 План § 1. Значение фотосинтеза § 2. История изучения фотосинтеза § 3. Хлоропласт. Строение § 4. Пигменты фотосинтеза § 4. 1. Хлорофиллы § 4. 2. Фикобилины § 4. 3. Каротиноиды
План § 1. Значение фотосинтеза § 2. История изучения фотосинтеза § 3. Хлоропласт. Строение § 4. Пигменты фотосинтеза § 4. 1. Хлорофиллы § 4. 2. Фикобилины § 4. 3. Каротиноиды
 Фотосинтез – процесс трансформации поглощенной организмом энергии света в химическую энергию органических (и неорганичесих) соединений.
Фотосинтез – процесс трансформации поглощенной организмом энергии света в химическую энергию органических (и неорганичесих) соединений.
 Значение фотосинтеза § Делает доступной энергию света для всего живого в виде пищи § Обеспечивает все живое кислородом § Снижая содержание углекислого газа, защищает планету от «парникового эффекта»
Значение фотосинтеза § Делает доступной энергию света для всего живого в виде пищи § Обеспечивает все живое кислородом § Снижая содержание углекислого газа, защищает планету от «парникового эффекта»
 История изучения вопроса § Английский химик Дж. Пристли (1771 г. ) основоположник экспериментального изучения фотосинтеза § Голландский врач Я. Ингенгауз доказал, что выделение кислорода растениями происходит только на свету § В 1782 г. швейцарский естествоиспытатель Ж. Сенебье
История изучения вопроса § Английский химик Дж. Пристли (1771 г. ) основоположник экспериментального изучения фотосинтеза § Голландский врач Я. Ингенгауз доказал, что выделение кислорода растениями происходит только на свету § В 1782 г. швейцарский естествоиспытатель Ж. Сенебье
 § Швейцарский ученый Т. Соссюр в 1804 г. . используя количественные методы анализа, обнаружил, что для увеличения вегетативной массы растения потребляют не только углекислый газ, но и воду. § В 1817 г. французские химики П. Ж. Пельтье и Ж. Каванту выделили из листьев зеленый пигмент и назвали его хлорофиллом. § В 1865 г. немецкий физиолог растений Ю. Сакс продемонстрировал, что на свету в листьях образуется крахмал и что он локализован в хлоропластах.
§ Швейцарский ученый Т. Соссюр в 1804 г. . используя количественные методы анализа, обнаружил, что для увеличения вегетативной массы растения потребляют не только углекислый газ, но и воду. § В 1817 г. французские химики П. Ж. Пельтье и Ж. Каванту выделили из листьев зеленый пигмент и назвали его хлорофиллом. § В 1865 г. немецкий физиолог растений Ю. Сакс продемонстрировал, что на свету в листьях образуется крахмал и что он локализован в хлоропластах.
 § В середине 19 в. в работах. американского физика Дж. У. Дрепер, Ю. Сакса и Пфеффера появились первые сведения о роли света в процессе фотосинтеза § 1875 г. К. А. Тимирязев установил, что ассимиляция углекислого газа максимальна при освещении красным светом, определил роль хлорофилла в процессе фотосинтеза и сформулировал идею о космической роли этого процесса.
§ В середине 19 в. в работах. американского физика Дж. У. Дрепер, Ю. Сакса и Пфеффера появились первые сведения о роли света в процессе фотосинтеза § 1875 г. К. А. Тимирязев установил, что ассимиляция углекислого газа максимальна при освещении красным светом, определил роль хлорофилла в процессе фотосинтеза и сформулировал идею о космической роли этого процесса.
 Общая формула фотосинтеза свет, хлорофилл § 6 СО 2 + 6 Н 2 О → С 6 Н 12 О 6 + 6 О 2
Общая формула фотосинтеза свет, хлорофилл § 6 СО 2 + 6 Н 2 О → С 6 Н 12 О 6 + 6 О 2
 § Немецкий химик А. Байер в 1870 г. . предположил, что под воздействием света происходит разложение углекислого газа и что для синтеза углеводов используются промежуточные продукты – СО и формальдегид. § В 1893 г. русский биохимик А. Н. Бах предположил, что О 2 выделяется из воды через промежуточные перекисные соединения.
§ Немецкий химик А. Байер в 1870 г. . предположил, что под воздействием света происходит разложение углекислого газа и что для синтеза углеводов используются промежуточные продукты – СО и формальдегид. § В 1893 г. русский биохимик А. Н. Бах предположил, что О 2 выделяется из воды через промежуточные перекисные соединения.
 Полное уравнение фотосинтеза по Ван Нилю ( 1937 -1941 гг. ) свет, хлорофилл СО 2 + 4 Н 2 О → [СН 2 О] + 3 Н 2 О + О 2 свет, хлорофилл 1. 4 Н 2 О → 4 [ОН] + 4 [Н] 2. СО 2 + 4 [Н] → [СН 2 О] + Н 2 О 3. 4 [ОН] → 2 Н 2 О + О 2
Полное уравнение фотосинтеза по Ван Нилю ( 1937 -1941 гг. ) свет, хлорофилл СО 2 + 4 Н 2 О → [СН 2 О] + 3 Н 2 О + О 2 свет, хлорофилл 1. 4 Н 2 О → 4 [ОН] + 4 [Н] 2. СО 2 + 4 [Н] → [СН 2 О] + Н 2 О 3. 4 [ОН] → 2 Н 2 О + О 2
 § Прямые экспериментальные. доказательства фотолиза воды с помощью меченного кислорода были получены в 1941 г. независимо А. П. Виноградовым (СССР) и Р. В. Тейсом (США). § Экспериментальные доказательства реального существования двух фаз фотосинтеза были получены в опытах с мигающим светом А. А. Рихтером (СССР) и Р. Эмерсоном, У. Арнольдом (США).
§ Прямые экспериментальные. доказательства фотолиза воды с помощью меченного кислорода были получены в 1941 г. независимо А. П. Виноградовым (СССР) и Р. В. Тейсом (США). § Экспериментальные доказательства реального существования двух фаз фотосинтеза были получены в опытах с мигающим светом А. А. Рихтером (СССР) и Р. Эмерсоном, У. Арнольдом (США).
 Структура хлоропласта
Структура хлоропласта
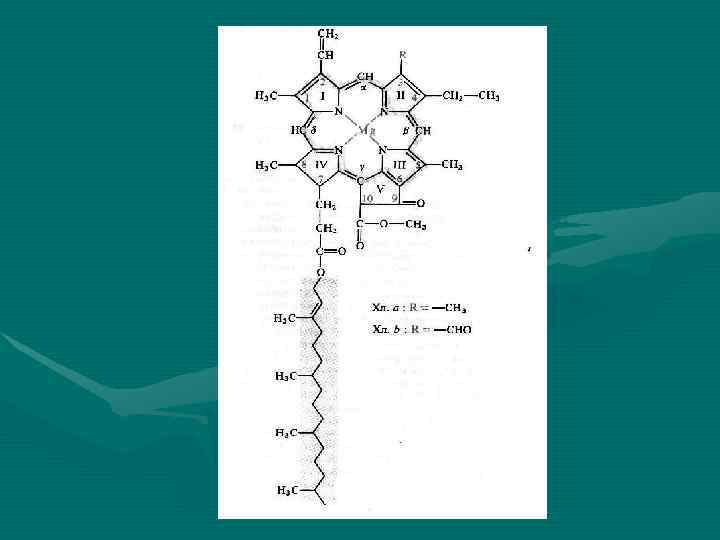
 Хлорофилл • – сложный эфир дикарбоновой кислоты хлорофиллина, у которой одна карбоксильная группа этерефицирована остатком метилового спирта, а другая – остатком непредельного спитра фитола. Элементарный состав хлорофилла а - С 55 Н 72 О 5 N 4 Мg и хлорофилла в – С 55 Н 70 О 6 N 4 Mg
Хлорофилл • – сложный эфир дикарбоновой кислоты хлорофиллина, у которой одна карбоксильная группа этерефицирована остатком метилового спирта, а другая – остатком непредельного спитра фитола. Элементарный состав хлорофилла а - С 55 Н 72 О 5 N 4 Мg и хлорофилла в – С 55 Н 70 О 6 N 4 Mg
 .
.
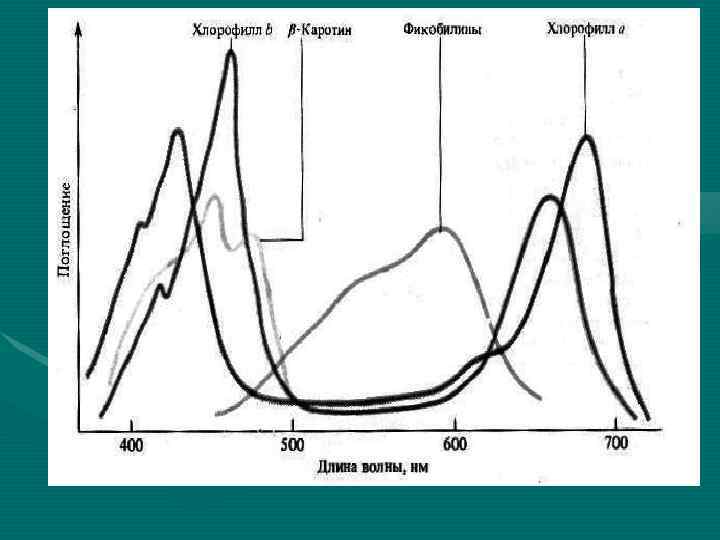
 Физико-химические свойства хлороф 1. не растворим в воде; 2. хорошо растворимы в этиловом эфире, бензоле, хлороформе, ацетоне, этиловом спирте; 3. два максимума поглощения света – в синей (430 -460 нм) и красной (650 -700 нм) областях спектра; 4. растворы хлорофилла в полярных растворителях обладают яркой флуоресценцией (люминесценцией). В этиловом эфире у хлорофилла а наблюдается рубиново- красная флуоресценция; 5. растворы хлорофиллов способны также к фосфоресценции (т. е. длительному послесвечению), максимум которого лежит в инфракрасной области.
Физико-химические свойства хлороф 1. не растворим в воде; 2. хорошо растворимы в этиловом эфире, бензоле, хлороформе, ацетоне, этиловом спирте; 3. два максимума поглощения света – в синей (430 -460 нм) и красной (650 -700 нм) областях спектра; 4. растворы хлорофилла в полярных растворителях обладают яркой флуоресценцией (люминесценцией). В этиловом эфире у хлорофилла а наблюдается рубиново- красная флуоресценция; 5. растворы хлорофиллов способны также к фосфоресценции (т. е. длительному послесвечению), максимум которого лежит в инфракрасной области.
 .
.
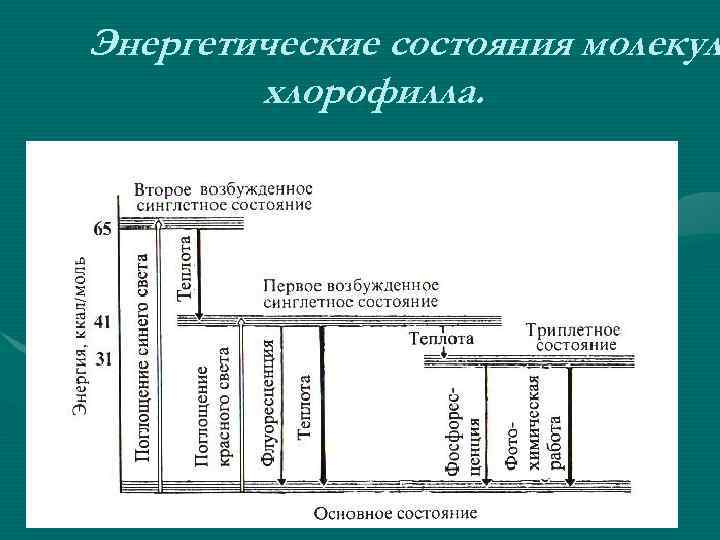
 Энергетические состояния молекул хлорофилла.
Энергетические состояния молекул хлорофилла.
 Функции молекулы хлорофилла: u- избирательное поглощение энергии света; u - запасание ее в виде энергии электронного возбуждения; u - фотохимическое преобразование энергии возбужденного состояния в химическую энергию первичных фотовосстановленных и фотоокисленных соединений.
Функции молекулы хлорофилла: u- избирательное поглощение энергии света; u - запасание ее в виде энергии электронного возбуждения; u - фотохимическое преобразование энергии возбужденного состояния в химическую энергию первичных фотовосстановленных и фотоокисленных соединений.
 Фикобилины n Это хромофорная часть фикобилипротеинов. Эта группа пигментов характерна для красных, синезеленых и криптофитовых водорослей. Наиболее известны представители фикобилинов – фикоэритробилины, аллофикоцианобилины и фикоцианобилины. По химической структуре – это тетрапирролы с открытой цепью, имеющих ситему коньюгированных двойных и одинарных связей. В своем составе они не содержат атомов магния, других металлов, а также фитола. Фикобилипротеины растворимы в воде.
Фикобилины n Это хромофорная часть фикобилипротеинов. Эта группа пигментов характерна для красных, синезеленых и криптофитовых водорослей. Наиболее известны представители фикобилинов – фикоэритробилины, аллофикоцианобилины и фикоцианобилины. По химической структуре – это тетрапирролы с открытой цепью, имеющих ситему коньюгированных двойных и одинарных связей. В своем составе они не содержат атомов магния, других металлов, а также фитола. Фикобилипротеины растворимы в воде.
 Максимум поглощения фикобилинов: n фикоэритрины – 498 -568 нм (оранжевая часть спектра); n фикоцианины – 585 -630 нм (желтая); аллофикоцианины – 585 -650 нм (зеленая). n Таким образом, максимуму поглощения света у фикобилинов находятся между максимумами поглощения у хлорофилла аиb
Максимум поглощения фикобилинов: n фикоэритрины – 498 -568 нм (оранжевая часть спектра); n фикоцианины – 585 -630 нм (желтая); аллофикоцианины – 585 -650 нм (зеленая). n Таким образом, максимуму поглощения света у фикобилинов находятся между максимумами поглощения у хлорофилла аиb
 Функции фикобилинов n. Входятв светособирающий комплекс
Функции фикобилинов n. Входятв светособирающий комплекс
 Каротиноиды n – жирорастворимые пигменты желтого, оранжевого и красного цвета.
Каротиноиды n – жирорастворимые пигменты желтого, оранжевого и красного цвета.
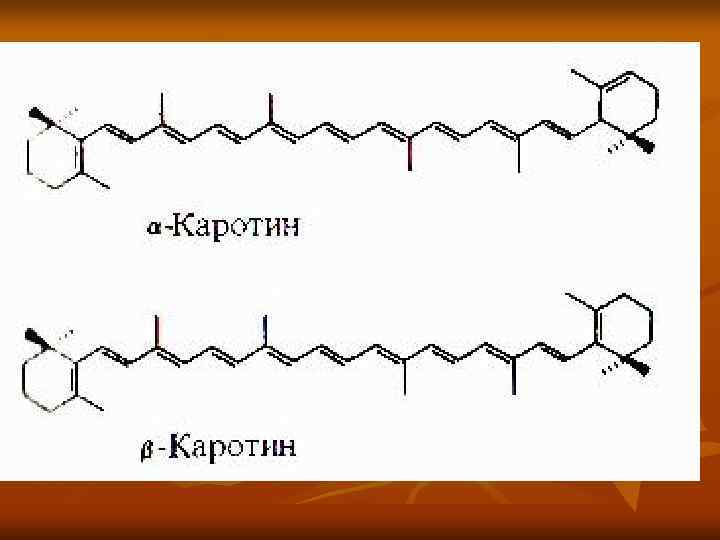
 Классификация каротиноидов n 1) оранжевые или красные пигменты каротины (С 40 Н 56); n 2) желтые ксантофиллы (С 40 Н 56 О 2 и С 40 Н 56 О 4); n 3) каротиноидные кислоты – продукты окисления каротиноидов с укороченной цепочкой и карбоксильными группами.
Классификация каротиноидов n 1) оранжевые или красные пигменты каротины (С 40 Н 56); n 2) желтые ксантофиллы (С 40 Н 56 О 2 и С 40 Н 56 О 4); n 3) каротиноидные кислоты – продукты окисления каротиноидов с укороченной цепочкой и карбоксильными группами.
 .
.
 Физико-химическме свойства каротиноидов n Каротины и ксантофиллы хорошо растворимы в хлороформе, бензоле, сероуглероде, ацетоне. Каротины легко растворимы в эфирах, но не растворимы в метаноле, этаноле. Ксантофиллы хорошо ратворимы в спиртах и значительно хуже в петролейном эфире. n Спектры поглощения каротиноидов характеризуются двумя полосами в фиолетово- синей и синей области (от 400 до 500 нм).
Физико-химическме свойства каротиноидов n Каротины и ксантофиллы хорошо растворимы в хлороформе, бензоле, сероуглероде, ацетоне. Каротины легко растворимы в эфирах, но не растворимы в метаноле, этаноле. Ксантофиллы хорошо ратворимы в спиртах и значительно хуже в петролейном эфире. n Спектры поглощения каротиноидов характеризуются двумя полосами в фиолетово- синей и синей области (от 400 до 500 нм).
 Функции каротиноидов n 1) участвуют в поглощении света в качестве дополнительных пигментов; n 2) зашищают молекулу хлорофилла от необратимого фотоокисления, т. е. выполняют функцию фотопротекторов; n 3) необходимы для фототропизмов растений и фототаксисов у жгутиковых; n 4) обусловливают цвет лепестков и плодов, делая их более привлекательными; n 5) некоторые производные каротиноидов – витамин А, ксантоксин действуют подобно фитогормону АБК и других биологически активных веществ.
Функции каротиноидов n 1) участвуют в поглощении света в качестве дополнительных пигментов; n 2) зашищают молекулу хлорофилла от необратимого фотоокисления, т. е. выполняют функцию фотопротекторов; n 3) необходимы для фототропизмов растений и фототаксисов у жгутиковых; n 4) обусловливают цвет лепестков и плодов, делая их более привлекательными; n 5) некоторые производные каротиноидов – витамин А, ксантоксин действуют подобно фитогормону АБК и других биологически активных веществ.

