Фосфор Историческая справка Фосфор открыт гамбургским














fosfor.pptx
- Размер: 164.5 Кб
- Автор:
- Количество слайдов: 17
Описание презентации Фосфор Историческая справка Фосфор открыт гамбургским по слайдам
 Фосфор
Фосфор
 Историческая справка Фосфор открыт гамбургским алхимиком Геннингом Брандом в 1669 г. Подобно другим алхимикам, Бранд пытался отыскать эликсир жизни или философский камень, а получил светящееся вещество. Существуют данные, что фосфор умели получать еще арабские алхимики в XII в. То, что фосфор – простое вещество доказал Лавуазье. Название «фосфор» происходит от греческих слов «фос» – свет и «феро» – несу.
Историческая справка Фосфор открыт гамбургским алхимиком Геннингом Брандом в 1669 г. Подобно другим алхимикам, Бранд пытался отыскать эликсир жизни или философский камень, а получил светящееся вещество. Существуют данные, что фосфор умели получать еще арабские алхимики в XII в. То, что фосфор – простое вещество доказал Лавуазье. Название «фосфор» происходит от греческих слов «фос» – свет и «феро» – несу.
 Строение На внешнем энергетическом уровне атома фосфора содержится 5 электронов, которые имеют электронную конфигурацию 3 s 2 3 p 3. Фосфор проявляет степени окисления -3, +5. Фосфор – типичный неметалл, в зависимости от типа превращения элемент может быть окислителем и восстановителем.
Строение На внешнем энергетическом уровне атома фосфора содержится 5 электронов, которые имеют электронную конфигурацию 3 s 2 3 p 3. Фосфор проявляет степени окисления -3, +5. Фосфор – типичный неметалл, в зависимости от типа превращения элемент может быть окислителем и восстановителем.
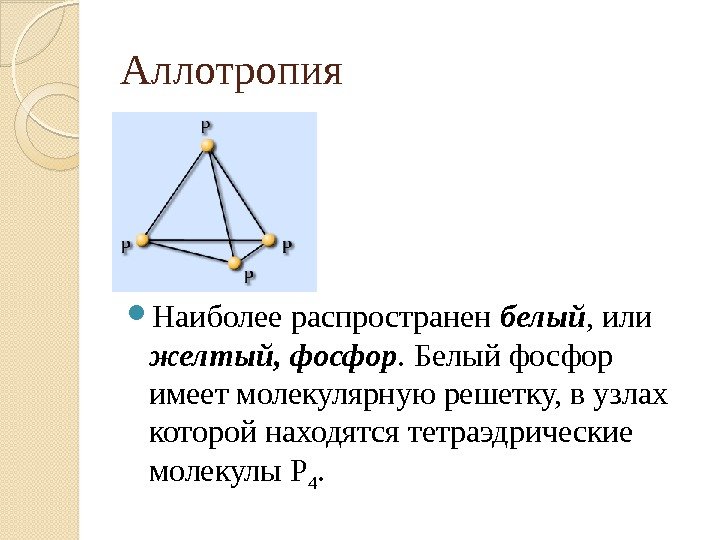
 Аллотропия Наиболее распространен белый , или желтый, фосфор. Белый фосфор имеет молекулярную решетку, в узлах которой находятся тетраэдрические молекулы Р 4.
Аллотропия Наиболее распространен белый , или желтый, фосфор. Белый фосфор имеет молекулярную решетку, в узлах которой находятся тетраэдрические молекулы Р 4.
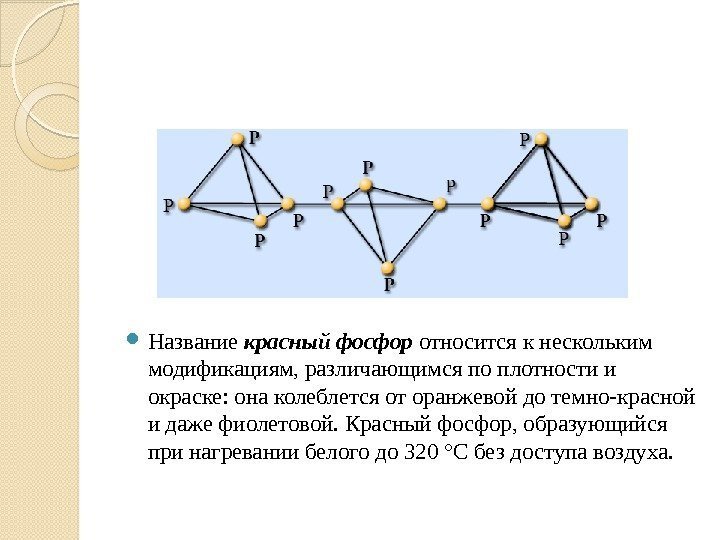
 Название красный фосфор относится к нескольким модификациям, различающимся по плотности и окраске: она колеблется от оранжевой до темно-красной и даже фиолетовой. Красный фосфор, образующийся при нагревании белого до 320 °С без доступа воздуха.
Название красный фосфор относится к нескольким модификациям, различающимся по плотности и окраске: она колеблется от оранжевой до темно-красной и даже фиолетовой. Красный фосфор, образующийся при нагревании белого до 320 °С без доступа воздуха.
 При повышенном давлении белый фосфор переходит в черный фосфор. Это самая устойчивая модификация фосфора. Кристаллический черный фосфор тоже имеет несколько модификаций. Ромбическая модификация построена из гексагональных колец Р 6 , упакованных в слои, причем кольца не являются плоскими.
При повышенном давлении белый фосфор переходит в черный фосфор. Это самая устойчивая модификация фосфора. Кристаллический черный фосфор тоже имеет несколько модификаций. Ромбическая модификация построена из гексагональных колец Р 6 , упакованных в слои, причем кольца не являются плоскими.
 Получение Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и песком при температуре 1500 °С: 2 Ca 3 (PO 4 ) 2 + 10 C + 6 Si. O 2 = 4 P + 10 CO + 6 Ca. Si. O 3. Образующиеся пары белого фосфора конденсируются в приемнике под водой. Вместо фосфоритов восстановлению можно подвергнуть и другие соединения, например, метафосфорную кислоту: 4 HPO 3 + 12 C = 4 P + 2 H 2 + 12 CO.
Получение Фосфор получают из апатитов или фосфоритов в результате взаимодействия с коксом и песком при температуре 1500 °С: 2 Ca 3 (PO 4 ) 2 + 10 C + 6 Si. O 2 = 4 P + 10 CO + 6 Ca. Si. O 3. Образующиеся пары белого фосфора конденсируются в приемнике под водой. Вместо фосфоритов восстановлению можно подвергнуть и другие соединения, например, метафосфорную кислоту: 4 HPO 3 + 12 C = 4 P + 2 H 2 + 12 CO.
 Химические свойства Взаимодействие с простыми веществами Фосфор легко окисляется кислородом: 4 P + 5 O 2 = 2 P 2 O 5 , 4 P + 3 O 2 = 2 P 2 O 3. с металлами – окислитель, образует фосфиды: 2 P + 3 Ca = Ca 3 P 2.
Химические свойства Взаимодействие с простыми веществами Фосфор легко окисляется кислородом: 4 P + 5 O 2 = 2 P 2 O 5 , 4 P + 3 O 2 = 2 P 2 O 3. с металлами – окислитель, образует фосфиды: 2 P + 3 Ca = Ca 3 P 2.
 с неметаллами – восстановитель : 2 P + 3 S = P 2 S 3 , 2 P + 3 Cl 2 = 2 PCl 3. Взаимодействует с водой, при этом диспропорционирует: 4 Р + 6 Н 2 О = РН 3 + 3 Н 3 РО 2 (фосфорноватистая кислота). В растворах щелочей диспропорционирование происходит в большей степени: 4 Р + 3 KOH + 3 Н 2 О = РН 3 + 3 KН 2 РО 2 . Сильные окислители превращают фосфор в фосфорную кислоту: 3 P + 5 HNO 3 + 2 H 2 O = 3 H 3 PO 4 + 5 NO; 2 P + 5 H 2 SO 4 = 2 H 3 PO 4 + 5 SO 2 + 2 H 2 O. 6 P + 5 KCl. O 3 = 5 KCl + 3 P 2 O 5.
с неметаллами – восстановитель : 2 P + 3 S = P 2 S 3 , 2 P + 3 Cl 2 = 2 PCl 3. Взаимодействует с водой, при этом диспропорционирует: 4 Р + 6 Н 2 О = РН 3 + 3 Н 3 РО 2 (фосфорноватистая кислота). В растворах щелочей диспропорционирование происходит в большей степени: 4 Р + 3 KOH + 3 Н 2 О = РН 3 + 3 KН 2 РО 2 . Сильные окислители превращают фосфор в фосфорную кислоту: 3 P + 5 HNO 3 + 2 H 2 O = 3 H 3 PO 4 + 5 NO; 2 P + 5 H 2 SO 4 = 2 H 3 PO 4 + 5 SO 2 + 2 H 2 O. 6 P + 5 KCl. O 3 = 5 KCl + 3 P 2 O 5.
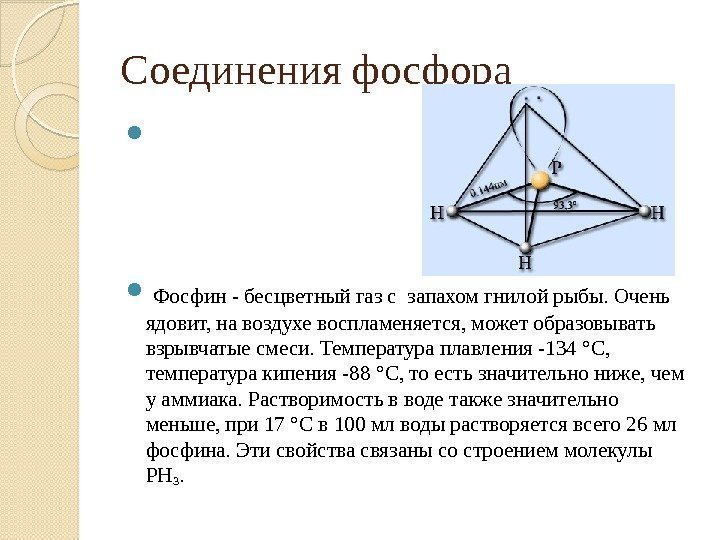
 Соединения фосфора Фосфин — бесцветный газ с запахом гнилой рыбы. Очень ядовит, на воздухе воспламеняется, может образовывать взрывчатые смеси. Температура плавления -134 °С, температура кипения -88 °С, то есть значительно ниже, чем у аммиака. Растворимость в воде также значительно меньше, при 17 °С в 100 мл воды растворяется всего 26 мл фосфина. Эти свойства связаны со строением молекулы РН 3.
Соединения фосфора Фосфин — бесцветный газ с запахом гнилой рыбы. Очень ядовит, на воздухе воспламеняется, может образовывать взрывчатые смеси. Температура плавления -134 °С, температура кипения -88 °С, то есть значительно ниже, чем у аммиака. Растворимость в воде также значительно меньше, при 17 °С в 100 мл воды растворяется всего 26 мл фосфина. Эти свойства связаны со строением молекулы РН 3.
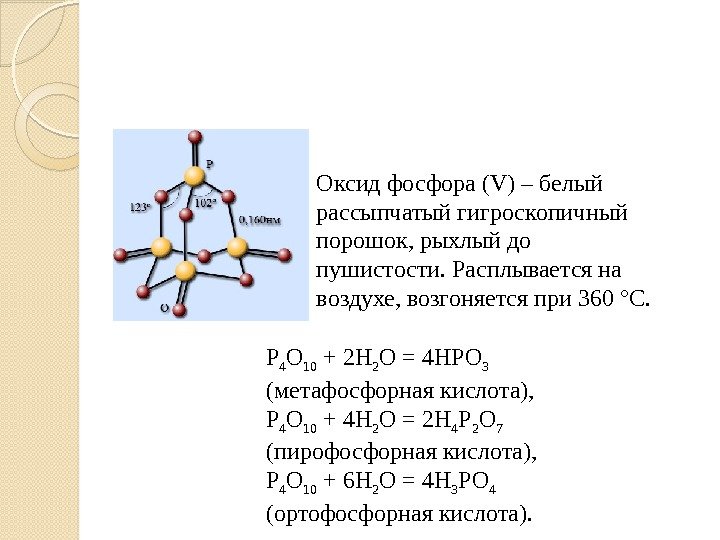
 Оксид фосфора (V) – белый рассыпчатый гигроскопичный порошок, рыхлый до пушистости. Расплывается на воздухе, возгоняется при 360 °С. P 4 O 10 + 2 H 2 O = 4 HPO 3 (метафосфорная кислота), P 4 O 10 + 4 H 2 O = 2 H 4 P 2 O 7 (пирофосфорная кислота), P 4 O 10 + 6 H 2 O = 4 H 3 PO 4 (ортофосфорная кислота).
Оксид фосфора (V) – белый рассыпчатый гигроскопичный порошок, рыхлый до пушистости. Расплывается на воздухе, возгоняется при 360 °С. P 4 O 10 + 2 H 2 O = 4 HPO 3 (метафосфорная кислота), P 4 O 10 + 4 H 2 O = 2 H 4 P 2 O 7 (пирофосфорная кислота), P 4 O 10 + 6 H 2 O = 4 H 3 PO 4 (ортофосфорная кислота).
 Свойства кислотного оксида Типичный кислотный оксид: 6 Ca. O + P 4 O 10 = 2 Ca 3 (PO 4 ) 2 , 6 Ca(OH) 2 + P 4 O 10 = 2 Ca 3 (PO 4 ) 2 + 6 H 2 O. Водоотнимающее свойство Эффективное водоотнимающее средство, способен превращать азотную и серную кислоты в оксиды: 2 HNO 3 + P 2 O 5 = 2 HPO 3 + N 2 O 5 ; H 2 SO 4 + P 2 O 5 = 2 HPO 3 + SO 3. Получается при горении фосфора в избытке кислорода: 4 Р + 2 О 5 = Р 4 О 10.
Свойства кислотного оксида Типичный кислотный оксид: 6 Ca. O + P 4 O 10 = 2 Ca 3 (PO 4 ) 2 , 6 Ca(OH) 2 + P 4 O 10 = 2 Ca 3 (PO 4 ) 2 + 6 H 2 O. Водоотнимающее свойство Эффективное водоотнимающее средство, способен превращать азотную и серную кислоты в оксиды: 2 HNO 3 + P 2 O 5 = 2 HPO 3 + N 2 O 5 ; H 2 SO 4 + P 2 O 5 = 2 HPO 3 + SO 3. Получается при горении фосфора в избытке кислорода: 4 Р + 2 О 5 = Р 4 О 10.
 Фосфорноватистая кислота – это белые кристаллы, хорошо растворимые в воде и в органических растворителях. Температура плавления 27 °С. Химические свойства Одноосновная кислота средней силы. Очень сильный восстановитель: 5 H 3 PO 2 + 4 KMn. O 4 + 6 H 2 SO 4 = 5 H 3 PO 4 + 4 Mn. SO 4 + 2 K 2 SO 4 + 6 H 2 O. При температуре около 50 °С разлагается: 3 H 3 PO 2 = PH 3 + 2 H 3 PO 3. Соли – гипофосфиты. Практически все хорошо растворимы в воде, соли переходных металлов мгновенно разлагаются. Получение При диспропорционировании белого фосфора в концентрированной щелочи образуется гипофосфит – соль фосфорноватистой кислоты, раствор кислоты легко получается действием серной кислоты на гипофосфит: 2 P 4 + 3 Ba(OH) 2 + 6 H 2 O = PH 3 + 3 Ba(H 2 PO 2 ) 2 ; Ba(H 2 PO 2 ) 2 + H 2 SO 4 = 2 H 3 PO 2 + Ba. SO 4.
Фосфорноватистая кислота – это белые кристаллы, хорошо растворимые в воде и в органических растворителях. Температура плавления 27 °С. Химические свойства Одноосновная кислота средней силы. Очень сильный восстановитель: 5 H 3 PO 2 + 4 KMn. O 4 + 6 H 2 SO 4 = 5 H 3 PO 4 + 4 Mn. SO 4 + 2 K 2 SO 4 + 6 H 2 O. При температуре около 50 °С разлагается: 3 H 3 PO 2 = PH 3 + 2 H 3 PO 3. Соли – гипофосфиты. Практически все хорошо растворимы в воде, соли переходных металлов мгновенно разлагаются. Получение При диспропорционировании белого фосфора в концентрированной щелочи образуется гипофосфит – соль фосфорноватистой кислоты, раствор кислоты легко получается действием серной кислоты на гипофосфит: 2 P 4 + 3 Ba(OH) 2 + 6 H 2 O = PH 3 + 3 Ba(H 2 PO 2 ) 2 ; Ba(H 2 PO 2 ) 2 + H 2 SO 4 = 2 H 3 PO 2 + Ba. SO 4.
 Фосфористая кислота – это бесцветные кристаллы, хорошо растворимые в воде и спирте, температура плавления 74 °С, температура разложения 197 °С. Химические свойства Двухосновная кислота средней силы. Является хорошим восстановителем, хотя и менее сильным, чем фосфорноватистая кислота, она также обесцвечивает раствор перманганата калия: 5 H 3 PO 3 + 2 KMn. O 4 + 3 H 2 SO 4 = 5 H 3 PO 4 + 2 Mn. SO 4 + K 2 SO 4 + 3 H 2 O. При нагревании до 200 °С разлагается: 4 H 3 PO 3 = PH 3 + 3 H 3 PO 4. Соли – фосфиты и гидрофосфиты. Практически все хорошо растворимы в воде, соли переходных металлов разлагаются: при незначительном нагревании: Ag 2 HPO 3 = 2 Ag + HPO 3. Получение Образуется при гидролизе трихлорида фосфора: PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HC l.
Фосфористая кислота – это бесцветные кристаллы, хорошо растворимые в воде и спирте, температура плавления 74 °С, температура разложения 197 °С. Химические свойства Двухосновная кислота средней силы. Является хорошим восстановителем, хотя и менее сильным, чем фосфорноватистая кислота, она также обесцвечивает раствор перманганата калия: 5 H 3 PO 3 + 2 KMn. O 4 + 3 H 2 SO 4 = 5 H 3 PO 4 + 2 Mn. SO 4 + K 2 SO 4 + 3 H 2 O. При нагревании до 200 °С разлагается: 4 H 3 PO 3 = PH 3 + 3 H 3 PO 4. Соли – фосфиты и гидрофосфиты. Практически все хорошо растворимы в воде, соли переходных металлов разлагаются: при незначительном нагревании: Ag 2 HPO 3 = 2 Ag + HPO 3. Получение Образуется при гидролизе трихлорида фосфора: PCl 3 + 3 H 2 O = H 3 PO 3 + 3 HC l.
 При комнатной температуре довольно инертна, при нагревании проявляет свойства кислот, относится к кислотам средней силы. Диссоциация в водном растворе: Н 3 РО 4 = Н 2 РО 4 — + Н 2 РО 4 — = НРО 4 2 — + НРО 4 2 — = РО 4 3 — + Н + Суммарное уравнение: Н 3 РО 4 = РО 4 3 — + 3 Н +. Свойства кислоты Реагирует с металлами, стоящими в ряду напряжений металлов до водорода: 3 Zn + 2 H 3 PO 4 = Zn 3 (PO 4 ) 2 + 3 H 2. С оксидами металлов: 3 Ca. O + 2 H 3 PO 4 = Ca 3 (PO 4 ) 2 + 3 H 2 O. С основаниями: 3 Ca(OН) 2 + 2 H 3 PO 4 = Ca 3 (PO 4 ) 2 + 6 Н 2 О; Ca(OН) 2 + H 3 PO 4 = Ca. НPO 4 + 2 Н 2 О; Ca(OН) 2 + 2 H 3 PO 4 = Ca(Н 2 PO 4 ) 2 + 2 Н 2 О. Не проявляет ни окислительных, ни восстановительных свойств.
При комнатной температуре довольно инертна, при нагревании проявляет свойства кислот, относится к кислотам средней силы. Диссоциация в водном растворе: Н 3 РО 4 = Н 2 РО 4 — + Н 2 РО 4 — = НРО 4 2 — + НРО 4 2 — = РО 4 3 — + Н + Суммарное уравнение: Н 3 РО 4 = РО 4 3 — + 3 Н +. Свойства кислоты Реагирует с металлами, стоящими в ряду напряжений металлов до водорода: 3 Zn + 2 H 3 PO 4 = Zn 3 (PO 4 ) 2 + 3 H 2. С оксидами металлов: 3 Ca. O + 2 H 3 PO 4 = Ca 3 (PO 4 ) 2 + 3 H 2 O. С основаниями: 3 Ca(OН) 2 + 2 H 3 PO 4 = Ca 3 (PO 4 ) 2 + 6 Н 2 О; Ca(OН) 2 + H 3 PO 4 = Ca. НPO 4 + 2 Н 2 О; Ca(OН) 2 + 2 H 3 PO 4 = Ca(Н 2 PO 4 ) 2 + 2 Н 2 О. Не проявляет ни окислительных, ни восстановительных свойств.
 Термический способ получения фосфорной кислоты основан на окислении элементарного фосфора в избытке воздуха с последующей гидратацией и образующегося оксида фосфора (V) и конденсацией фосфорной кислоты: 4 Р + 5 О 2 = Р 4 О 10 ; n. Р 4 О 10 + 2 n. H 2 O = 4(HPO 3 ) n при 700 °С, 4(HPO 3 ) n + 2 n. H 2 O = 2 n. H 4 P 2 O 7 при 450 °С, 2 n. H 4 P 2 O 7 + 2 n. H 2 O = 4 n. H 3 PO 4 ниже 230 °С. Суммарное уравнение: Р 4 О 10 + 6 H 2 O = 4 H 3 PO 4. Также ортофосфорную кислоту получают при переработке апатитов: Ca 5 (PO 4 ) 3 F + 5 H 2 SO 4 + 10 H 2 O = 5 Ca. SO 4 · 2 H 2 O + 3 H 3 PO 4 + HF.
Термический способ получения фосфорной кислоты основан на окислении элементарного фосфора в избытке воздуха с последующей гидратацией и образующегося оксида фосфора (V) и конденсацией фосфорной кислоты: 4 Р + 5 О 2 = Р 4 О 10 ; n. Р 4 О 10 + 2 n. H 2 O = 4(HPO 3 ) n при 700 °С, 4(HPO 3 ) n + 2 n. H 2 O = 2 n. H 4 P 2 O 7 при 450 °С, 2 n. H 4 P 2 O 7 + 2 n. H 2 O = 4 n. H 3 PO 4 ниже 230 °С. Суммарное уравнение: Р 4 О 10 + 6 H 2 O = 4 H 3 PO 4. Также ортофосфорную кислоту получают при переработке апатитов: Ca 5 (PO 4 ) 3 F + 5 H 2 SO 4 + 10 H 2 O = 5 Ca. SO 4 · 2 H 2 O + 3 H 3 PO 4 + HF.


