Формирование химического состава подземных вод C троение











formirovanie_himicheskogo_sostava_podzemnyh_vod.ppt
- Размер: 758.0 Кб
- Автор:
- Количество слайдов: 14
Описание презентации Формирование химического состава подземных вод C троение по слайдам
 Формирование химического состава подземных вод
Формирование химического состава подземных вод
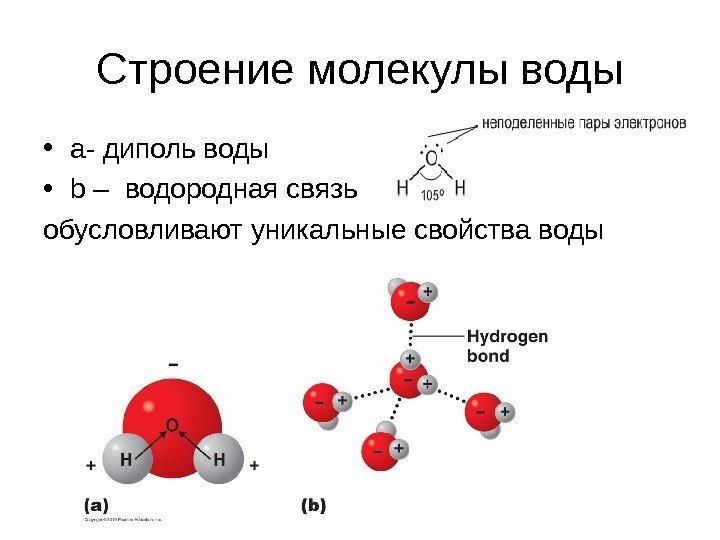
 C троение молекулы воды • а- диполь воды • b – водородная связь обусловливают уникальные свойства воды
C троение молекулы воды • а- диполь воды • b – водородная связь обусловливают уникальные свойства воды
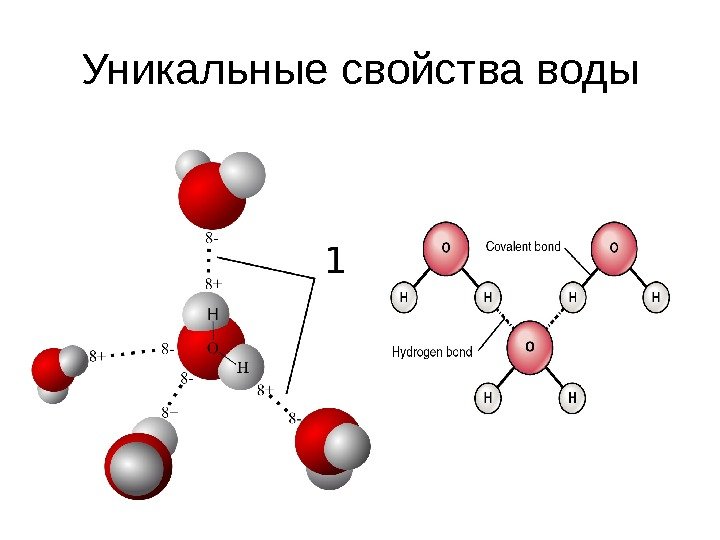
 Уникальные свойства воды
Уникальные свойства воды
 Водородная связь • Две поделенные электронные пары участвуют в образовании двух полярных ковалентных связей, а оставшиеся две неподеленные пары электронов тоже играют важную роль в свойствах воды. • Все заместители у атома кислорода, включая неподеленные пары, стремятся расположиться как можно дальше друг от друга. Это приводит к тому, что молекула приобретает форму искаженного тетраэдра с атомом кислорода в центре. • В четырех вершинах этого «тетраэдра» находятся два атома водорода и две неподеленные пары электронов. • Но если смотреть только по центрам атомов, то получается, что молекула воды имеет угловое строение, причем угол Н–О–Н составляет примерно 105 градусов.
Водородная связь • Две поделенные электронные пары участвуют в образовании двух полярных ковалентных связей, а оставшиеся две неподеленные пары электронов тоже играют важную роль в свойствах воды. • Все заместители у атома кислорода, включая неподеленные пары, стремятся расположиться как можно дальше друг от друга. Это приводит к тому, что молекула приобретает форму искаженного тетраэдра с атомом кислорода в центре. • В четырех вершинах этого «тетраэдра» находятся два атома водорода и две неподеленные пары электронов. • Но если смотреть только по центрам атомов, то получается, что молекула воды имеет угловое строение, причем угол Н–О–Н составляет примерно 105 градусов.
 Водородная связь • Энергия водородной связи Н—О воды (H 2 O)2 составляет 21, 5 к. Дж/моль, а ее длина 2, 04 А. Таким образом, эти связи более длинные и примерно в 10 -20 раз менее прочные, чем обычные ковалентные, но именно они заставляют воду быть жидкостью или льдом (а не газом) в обычных условиях. Водородные связи разрушаются только тогда, когда жидкая вода переходит в пар. • В жидкой воде молекулы связаны между собой лишь в отдельные агрегаты из нескольких молекул. Эти агрегаты могут свободно двигаться рядом друг с другом, образуя подвижную жидкость. Но при понижении температуры упорядоченность становится все больше и больше, а агрегаты – все крупнее. Наконец, образуется лед. • В кристалле льда между молекулами остаются пустоты. Объем пустот чуть больше, чем размер отдельной молекулы Н 2 О. Поэтому лед имеет меньшую плотность, чем жидкая вода и плавает на поверхности. Большинство же других веществ при замерзании увеличивает свою плотность.
Водородная связь • Энергия водородной связи Н—О воды (H 2 O)2 составляет 21, 5 к. Дж/моль, а ее длина 2, 04 А. Таким образом, эти связи более длинные и примерно в 10 -20 раз менее прочные, чем обычные ковалентные, но именно они заставляют воду быть жидкостью или льдом (а не газом) в обычных условиях. Водородные связи разрушаются только тогда, когда жидкая вода переходит в пар. • В жидкой воде молекулы связаны между собой лишь в отдельные агрегаты из нескольких молекул. Эти агрегаты могут свободно двигаться рядом друг с другом, образуя подвижную жидкость. Но при понижении температуры упорядоченность становится все больше и больше, а агрегаты – все крупнее. Наконец, образуется лед. • В кристалле льда между молекулами остаются пустоты. Объем пустот чуть больше, чем размер отдельной молекулы Н 2 О. Поэтому лед имеет меньшую плотность, чем жидкая вода и плавает на поверхности. Большинство же других веществ при замерзании увеличивает свою плотность.
 Возникновение водородных связей • Для возникновения водородных связей важно, чтобы в молекулах вещества были атомы водорода, связанные с небольшими, но электроотрицательными атомами, например: O, N, F. • Это создает заметный частичный положительный заряд на атомах водорода. С другой стороны, важно, чтобы у электроотрицательных атомов были неподеленные электронные пары. Когда обедненный электронами атом водорода одной молекулы (акцептор) взаимодействует с неподеленной электронной парой на атоме N, O или F другой молекулы (донор), то возникает связь, похожая на полярную ковалентную.
Возникновение водородных связей • Для возникновения водородных связей важно, чтобы в молекулах вещества были атомы водорода, связанные с небольшими, но электроотрицательными атомами, например: O, N, F. • Это создает заметный частичный положительный заряд на атомах водорода. С другой стороны, важно, чтобы у электроотрицательных атомов были неподеленные электронные пары. Когда обедненный электронами атом водорода одной молекулы (акцептор) взаимодействует с неподеленной электронной парой на атоме N, O или F другой молекулы (донор), то возникает связь, похожая на полярную ковалентную.
 Факторы формирования — это естественные или искусственные причины, определяющие возникновение и протекание гидрогеохимических процессов в земной коре. Физико-химические факторы : свойства воды и водных растворов, химических элементов и их соединений; Физические : температура, давление, гравитация, радиоактивность; Физико-географичекие : климат (осадки и испарение, температура), рельеф, поверхностные воды, почвенно-растительный покров; Геолого-гидрогеологические : тектоника, магматизм и метаморфизм, состав пород, фильтрационные свойства пород; Микробиологические : микрофлора и микрофауна; Антропогенные (техногенные): промышленные и с/х предприятия, коммунально-бытовые отходы и др.
Факторы формирования — это естественные или искусственные причины, определяющие возникновение и протекание гидрогеохимических процессов в земной коре. Физико-химические факторы : свойства воды и водных растворов, химических элементов и их соединений; Физические : температура, давление, гравитация, радиоактивность; Физико-географичекие : климат (осадки и испарение, температура), рельеф, поверхностные воды, почвенно-растительный покров; Геолого-гидрогеологические : тектоника, магматизм и метаморфизм, состав пород, фильтрационные свойства пород; Микробиологические : микрофлора и микрофауна; Антропогенные (техногенные): промышленные и с/х предприятия, коммунально-бытовые отходы и др.
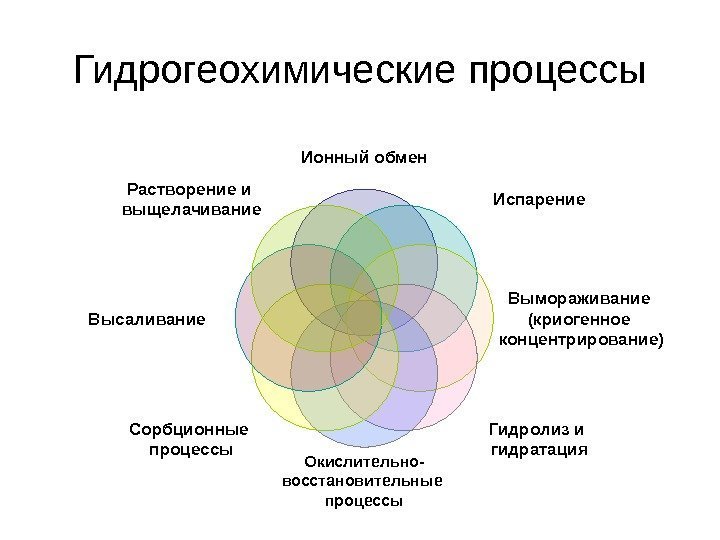
 Гидрогеохимические процессы Ионный обмен Испарение Вымораживание (криогенное концентрирование) Гидролиз и гидратация Окислительно- восстановительные процессы. Сорбционные процессы. Высаливание Растворение и выщелачивание
Гидрогеохимические процессы Ионный обмен Испарение Вымораживание (криогенное концентрирование) Гидролиз и гидратация Окислительно- восстановительные процессы. Сорбционные процессы. Высаливание Растворение и выщелачивание
 Окислительно-восстановительные процессы ОКИСЛЕНИЕ – переход элементов с низкой валентностью в высоковалентные Fe. S 2 + n. H 2 O + m. O 2 Fe. SO 4 Fe 2 (SO 4) 3 Fe(OH) 3 + H 2 SO 4 ВОССТАНОВЛЕНИЕ – элементы с высокой валентностью переходят в соединения с более низкой валентностью Me. SO 4 + 2 C = Me. S + 2 CO 3 Na 2 SO 4 + 2 C + H 2 O = Na 2 CO 3 + H 2 S + CO 2 переходит в р-р, повышает щелочность подземных вод Ca. SO 4 + 2 C + H 2 O = Ca. CO 3 + H 2 S + CO 2 кальцит не растворим, ухудшает проницаемость пород
Окислительно-восстановительные процессы ОКИСЛЕНИЕ – переход элементов с низкой валентностью в высоковалентные Fe. S 2 + n. H 2 O + m. O 2 Fe. SO 4 Fe 2 (SO 4) 3 Fe(OH) 3 + H 2 SO 4 ВОССТАНОВЛЕНИЕ – элементы с высокой валентностью переходят в соединения с более низкой валентностью Me. SO 4 + 2 C = Me. S + 2 CO 3 Na 2 SO 4 + 2 C + H 2 O = Na 2 CO 3 + H 2 S + CO 2 переходит в р-р, повышает щелочность подземных вод Ca. SO 4 + 2 C + H 2 O = Ca. CO 3 + H 2 S + CO 2 кальцит не растворим, ухудшает проницаемость пород
 Гидратация ГИДРАТАЦИЯ – химическое присоединение воды к минералам горных пород с образованием новых минералов (гидроокислов и гидросиликатов) Fe 2 O 3 + n H 2 O Fe 2 O 3 ×n. H 2 O гематит лимонит C а SO 4 + 2 H 2 O Ca. SO 4 × 2 H 2 O ангидрит гипс
Гидратация ГИДРАТАЦИЯ – химическое присоединение воды к минералам горных пород с образованием новых минералов (гидроокислов и гидросиликатов) Fe 2 O 3 + n H 2 O Fe 2 O 3 ×n. H 2 O гематит лимонит C а SO 4 + 2 H 2 O Ca. SO 4 × 2 H 2 O ангидрит гипс
 Гидролиз ГИДРОЛИЗ алюмосиликатов – обменное разложение вещества под влиянием гидролитической диссоциации воды, сопровождающееся разрушением одних и образованием других минералов K[Al. Si 3 O 8 ] + n H 2 O + CO 2 K 2 CO 3 + Al 4 [Si 4 O 10 ](OH) 8 + в р-р каолинит Si. O 2 ×n. H 2 O опал Дальнейший гидролиз каолинита приводит к его полному разложению и образованию латерита Al 4 [Si 4 O 10 ](OH) 8 H 2 Al 2 O 4 + Si. O 2 + n. H 2 O каолинит латерит
Гидролиз ГИДРОЛИЗ алюмосиликатов – обменное разложение вещества под влиянием гидролитической диссоциации воды, сопровождающееся разрушением одних и образованием других минералов K[Al. Si 3 O 8 ] + n H 2 O + CO 2 K 2 CO 3 + Al 4 [Si 4 O 10 ](OH) 8 + в р-р каолинит Si. O 2 ×n. H 2 O опал Дальнейший гидролиз каолинита приводит к его полному разложению и образованию латерита Al 4 [Si 4 O 10 ](OH) 8 H 2 Al 2 O 4 + Si. O 2 + n. H 2 O каолинит латерит
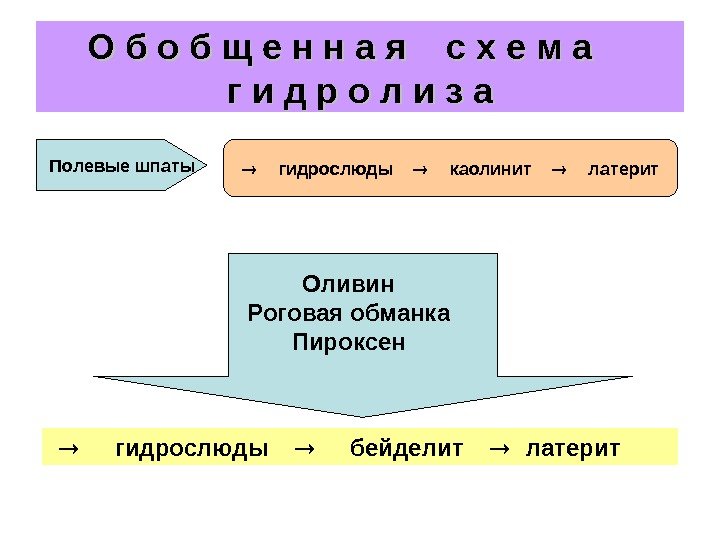
 О б о б щ е н н а я с х е м а г и д р о л и з а Оливин Роговая обманка Пироксен гидрослюды бейделит латерит. Полевые шпаты гидрослюды каолинит латерит
О б о б щ е н н а я с х е м а г и д р о л и з а Оливин Роговая обманка Пироксен гидрослюды бейделит латерит. Полевые шпаты гидрослюды каолинит латерит
 Гидрогеохимические процессы
Гидрогеохимические процессы
 Гидробиохимические процессы Сульфофикация (аэробные условия) Сульфатредукция (анаэробные условия)
Гидробиохимические процессы Сульфофикация (аэробные условия) Сульфатредукция (анаэробные условия)

