F-фтор, Cl-хлор, Br-бром, I-йод, At-астат Фтор F


F-фтор, Cl-хлор, Br-бром, I-йод, At-астат

Фтор F 2 - открыт А. Муассан в 1866 г. Хлор Cl 2 - открыт К. Шееле в 1774 г Бром Br 2 - открыт Ж. Баларом в 1826 г. Йод I 2 - открыт Б. Куртуа в 1811 г. А. Бала р А. Балар А. Муассан Прибор А. Муассана для получения К. Шееле фтора. Платиновый электролизёр помещён в стеклянный сосуд с жидким метилхлоридом tкип=-24, 2 °С). Выделяющийся на аноде фтор собирают в пробирку. Б. Куртуа
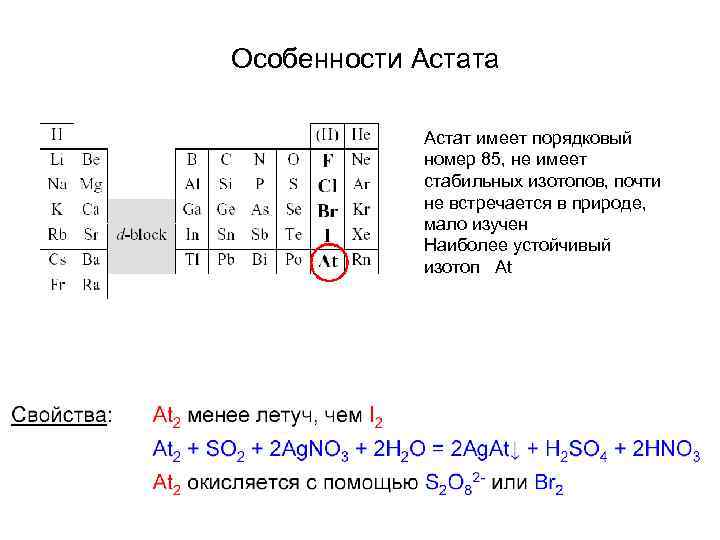
Особенности Астата Астат имеет порядковый номер 85, не имеет стабильных изотопов, почти не встречается в природе, мало изучен Наиболее устойчивый изотоп At

Ca 5 F(PO 4)3 -фторапатит Ca. F 2 -плавиковый шпат Na 3 Al. F 6 -криолит

Лабораторный метод: 2 K 2 Mn. F 6+4 Sb. F 5=4 KSb. F 6+2 Mn. F 3+F 2 Промышленный метод: Электролиз расплава кислого фторида калия KF· 3 HF

1) Si. O 2+2 F 2=Si. F 4+O 2 2) 2 F 2+Na 2 SO 4=2 Na. F+SO 2 F 2+O 2 3) 2 H 2 O+2 F 2=4 HF+O 2 4) S+3 F 2=SF 6 5) 2 P+5 F 2=2 PF 5 6) Xe+2 F 2=Xe. F 4 7) 2 Na+F 2=2 Na. F

Получение: 1) Ca. F 2+H 2 SO 4=Ca. SO 4+2 HF 2) H 2+F 2=2 HF 3) Химические свойства: 4) 1)Mg. O+2 HF=Mg. F 2+H 2 O 5) 2) HF+Na. OH=Na. F+H 2 O 6) 3) HF+Na 2 O 2=2 Na. F+H 2 O 2
Хлор
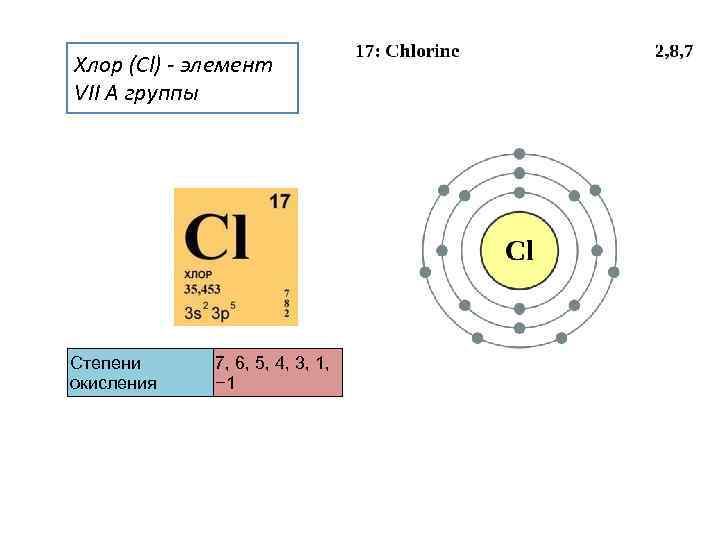
Хлор (Cl) - элемент VII A группы Степени 7, 6, 5, 4, 3, 1, окисления − 1

История открытия Впервые хлор был получен в 1774 г. Карлом Вильгельмом Шееле: 4 HCl + Mn. O 2 = Cl 2 + Mn. Cl 2 2 H 2 O • Однако Шееле предположил, что хлор представляет собой оксид соляной кислоты. • И только Дэви удалось электролизом разложить поваренную соль на натрий и хлор. Этот газ Гэмфри Дэви, английский химик, в 1810 году назвал хлорином. По древнегречески «хлорос» - желто-зеленый Современное название этому газу «хлор» дал в 1812 году французский химик Гей-Люссак
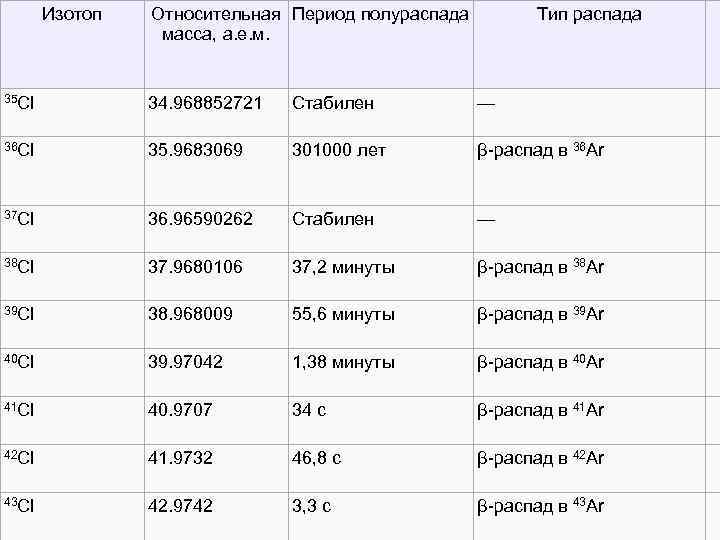
Изотоп Относительная Период полураспада Тип распада масса, а. е. м. 35 Cl 34. 968852721 Стабилен — 36 Cl 35. 9683069 301000 лет β-распад в 36 Ar 37 Cl 36. 96590262 Стабилен — 38 Cl 37. 9680106 37, 2 минуты β-распад в 38 Ar 39 Cl 38. 968009 55, 6 минуты β-распад в 39 Ar 40 Cl 39. 97042 1, 38 минуты β-распад в 40 Ar 41 Cl 40. 9707 34 c β-распад в 41 Ar 42 Cl 41. 9732 46, 8 c β-распад в 42 Ar 43 Cl 42. 9742 3, 3 c β-распад в 43 Ar
Распространение в природе В природе он встречается только в Хлор – активный виде соединений в составе элемент минералов: галита Na. CI, сильвина KCl, сильвинита KCl · Na. Cl, Самые большие бишофита Mg. Cl 2 · 6 H 2 O, запасы хлора карналлита KCl · Mg. Cl 2 · 6 Н 2 O, содержатся в каинита KCl · Mg. SO 4 · 3 Н 2 О. составе солей вод морей и океанов. В организме человека и животных хлор содержится в основном в межклеточных В природе жидкостях (в том числе в крови) и играет встречаются 2 важную роль в регуляции осмотических стабильных изотопа процессов, а также в процессах, хлора: с массовым связанных с работой нервных клеток. числом 35 и 37.

Содержание элемента хлора в земной коре составляет 1, 7*10 -2 по массе. В природе хлор содержится в виде минералов: галита (каменной соли) Na. Cl, сильвинита KCl *Na. Cl, бишофита Mg. Cl 2 * 2 H 2 O карналлита KCl*Ng. Cl 2*6 H 2 O , каинита KCl*Mg. SO 4 *3 H 2 O
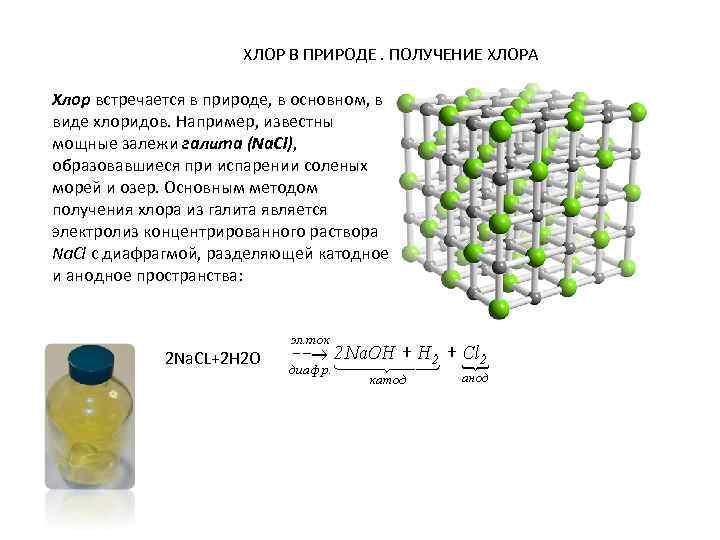
ХЛОР В ПРИРОДЕ. ПОЛУЧЕНИЕ ХЛОРА Хлор встречается в природе, в основном, в виде хлоридов. Например, известны мощные залежи галита (Na. Cl), образовавшиеся при испарении соленых морей и озер. Основным методом получения хлора из галита является электролиз концентрированного раствора Na. Cl с диафрагмой, разделяющей катодное и анодное пространства: 2 Na. CL+2 H 2 O

Физические свойства При н. у. хлор - Растворитель Растворимость ядовитый газ желтовато- г/100 г зелёного цвета, с резким, удушающим запахом. Бензол Растворим Вода (0 °C) 1, 48 Вода (80 °C) 0, 22 Хлороформ Хорошо растворим По электропроводности жидкий хлор занимает одно из первых мест среди самых сильных изоляторов: он проводит ток почти в миллиард раз хуже, чем дистиллированная вода. Скорость звука в хлоре примерно в полтора раза меньше, чем в воздухе.
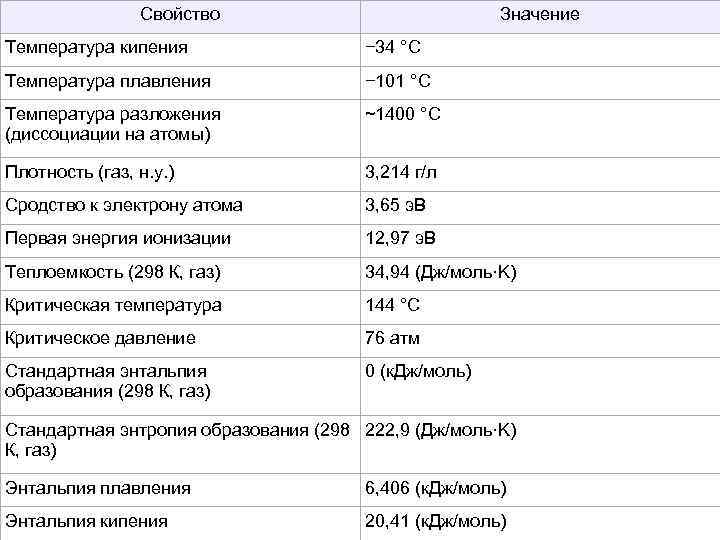
Свойство Значение Температура кипения − 34 °C Температура плавления − 101 °C Температура разложения ~1400 °C (диссоциации на атомы) Плотность (газ, н. у. ) 3, 214 г/л Сродство к электрону атома 3, 65 э. В Первая энергия ионизации 12, 97 э. В Теплоемкость (298 К, газ) 34, 94 (Дж/моль·K) Критическая температура 144 °C Критическое давление 76 атм Стандартная энтальпия 0 (к. Дж/моль) образования (298 К, газ) Стандартная энтропия образования (298 222, 9 (Дж/моль·K) К, газ) Энтальпия плавления 6, 406 (к. Дж/моль) Энтальпия кипения 20, 41 (к. Дж/моль)
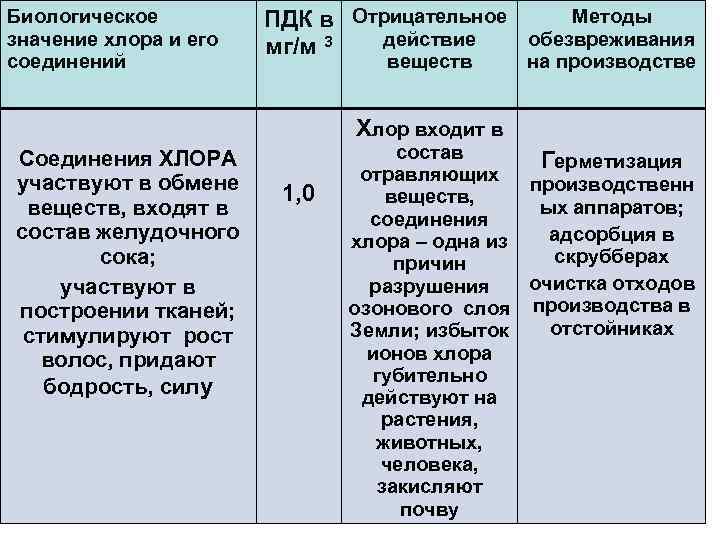
Биологическое ПДК в Отрицательное Методы значение хлора и его мг/м 3 действие обезвреживания соединений веществ на производстве Хлор входит в Соединения ХЛОРА состав Герметизация участвуют в обмене отравляющих 1, 0 производственн веществ, входят в соединения ых аппаратов; состав желудочного хлора – одна из адсорбция в сока; причин скрубберах участвуют в разрушения очистка отходов построении тканей; озонового слоя производства в стимулируют рост Земли; избыток отстойниках волос, придают ионов хлора губительно бодрость, силу действуют на растения, животных, человека, закисляют почву

Химические свойства 1)ВЗАИМОДЕЙСТВИЕ С Ме 2 Na+Cl 2=2 Na. CL 2 AL+3 CL 2=2 ALCL 3 Cu+CL 2=Cu. CL 2 2) ВЗАИМОДЕЙСТВИЕ С НЕМе H 2+Cl 2=2 HCL 2 S+CL 2=S 2 CL 2 3)ВЗАИМОДЕЙСТВИЕ С ВОДОЙ СL 2+H 2 O=HCL+HCLO Производство взрывчатой желтой маслянистой жидкости 4 NН 3 + ЗСl 2 = NСl 3 + ЗNН 4 Сl

1)2 Hg. O +2 Cl 2= Hg. O*Hg. Cl 2 +Cl 2 O 2)3 KCl. O 3 +3 h 2 so 4=3 KHSO 4+2 CLO 2+HCLO 4+H 2 O 3)2 Na. CLO 3+ SO 2+H 2 SO 4=2 CLO 2 +2 Na. HSO 4 4)2 KCLO 3+H 3 C 2 O 4+H 2 SO 4=2 CLO 2+2 Na. HSO 4 CL 2+H 2 O=2 HCl. O
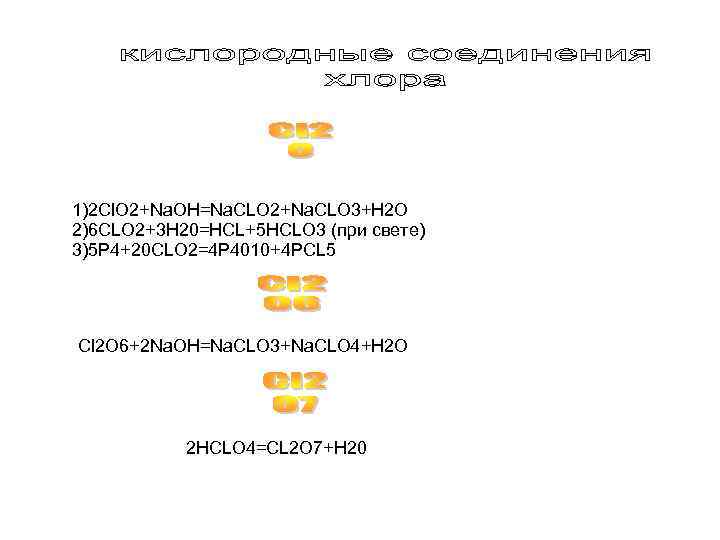
1)2 Cl. O 2+Na. OH=Na. CLO 2+Na. CLO 3+H 2 O 2)6 CLO 2+3 H 20=HCL+5 HCLO 3 (при свете) 3)5 P 4+20 CLO 2=4 P 4010+4 PCL 5 Cl 2 O 6+2 Na. OH=Na. CLO 3+Na. CLO 4+H 2 O 2 HCLO 4=CL 2 O 7+H 20

2 Ag. CLO 4+I 2=CL 2 O 8+2 Ag. I 2 HOCL=2 HCL+O 2 2 HOCL=CL 2 O+H 2 O 3 HOCL=HCLO 3+2 HCL

НЕКОТОРЫЕ Р-ЦИИ С ГИПОХЛОРИТОМ Ca И ГИПОГАЛОГЕНИТАМИ 1) 2 Ca. OCl 2=2 Ca. Cl 2 2) 3 Na. OCL=Na. Cl. O 3+2 Na. CL 3) Na. OCL+3 NH 3=N 2 H 4+Na. CL+H 2 O 4) Ca. OCL 2+2 HCL(k)=CL 2+Ca. CL 2+H 2 O 5) Ca. OCL+Pb(CH 3 COO)2+H 2 O=Pb. O 4+Ca. Cl 2 Ba. O 2+2 Cl. O 2=Ba(Cl. O 2)2+O 2 Ba(Cl. O 2)2+H 2 SO 4=Ba. SO 4+2 HCLO 2

2 Na. Cl. O 3+H 2 SO 4=2 HCLO 3 3 CL 2+6 KOH(гор)=5 KCL+KCLO 3+3 H 2 O 3 Na. Cl. O=Na. Cl. O 3+2 Na. Cl Примеры реа-ции с участием хлоратов 2 KCl. O 3=2 KCl+3 O 2 4 KCl. O 3=KCl+KCl. O 4 KCl. O 3+3 Mg=KCl+3 Mg. O

Получение: CL 2 O 7+H 20=2 HCLO 4 РАЗЛОЖЕНИЕ 4 HCLO 4=2 Сl 2+2 H 20+7 O 2

Бром
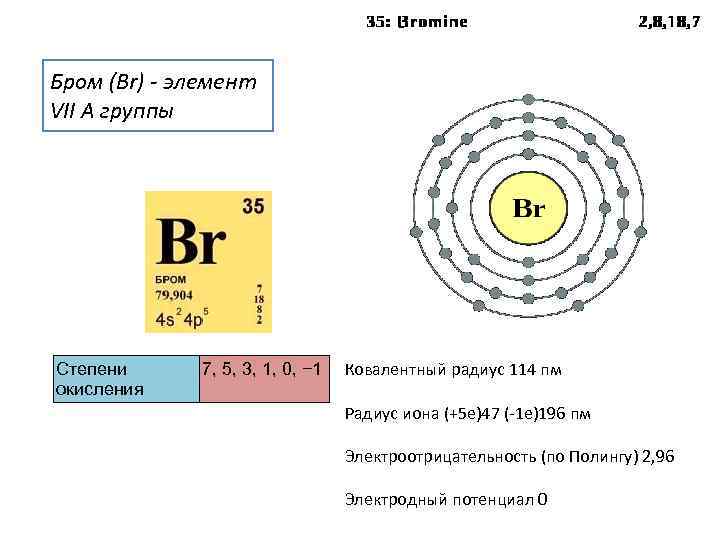
Бром (Br) - элемент VII A группы Степени 7, 5, 3, 1, 0, − 1 Ковалентный радиус 114 пм окисления Радиус иона (+5 e)47 (-1 e)196 пм Электроотрицательность (по Полингу) 2, 96 Электродный потенциал 0

2 Br-+Pb. O 2+4 H+=Br 2+Pb 2++2 H 2 O

История открытия Бром был открыт в 1826 году молодым преподавателем колледжа города Монпелье А. Ж. Баларом.
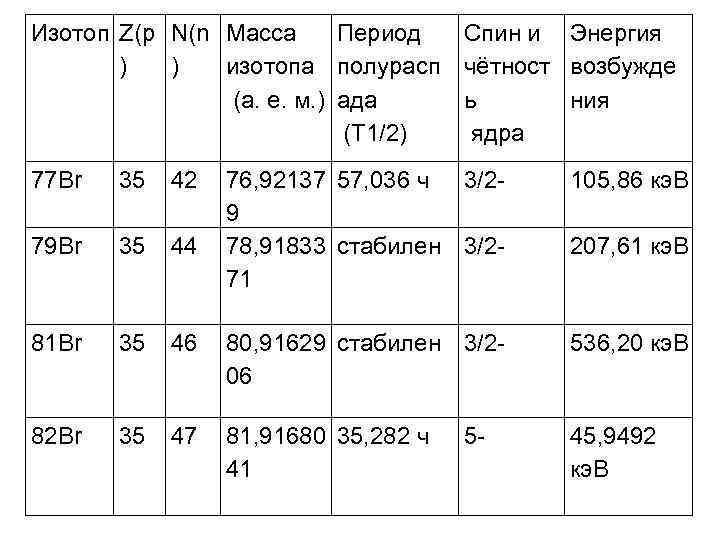
Изотоп Z(p N(n Масса Период Спин и Энергия ) ) изотопа полурасп чётност возбужде (а. е. м. ) ада ь ния (T 1/2) ядра 77 Br 35 42 76, 92137 57, 036 ч 3/2 - 105, 86 кэ. В 9 79 Br 35 44 78, 91833 стабилен 3/2 - 207, 61 кэ. В 71 81 Br 35 46 80, 91629 стабилен 3/2 - 536, 20 кэ. В 06 82 Br 35 47 81, 91680 35, 282 ч 5 - 45, 9492 41 кэ. В

Распространение в природе • Земная кора: Содержание брома в земной коре (1, 6· 10 -4% по массе) оценивается в 1015 -1016 т. • Атмосфера: около 4 млн т брома. • Организмы земных животных и рыб, у человека обнаружен в крови, почках, печени и мозге. • Входит в состав минералов.

Минералы Сильвин(KCl с Поваренная соль(Na. Cl с Карналлит(KCl·Mg. Cl 2· 6 H 2 O с примесями. КBr) примесями Na. Br) примесями солей брома)
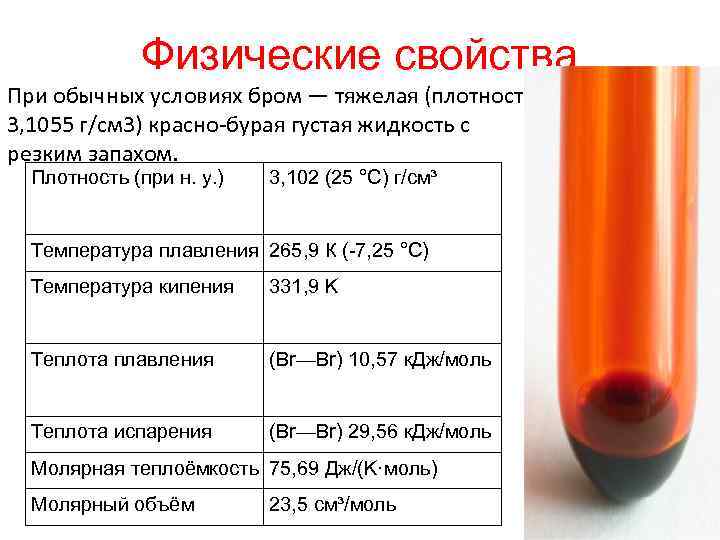
Физические свойства При обычных условиях бром — тяжелая (плотность 3, 1055 г/см 3) красно-бурая густая жидкость с резким запахом. Плотность (при н. у. ) 3, 102 (25 °C) г/см³ Температура плавления 265, 9 К (-7, 25 °C) Температура кипения 331, 9 K Теплота плавления (Br—Br) 10, 57 к. Дж/моль Теплота испарения (Br—Br) 29, 56 к. Дж/моль Молярная теплоёмкость 75, 69 Дж/(K·моль) Молярный объём 23, 5 см³/моль
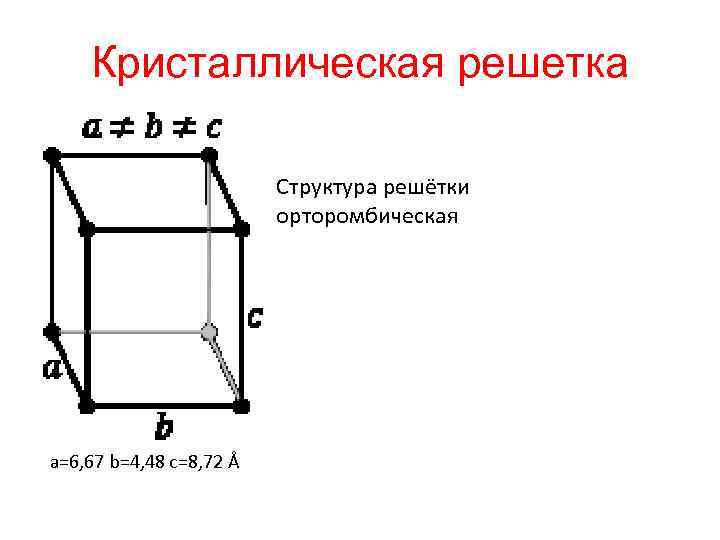
Кристаллическая решетка Структура решётки орторомбическая a=6, 67 b=4, 48 c=8, 72 Å

Химические свойства 1. Взаимодействие с водой: Br 2 + H 2 O = HBr + HBr. O 2. Взаимодействие с растворами иодидов: Br 2+ 2 KI = I 2+ 2 KBr 3. С органическими соединениями: C 2 H 4 + Br 2 = C 2 H 4 Br 2 4. С растворами карбонатов: Br 2 + 3 Na 2 CO 3 = 5 Na. Br + Na. Br. O 3+ 3 CO 2 5. С золотом: 2 Au+3 Br 2=2 Au. Br 3 6. С влажной пищевой содой: 6 Na. HCO 3+3 Br 2=5 Na. Br+Na. Br. O 3+^CO 2+3 H 2 O

Получение брома Бром получают химическим путём из рассола Br−:

Соединения брома Бромоводород HBr-представляет собой ядовитый (ПДК = 2 мг/м 3) бесцветный газ с резким запахом, дымящий на воздухе из-за взаимодействия с парами воды. При охлаждении до – 67° C бромоводород переходит в жидкое состояние.

Химические свойства HBr 1. В растворе HBr диссоциирует на ионы: HBr + H 2 O = H 3 O+ + Br– 2. Взаимодействие с концентрированной серной кислотой и кислородом воздуха: H 2 SO 4 + 2 HBr = Br 2 + SO 2+ 2 H 2 O 4 HBr + O 2 = 2 Br 2 + 2 H 2 O 3. Взаимодействие с гидроксидами Ме: HBr + KOH = KBr + H 2 O

Получение HBr 1. В промышленности: H 2 + Br 2 = 2 HBr(кат. : С, Pt) 2. В лаборатории: Na. Br + H 3 PO 4 = Na. H 2 PO 4 + HBr C 10 H 18 + Br 2 = C 10 H 17 Br + HBr

Применение бромоводорода Li 2 CO 3 + 2 HBr = 2 Li. Br + H 2 O + CO 2

Бромноватистая кислота HOBr 2 + 2 Hg. O + H 2 O = Hg. O·Hg. Br 2Ї + 2 HOBr При стоянии разлагается:

Бромистая кислота HO 2 Br Получение Реакция нитрата серебра и брома в водном растворе Образует соли — бромиты, например бромит бария Ba(Br. O 2)2 • H 2 O. Существует только в водных растворах, в течении 4 часов разлагается Ba(Br. O)2 + 2 Br 2 + 4 KOH = Ba(Br. O 2)2 + 4 KBr + 2 H 2 O

Бромноватая кислота HO 3 Br Получение 1. Окисление брома хлором в горячей воде: 2. Растворение брома растворе бромата серебра: 3. Гидролиз пентафторида брома: 4. Обменными реакциями:

Химические свойства 1. Разлагается при нагревании: 2. С щелочами образует соли броматы: 3. Является сильным окислителем:

Бромная кислота HO 4 Br Получение 1. Окисление бромноватой кислоты дифторидом ксенона: 2. Окислением броматов фтором с последующей обработкой кислотой:

Химические свойства 1. При нагревании, а при повышении концентрации даже при комнатной температуре, бромная кислота разлагается: 2. Бромная кислота является сильной одноосновной кислотой: 3. Бромная кислота — сильный (но медленный) окислитель:

Применение брома и его соединений

Биологическая роль и токсичность

Йод
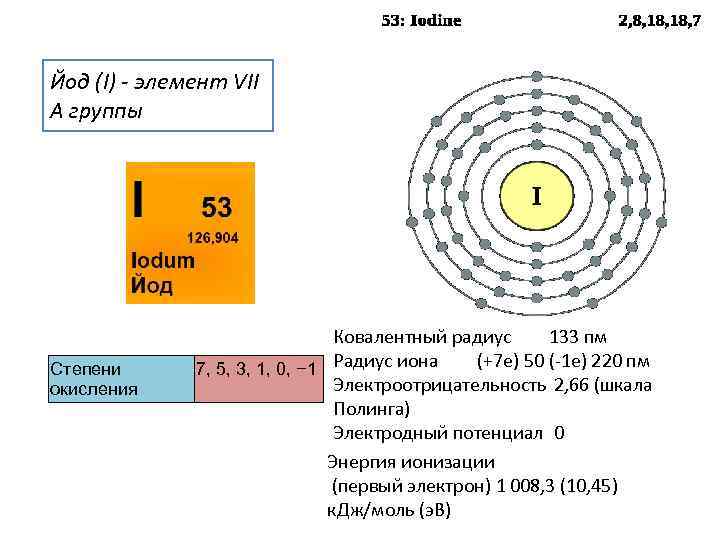
Йод (I) - элемент VII A группы Ковалентный радиус 133 пм Степени 7, 5, 3, 1, 0, − 1 Радиус иона (+7 e) 50 (-1 e) 220 пм окисления Электроотрицательность 2, 66 (шкала Полинга) Электродный потенциал 0 Энергия ионизации (первый электрон) 1 008, 3 (10, 45) к. Дж/моль (э. В)

История создания Иод был открыт в 1811 г. Куртуа С 1815 г. Гей-Люссак стал рассматривать его как химический элемент
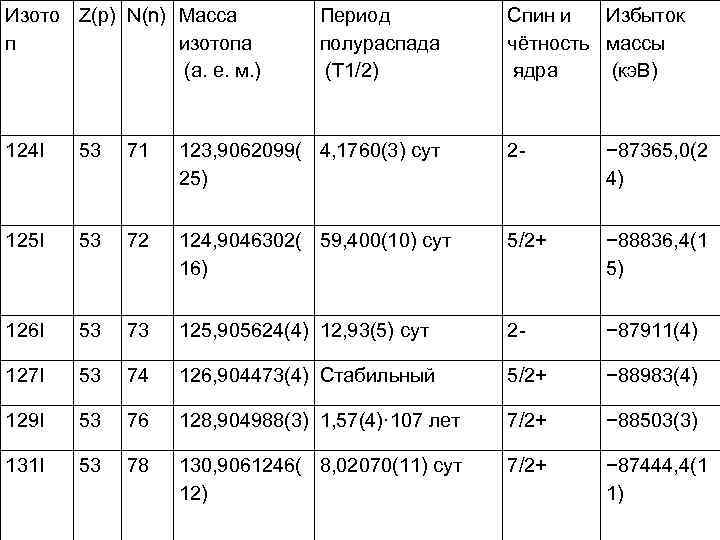
Изото Z(p) N(n) Масса Период Спин и Избыток п изотопа полураспада чётность массы (а. е. м. ) (T 1/2) ядра (кэ. В) 124 I 53 71 123, 9062099( 4, 1760(3) сут 2 - − 87365, 0(2 25) 4) 125 I 53 72 124, 9046302( 59, 400(10) сут 5/2+ − 88836, 4(1 16) 5) 126 I 53 73 125, 905624(4) 12, 93(5) сут 2 - − 87911(4) 127 I 53 74 126, 904473(4) Стабильный 5/2+ − 88983(4) 129 I 53 76 128, 904988(3) 1, 57(4)· 107 лет 7/2+ − 88503(3) 131 I 53 78 130, 9061246( 8, 02070(11) сут 7/2+ − 87444, 4(1 12) 1)

Распространение в природе -Его кларк всего 400 мг/т -Находится в виде иодидов в морской воде (20 — 30 мг на тонну морской воды) -Присутствует в живых организмах, больше всего в водорослях (5 кг на тонну высушенной морской капусты (ламинарии)) -Запасы природных иодидов оцениваются в 15 млн тонн, 99 % запасов находятся в Чили и Японии
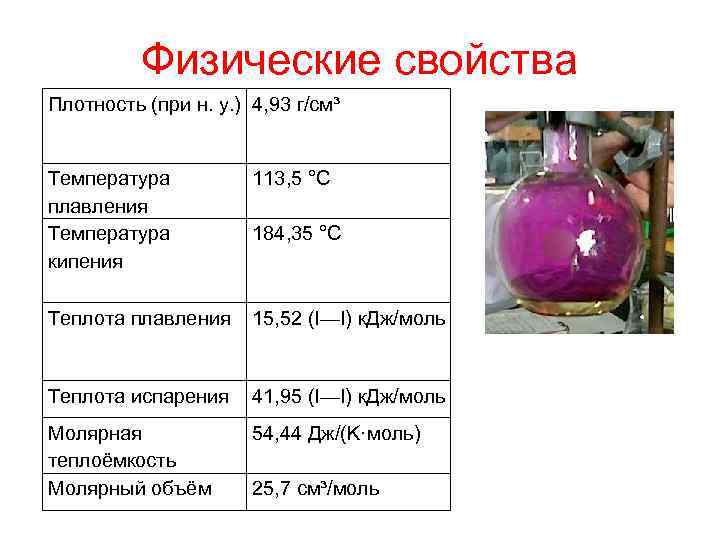
Физические свойства Плотность (при н. у. ) 4, 93 г/см³ Температура 113, 5 °C плавления Температура 184, 35 °C кипения Теплота плавления 15, 52 (I—I) к. Дж/моль Теплота испарения 41, 95 (I—I) к. Дж/моль Молярная 54, 44 Дж/(K·моль) теплоёмкость Молярный объём 25, 7 см³/моль
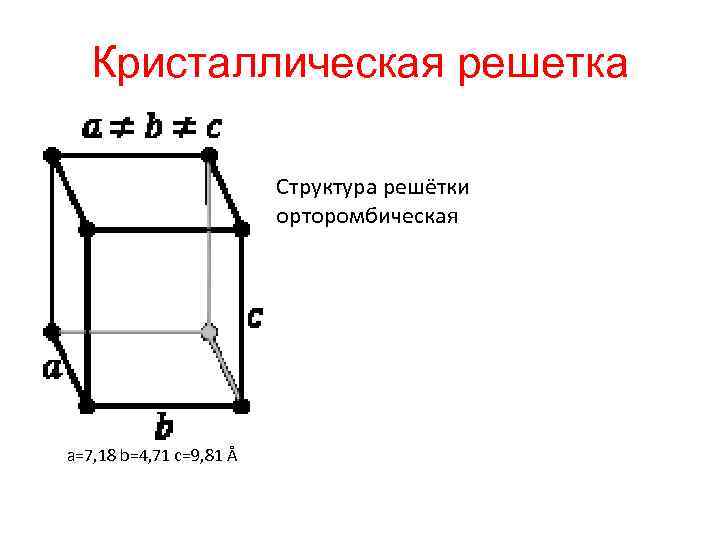
Кристаллическая решетка Структура решётки орторомбическая a=7, 18 b=4, 71 c=9, 81 Å

Химические свойства 1. Взаимодействие с Ме(t): 2. Взаимодействие с водородом (t): 3. С сероводородом: 4. С водой: p. Kc=15. 99 5. Реакция образования нитрида трииода:

Получение йода 2 Na. J + 2 Na. NO 2 + 2 H 2 SO 4 → 2 Na 2 SO 4 + 2 NO + J 2 + 2 H 2 O 2 НJ +Cl 2(хлорная вода) → 2 HCl + J 2 2 KJ +Br 2(хлорная вода) → 2 KBr+ J 2 8 НJ +H 2 SO 4(конц. ) → H 2 S↑+ 4 J 2+ 4 H 2 O 8 KJ +5 H 2 SO 4(конц. ) → H 2 S↑ + 4 J 2+ 4 K 2 SO 4 + 4 H 2 O

Соединения йода 1. Йодид водорода (HI). Бесцветный удушливый, легко разлагающийся газ. Обычно существует в виде едких водных растворов (йодистоводородная кислота), которые в концентрированном виде "дымят" на влажном воздухе. Применяется в органическом синтезе в качестве восстановителя или как среда для фиксирования йода. 2. Йодноватая кислота (HIO 3) и ее ангидрид (I 2 O 5) существуют в виде призматических кристаллов или в водных растворах. Используются в медицине или в качестве абсорбирующего агента в противогазах. 3. Перйодная кислота (HIO 4. 2 H 2 O). Обладает такими же свойствами, как йодноватая кислота.

Йодоводород Получение 1. В промышленности HI получают по реакции иода с гидразином: 2. В лаборатории HI можно получать с помощью окислительно- восстановительных реакций: и реакций обмена: 3. Иодоводород также получается при взаимодействии простых веществ. Эта реакция идет только при нагревании и протекает не до конца, так как в системе устанавливается равновесие:

Свойства 1. При стоянии водный раствор HI окрашивается в бурый цвет вследствие постепенного окисления его кислородом воздуха и выделения молекулярного иода: 2. HI способен восстанавливать концентрированную серную кислоту до сероводорода: 3. HI присоединяется к кратным связям (реакция электрофильного присоединения): 4. При гидролизе иодидов некоторых металлов низших степеней окисления выделяется водород:

5. Иодид калия присоединяет элементарный иод с образованием полииодидов: 6. Иодиды получают взаимодействием иода со щелочами в присутствии восстановителей, не образующих твердых побочных продуктов: муравьиная кислота, формальдегид, гидразин: 7. Ионы Cu 2+ при взаимодействии c иодидами легко дают малорастворимые соли одновалентной меди Cu. I:

Применение Иодоводород используют в лабораториях как восстановитель во многих органических синтезах, а также для приготовления различных иодсодержащих соединений. Спирты, галогениды и кислоты восстанавливаются HI, давая алканы

Йодноватая кислота Получение Получают в водных растворах при окислении иода хлором, перекисью водорода либо дымящей азотной кислотой: I 2 + 5 Cl 2 + 6 Н 2 О = 2 HIO 3 + 10 HCl I 2 + 5 H 2 O 2 = 2 HIO 3 + 4 H 2 O I 2 + 10 HNO 3 = 2 HIO 3 + 10 NO 2 + 4 H 2 O

Свойства 1. Иодноватая кислота хорошо растворима в воде, в концентрированных растворах проявляется ее склонность к полимеризации и устанавливается равновесие: n. HIO 3 → (HIO 3)n, n=2, 3 2. При нагревании HIO 3 до 230 °C образуется порошок иодноватого ангидрида, обладающего сильными окислительными свойствами, – I 2 O 5, который растворяется в воде, вновь образуя иодноватую кислоту: 2 HIO 3 → I 2 O 5 + H 2 O 3. Иодноватая кислота — сильная одноосновная кислота, обладает окислительными свойствами: E 0(HIO 3/I 2) = 1, 19 В. HIO 3 + 5 HI → 3 I 2 + 3 H 2 O

Применение йода и его соединений • В медицине • В криминалистике • В технике(источники света, аккумуляторы, лазерный термоядерный синтез, радиоэлектронная промышленность) • Динамика потребления йода
Биологическая роль и токсичность
Презентация галогены.ppt
- Количество слайдов: 65

