 Электролиз. Законы Фарадея. • Электролиз – совокупность процессов, протекающих при прохождении электрического тока через проводник второго рода (расплав или раствор электролита), или обратная работа гальванических элементов.
Электролиз. Законы Фарадея. • Электролиз – совокупность процессов, протекающих при прохождении электрического тока через проводник второго рода (расплав или раствор электролита), или обратная работа гальванических элементов.
 Некоторые варианты работы гальванического элемента Даниэля, Якоби:
Некоторые варианты работы гальванического элемента Даниэля, Якоби:
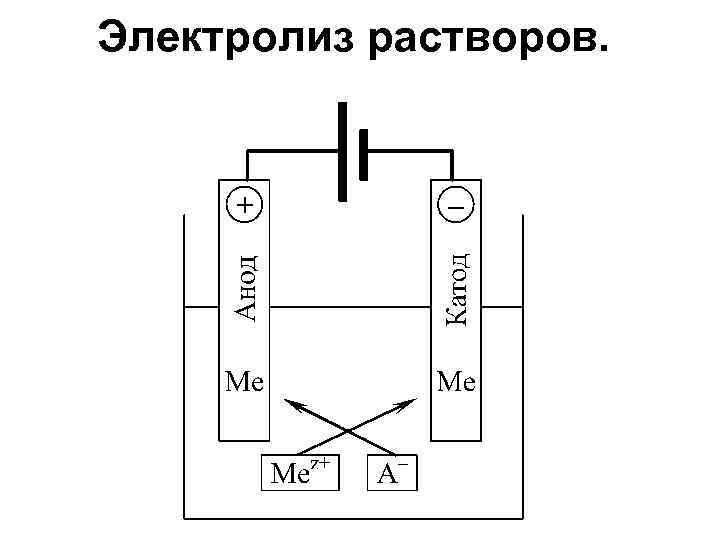 Электролиз растворов.
Электролиз растворов.
 Катодный процесс.
Катодный процесс.
 Существующая граница со значением – 0, 41 В
Существующая граница со значением – 0, 41 В
 Анодный процесс.
Анодный процесс.
 Электрохимический ряд напряжений.
Электрохимический ряд напряжений.
 Законы электролиза (М. Фарадей 1833). • Первый закон Фарадея. • Масса веществ, выделившихся на электродах при электролизе, прямо пропорциональна количеству электричества, прошедшего через раствор или расплав электролита. • Второй закон Фарадея. • При пропускании одинакового количества электричества через растворы или рас плавы различных электролитов масса веществ, выде ляющихся на электродах, пропорциональна их химическим эквивалентам. • Для выделения на электроде 1 химиче ского эквивалента вещества необходи мо пропустить через электрическую ячейку 96480 кулонов электричества.
Законы электролиза (М. Фарадей 1833). • Первый закон Фарадея. • Масса веществ, выделившихся на электродах при электролизе, прямо пропорциональна количеству электричества, прошедшего через раствор или расплав электролита. • Второй закон Фарадея. • При пропускании одинакового количества электричества через растворы или рас плавы различных электролитов масса веществ, выде ляющихся на электродах, пропорциональна их химическим эквивалентам. • Для выделения на электроде 1 химиче ского эквивалента вещества необходи мо пропустить через электрическую ячейку 96480 кулонов электричества.
 Масса вещества, выделившегося при электролизе: Обозначения: • Мэ(А) — молярная масса эквивалента вещества А, г/моль; • Q — количество электричества, прошедшего через электролит, Кл; • Q = I · t, I — сила тока, A; • t — время, с; • F = 96480 Кл/ моль постоянная Фарадея.
Масса вещества, выделившегося при электролизе: Обозначения: • Мэ(А) — молярная масса эквивалента вещества А, г/моль; • Q — количество электричества, прошедшего через электролит, Кл; • Q = I · t, I — сила тока, A; • t — время, с; • F = 96480 Кл/ моль постоянная Фарадея.
 Применение электролиза.
Применение электролиза.
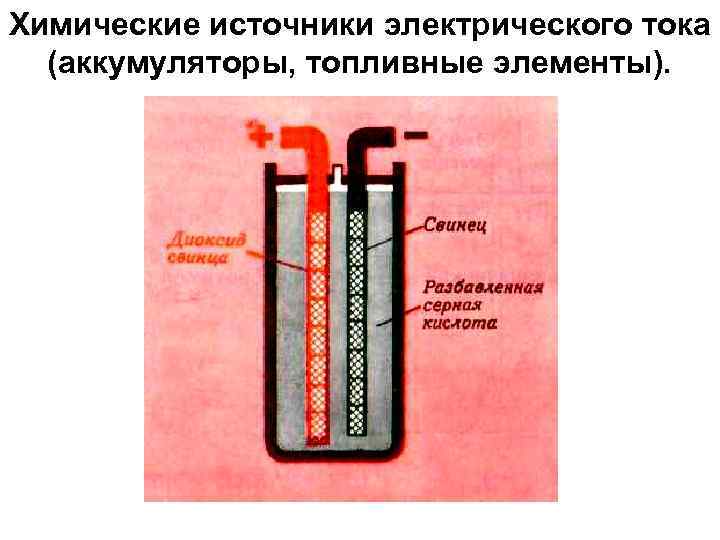 Химические источники электрического тока (аккумуляторы, топливные элементы).
Химические источники электрического тока (аккумуляторы, топливные элементы).
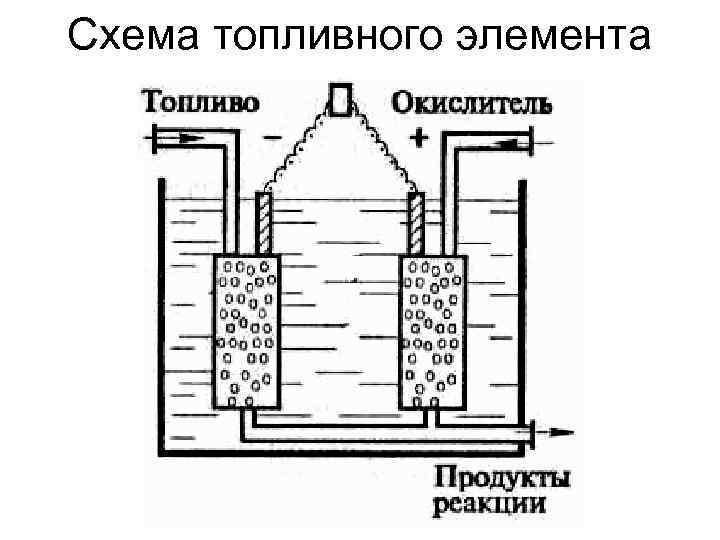 Схема топливного элемента
Схема топливного элемента