Эктодермальные производные Основные производные эктодермы Покровная эктодерма




tema---proizvodnye_ektodermy.ppt
- Размер: 56.2 Мб
- Автор:
- Количество слайдов: 44
Описание презентации Эктодермальные производные Основные производные эктодермы Покровная эктодерма по слайдам
 Эктодермальные производные
Эктодермальные производные
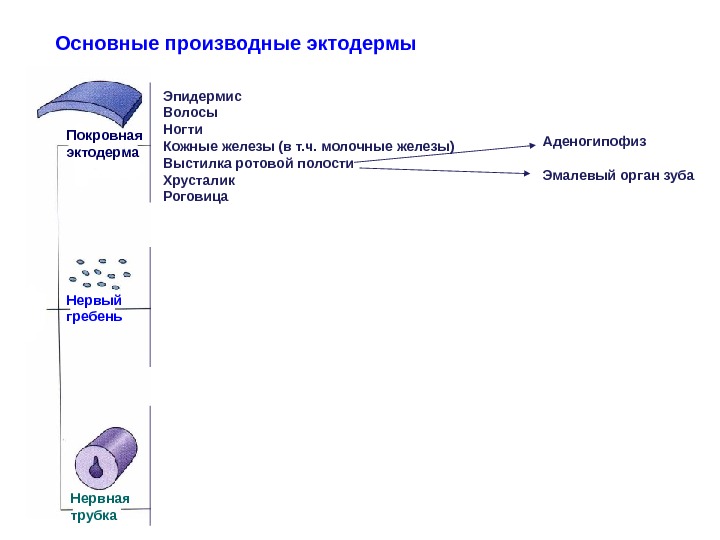
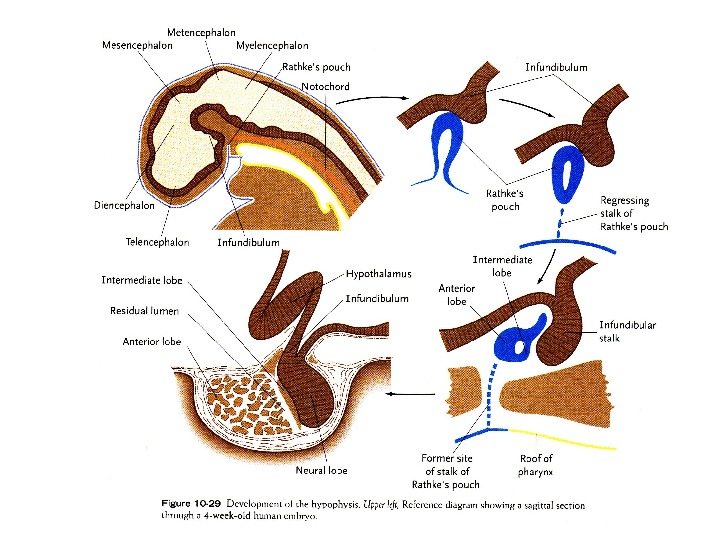
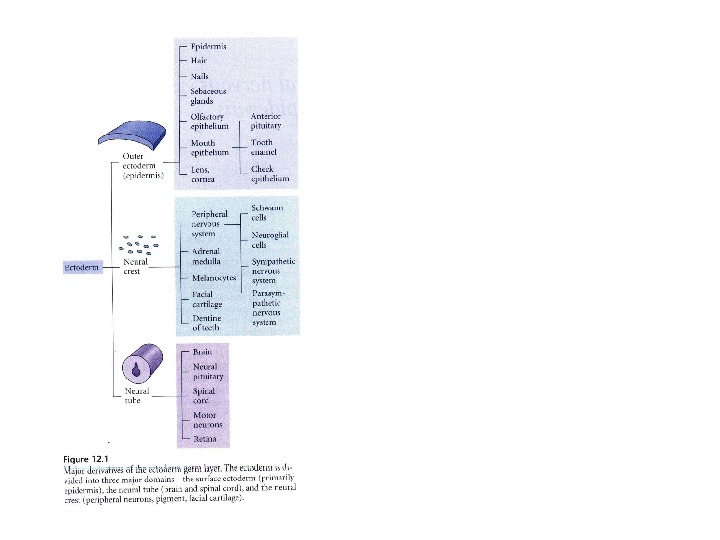
 Основные производные эктодермы Покровная эктодерма Нервый гребень Нервная трубка Эпидермис Волосы Ногти Кожные железы (в т. ч. молочные железы) Выстилка ротовой полости Хрусталик Роговица Аденогипофиз Эмалевый орган зуба
Основные производные эктодермы Покровная эктодерма Нервый гребень Нервная трубка Эпидермис Волосы Ногти Кожные железы (в т. ч. молочные железы) Выстилка ротовой полости Хрусталик Роговица Аденогипофиз Эмалевый орган зуба

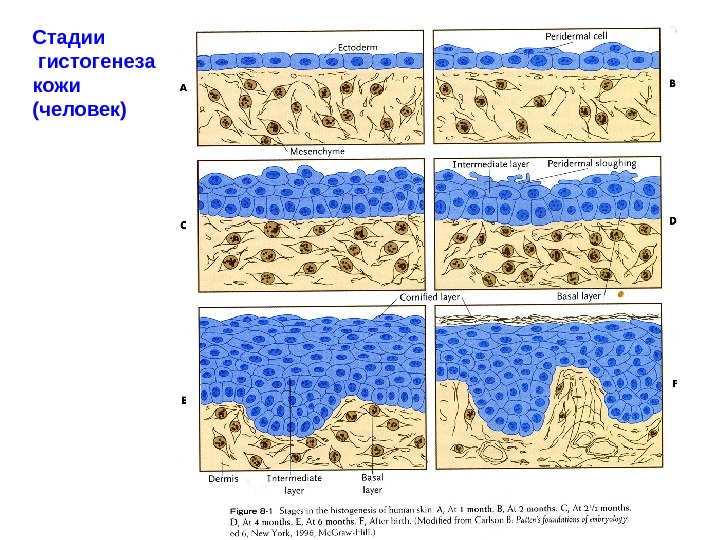
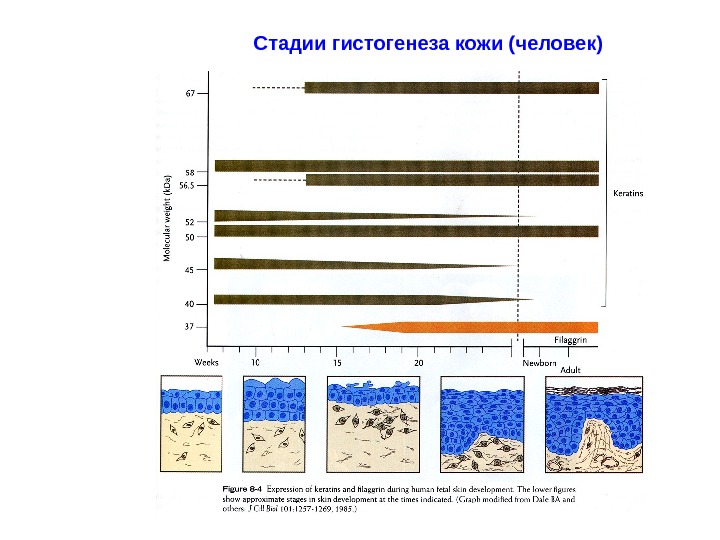
 Стадии гистогенеза кожи (человек)
Стадии гистогенеза кожи (человек)
 Стадии гистогенеза кожи (человек)
Стадии гистогенеза кожи (человек)
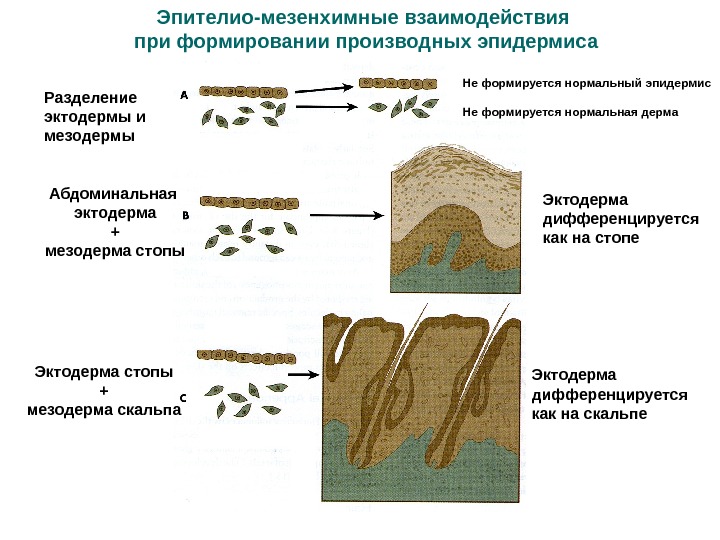
 Эпителио-мезенхимные взаимодействия при формировании производных эпидермиса Разделение эктодермы и мезодермы Не формируется нормальный эпидермис Не формируется нормальная дерма Абдоминальная эктодерма + мезодерма стопы Эктодерма дифференцируется как на стопе Эктодерма стопы + мезодерма скальпа Эктодерма дифференцируется как на скальпе
Эпителио-мезенхимные взаимодействия при формировании производных эпидермиса Разделение эктодермы и мезодермы Не формируется нормальный эпидермис Не формируется нормальная дерма Абдоминальная эктодерма + мезодерма стопы Эктодерма дифференцируется как на стопе Эктодерма стопы + мезодерма скальпа Эктодерма дифференцируется как на скальпе
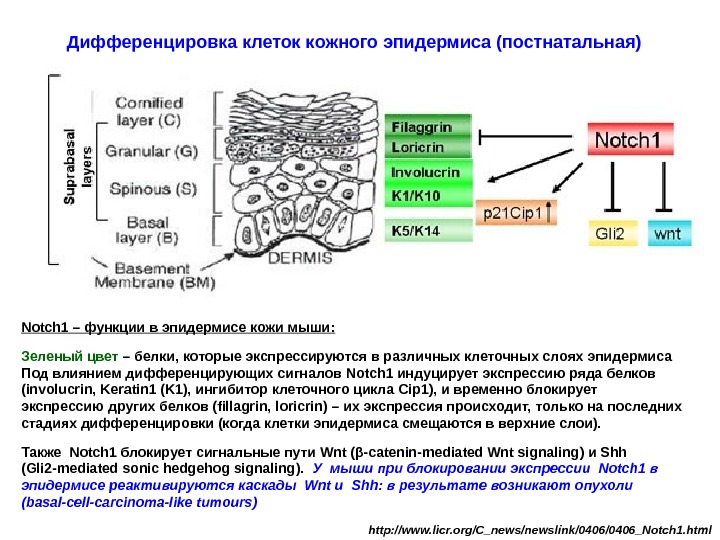
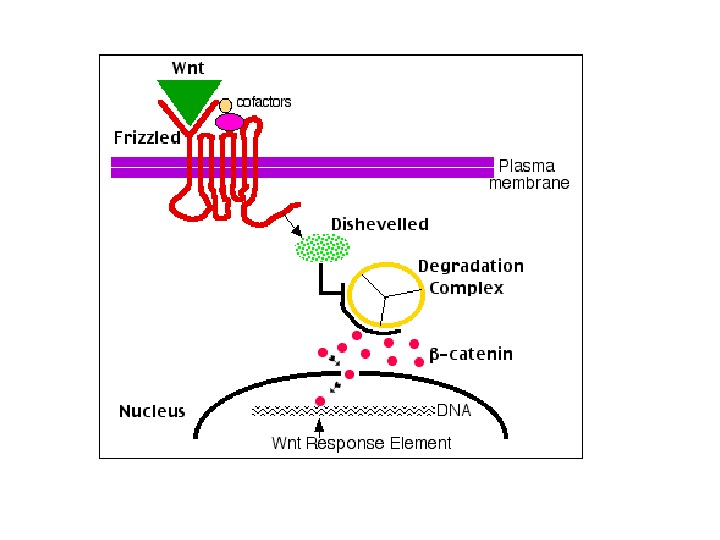
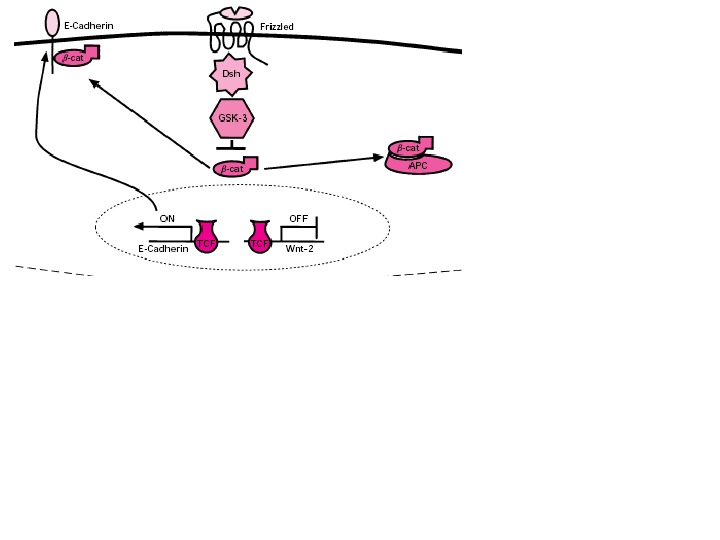
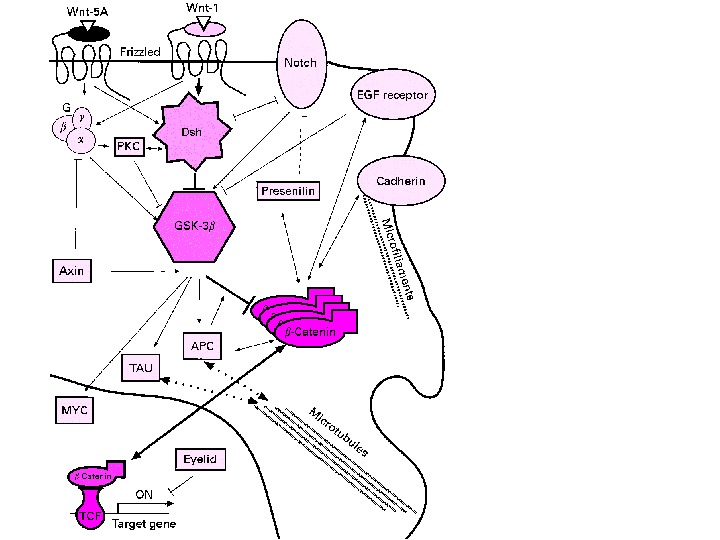
 Notch 1 – функции в эпидермисе кожи мыши: Зеленый цвет – белки, которые экспрессируются в различных клеточных слоях эпидермиса Под влиянием дифференцирующих сигналов Notch 1 индуцирует экспрессию ряда белков (involucrin, Keratin 1 (K 1), ингибитор клеточного цикла Cip 1), и временно блокирует экспрессию других белков (fillagrin, loricrin) – их экспрессия происходит, только на последних стадиях дифференцировки (когда клетки эпидермиса смещаются в верхние слои). Также Notch 1 блокирует сигнальные пути Wnt ( β-catenin-mediated Wnt signaling ) и Shh ( Gli 2 -mediated sonic hedgehog signaling ). У мыши при блокировании экспрессии Notch 1 в эпидермисе реактивируются каскады Wnt и Shh : в результате возникают опухоли (basal-cell-carcinoma-like tumours) http: //www. licr. org/C_news/newslink/0406_Notch 1. html. Дифференцировка клеток кожного эпидермиса (постнатальная)
Notch 1 – функции в эпидермисе кожи мыши: Зеленый цвет – белки, которые экспрессируются в различных клеточных слоях эпидермиса Под влиянием дифференцирующих сигналов Notch 1 индуцирует экспрессию ряда белков (involucrin, Keratin 1 (K 1), ингибитор клеточного цикла Cip 1), и временно блокирует экспрессию других белков (fillagrin, loricrin) – их экспрессия происходит, только на последних стадиях дифференцировки (когда клетки эпидермиса смещаются в верхние слои). Также Notch 1 блокирует сигнальные пути Wnt ( β-catenin-mediated Wnt signaling ) и Shh ( Gli 2 -mediated sonic hedgehog signaling ). У мыши при блокировании экспрессии Notch 1 в эпидермисе реактивируются каскады Wnt и Shh : в результате возникают опухоли (basal-cell-carcinoma-like tumours) http: //www. licr. org/C_news/newslink/0406_Notch 1. html. Дифференцировка клеток кожного эпидермиса (постнатальная)
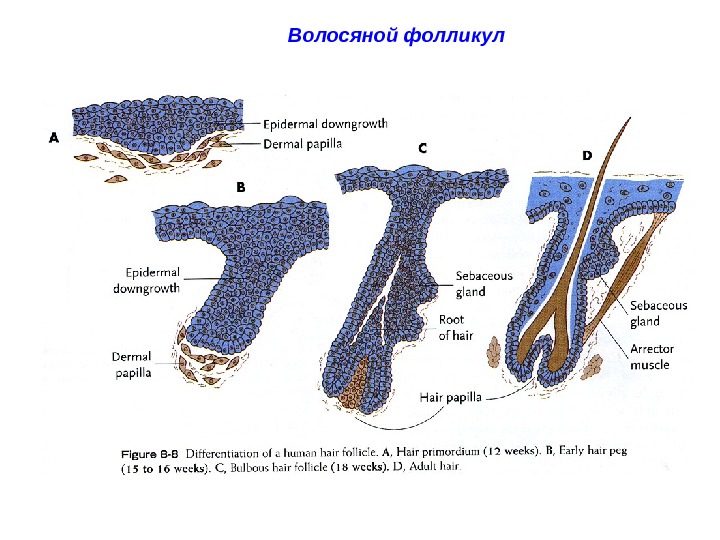
 Волосяной фолликул
Волосяной фолликул
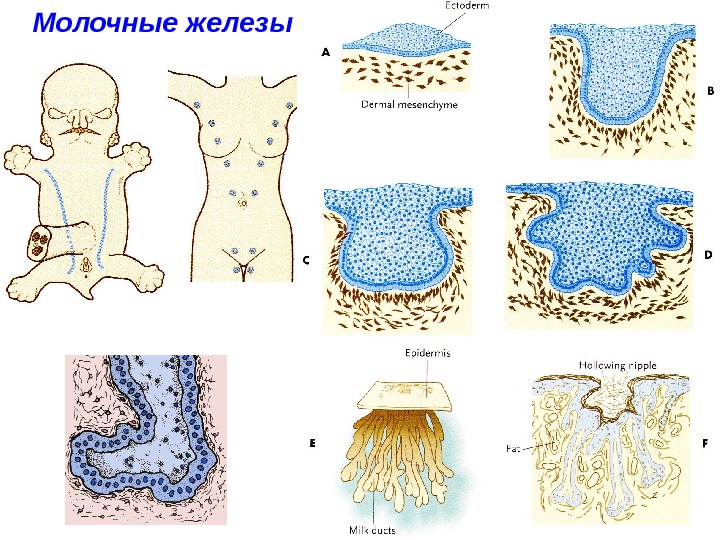
 Молочные железы
Молочные железы
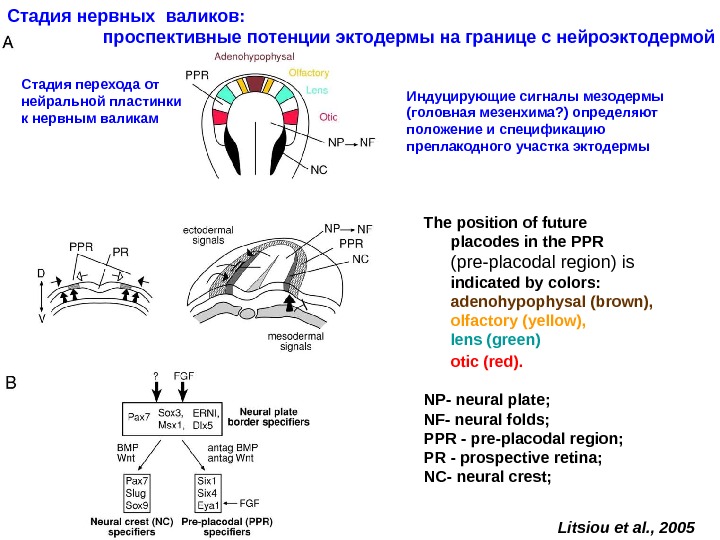
 The position of future placodes in the PPR (pre-placodal region) is indicated by colors: adenohypophysal (brown), olfactory (yellow), lens (green) otic (red). NP — neural plate; NF — neural folds; PPR — pre-placodal region; PR — prospective retina; NC- n eural crest; Litsiou et al. , 2005 Стадия нервных валиков: проспективные потенции эктодермы на границе с нейроэктодермой Стадия перехода от нейральной пластинки к нервным валикам Индуцирующие сигналы мезодермы (головная мезенхима ? ) определяют положение и спецификацию преплакодного участка эктодермы
The position of future placodes in the PPR (pre-placodal region) is indicated by colors: adenohypophysal (brown), olfactory (yellow), lens (green) otic (red). NP — neural plate; NF — neural folds; PPR — pre-placodal region; PR — prospective retina; NC- n eural crest; Litsiou et al. , 2005 Стадия нервных валиков: проспективные потенции эктодермы на границе с нейроэктодермой Стадия перехода от нейральной пластинки к нервным валикам Индуцирующие сигналы мезодермы (головная мезенхима ? ) определяют положение и спецификацию преплакодного участка эктодермы
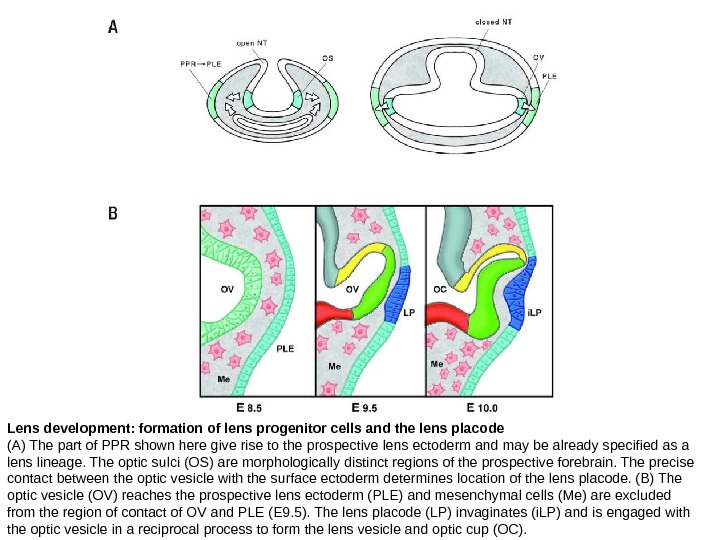
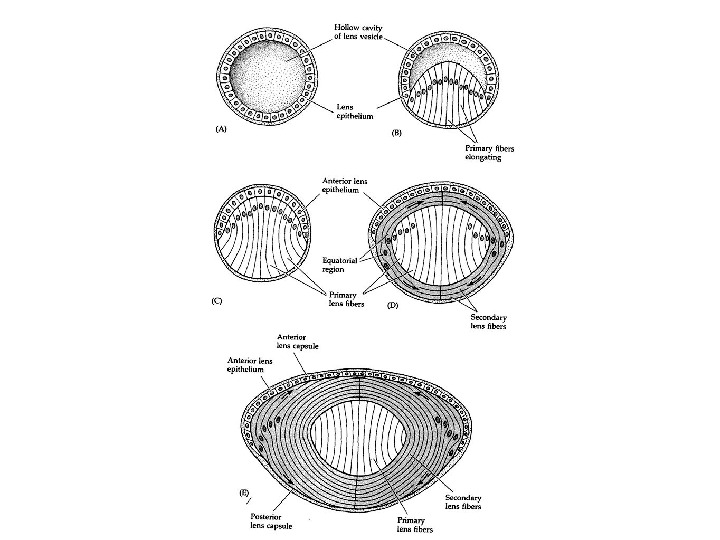
 Lens development: formation of lens progenitor cells and the lens placode (A) The part of PPR shown here give rise to the prospective lens ectoderm and may be already specified as a lens lineage. The optic sulci (OS) are morphologically distinct regions of the prospective forebrain. The precise contact between the optic vesicle with the surface ectoderm determines location of the lens placode. (B) The optic vesicle (OV) reaches the prospective lens ectoderm (PLE) and mesenchymal cells (Me) are excluded from the region of contact of OV and PLE (E 9. 5). The lens placode (LP) invaginates (i. LP) and is engaged with the optic vesicle in a reciprocal process to form the lens vesicle and optic cup (OC).
Lens development: formation of lens progenitor cells and the lens placode (A) The part of PPR shown here give rise to the prospective lens ectoderm and may be already specified as a lens lineage. The optic sulci (OS) are morphologically distinct regions of the prospective forebrain. The precise contact between the optic vesicle with the surface ectoderm determines location of the lens placode. (B) The optic vesicle (OV) reaches the prospective lens ectoderm (PLE) and mesenchymal cells (Me) are excluded from the region of contact of OV and PLE (E 9. 5). The lens placode (LP) invaginates (i. LP) and is engaged with the optic vesicle in a reciprocal process to form the lens vesicle and optic cup (OC).




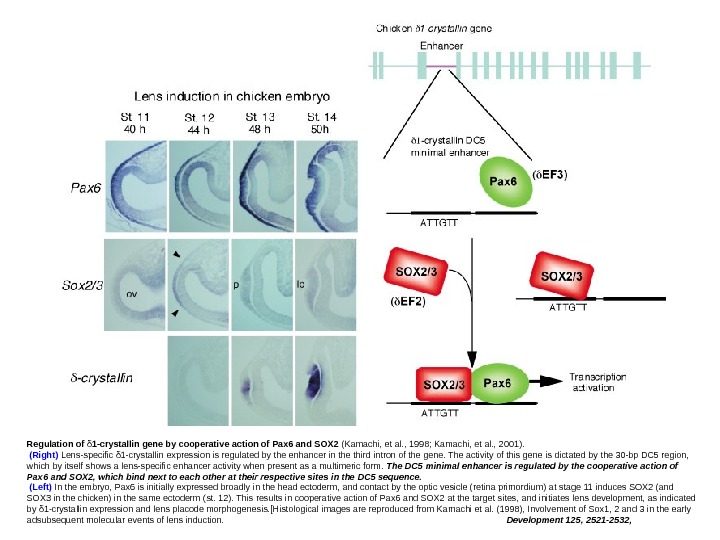
 Regulation of δ 1 -crystallin gene by cooperative action of Pax 6 and SOX 2 (Kamachi, et al. , 1998; Kamachi, et al. , 2001). (Right) Lens-specific δ 1 -crystallin expression is regulated by the enhancer in the third intron of the gene. The activity of this gene is dictated by the 30 -bp DC 5 region, which by itself shows a lens-specific enhancer activity when present as a multimeric form. The DC 5 minimal enhancer is regulated by the cooperative action of Pax 6 and SOX 2, which bind next to each other at their respective sites in the DC 5 sequence. (Left) In the embryo, Pax 6 is initially expressed broadly in the head ectoderm, and contact by the optic vesicle (retina primordium) at stage 11 induces SOX 2 (and SOX 3 in the chicken) in the same ectoderm (st. 12). This results in cooperative action of Pax 6 and SOX 2 at the target sites, and initiates lens development, as indicated by δ 1 -crystallin expression and lens placode morphogenesis. [Histological images are reproduced from Kamachi et al. (1998), Involvement of Sox 1, 2 and 3 in the early adsubsequent molecular events of lens induction. Development 125, 2521 -2532,
Regulation of δ 1 -crystallin gene by cooperative action of Pax 6 and SOX 2 (Kamachi, et al. , 1998; Kamachi, et al. , 2001). (Right) Lens-specific δ 1 -crystallin expression is regulated by the enhancer in the third intron of the gene. The activity of this gene is dictated by the 30 -bp DC 5 region, which by itself shows a lens-specific enhancer activity when present as a multimeric form. The DC 5 minimal enhancer is regulated by the cooperative action of Pax 6 and SOX 2, which bind next to each other at their respective sites in the DC 5 sequence. (Left) In the embryo, Pax 6 is initially expressed broadly in the head ectoderm, and contact by the optic vesicle (retina primordium) at stage 11 induces SOX 2 (and SOX 3 in the chicken) in the same ectoderm (st. 12). This results in cooperative action of Pax 6 and SOX 2 at the target sites, and initiates lens development, as indicated by δ 1 -crystallin expression and lens placode morphogenesis. [Histological images are reproduced from Kamachi et al. (1998), Involvement of Sox 1, 2 and 3 in the early adsubsequent molecular events of lens induction. Development 125, 2521 -2532,
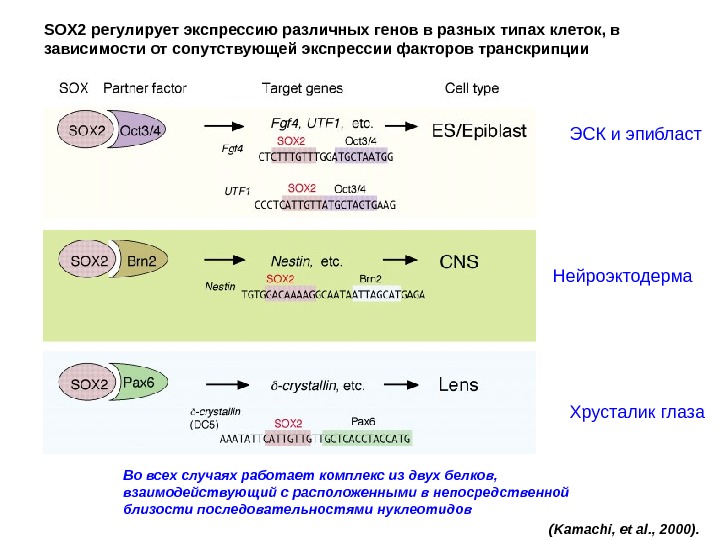
 (Kamachi, et al. , 2000). SOX 2 регулирует экспрессию различных генов в разных типах клеток, в зависимости от сопутствующей экспрессии факторов транскрипции ЭСК и эпибласт Нейроэктодерма Хрусталик глаза Во всех случаях работает комплекс из двух белков, взаимодействующий с расположенными в непосредственной близости последовательностями нуклеотидов
(Kamachi, et al. , 2000). SOX 2 регулирует экспрессию различных генов в разных типах клеток, в зависимости от сопутствующей экспрессии факторов транскрипции ЭСК и эпибласт Нейроэктодерма Хрусталик глаза Во всех случаях работает комплекс из двух белков, взаимодействующий с расположенными в непосредственной близости последовательностями нуклеотидов
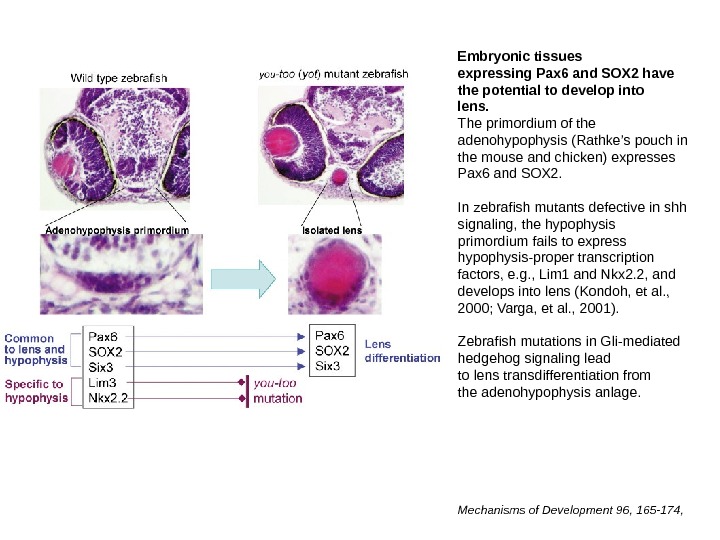
 Embryonic tissues expressing Pax 6 and SOX 2 have the potential to develop into lens. The primordium of the adenohypophysis (Rathke’s pouch in the mouse and chicken) expresses Pax 6 and SOX 2. In zebrafish mutants defective in shh signaling, the hypophysis primordium fails to express hypophysis-proper transcription factors, e. g. , Lim 1 and Nkx 2. 2, and develops into lens (Kondoh, et al. , 2000; Varga, et al. , 2001). Zebrafish mutations in Gli-mediated hedgehog signaling lead to lens transdifferentiation from the adenohypophysis anlage. Mechanisms of Development 96, 165 -174,
Embryonic tissues expressing Pax 6 and SOX 2 have the potential to develop into lens. The primordium of the adenohypophysis (Rathke’s pouch in the mouse and chicken) expresses Pax 6 and SOX 2. In zebrafish mutants defective in shh signaling, the hypophysis primordium fails to express hypophysis-proper transcription factors, e. g. , Lim 1 and Nkx 2. 2, and develops into lens (Kondoh, et al. , 2000; Varga, et al. , 2001). Zebrafish mutations in Gli-mediated hedgehog signaling lead to lens transdifferentiation from the adenohypophysis anlage. Mechanisms of Development 96, 165 -174,
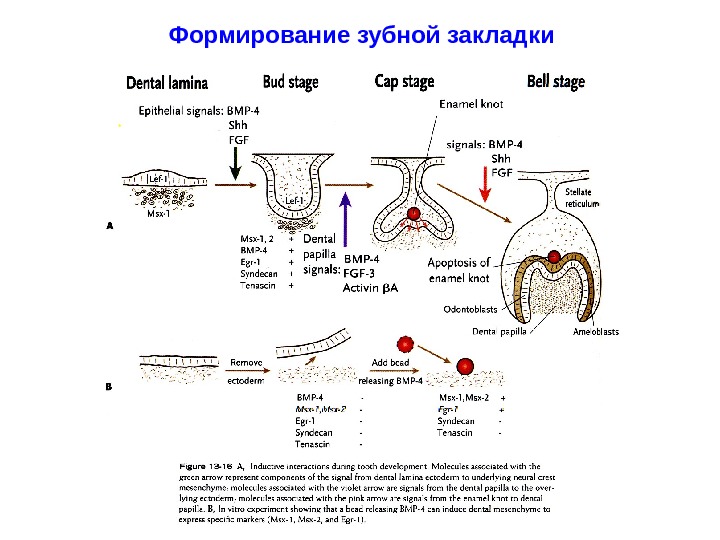
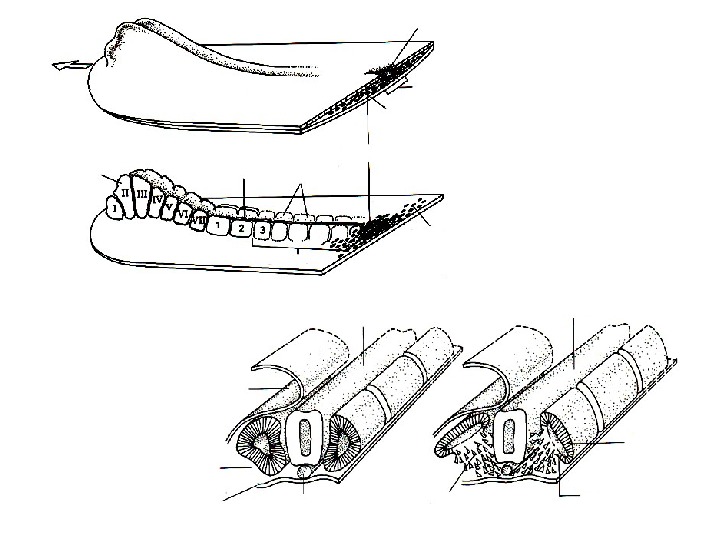
 Формирование зубной закладки
Формирование зубной закладки
 Формирование конечностей
Формирование конечностей
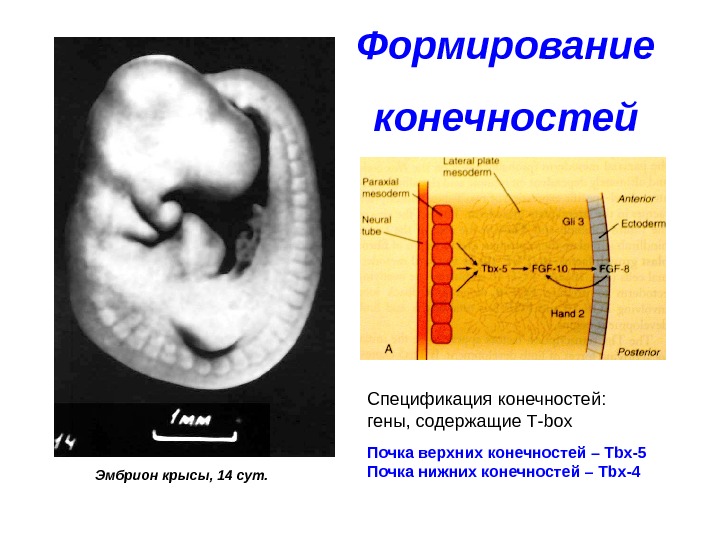
 Формирование конечностей Эмбрион крысы, 14 сут. Спецификация конечностей: гены, содержащие Т- box Почка верхних конечностей – Tbx-5 Почка нижних конечностей – Tbx-
Формирование конечностей Эмбрион крысы, 14 сут. Спецификация конечностей: гены, содержащие Т- box Почка верхних конечностей – Tbx-5 Почка нижних конечностей – Tbx-
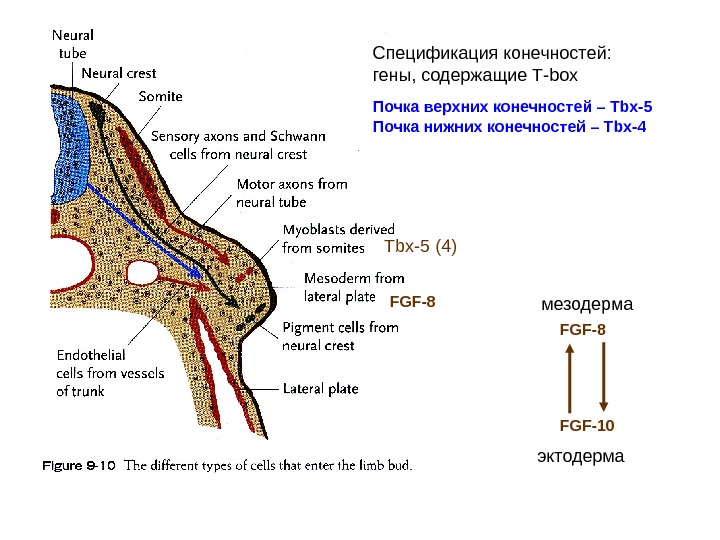
 Спецификация конечностей: гены, содержащие Т- box Почка верхних конечностей – Tbx-5 Почка нижних конечностей – Tbx- 4 Tbx-5 (4) FGF-8 FGF-10 мезодерма эктодерма
Спецификация конечностей: гены, содержащие Т- box Почка верхних конечностей – Tbx-5 Почка нижних конечностей – Tbx- 4 Tbx-5 (4) FGF-8 FGF-10 мезодерма эктодерма
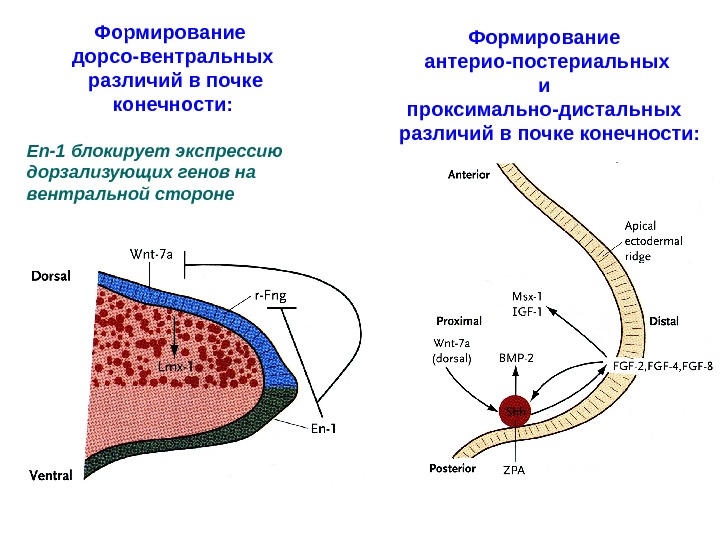
 Формирование дорсо-вентральных различий в почке конечности: En-1 блокирует экспрессию дорзализующих генов на вентральной стороне Формирование антерио-постериальных и проксимально-дистальных различий в почке конечности:
Формирование дорсо-вентральных различий в почке конечности: En-1 блокирует экспрессию дорзализующих генов на вентральной стороне Формирование антерио-постериальных и проксимально-дистальных различий в почке конечности:

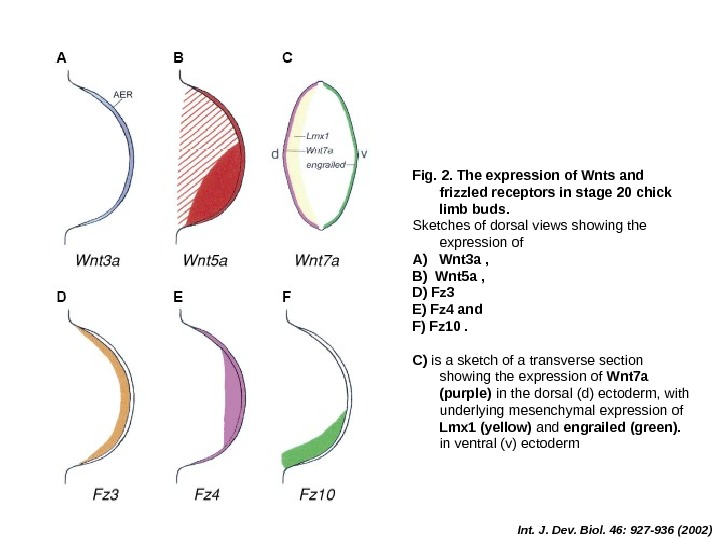
 Int. J. Dev. Biol. 46: 927 -936 (2002)Fig. 2. The expression of Wnts and frizzled receptors in stage 20 chick limb buds. Sketches of dorsal views showing the expression of A) Wnt 3 a , B) Wnt 5 a , D) Fz 3 E) Fz 4 and F) Fz 10. C) is a sketch of a transverse section showing the expression of Wnt 7 a (purple) in the dorsal (d) ectoderm, with underlying mesenchymal expression of Lmx 1 (yellow) and engrailed (green). in ventral (v) ectoderm
Int. J. Dev. Biol. 46: 927 -936 (2002)Fig. 2. The expression of Wnts and frizzled receptors in stage 20 chick limb buds. Sketches of dorsal views showing the expression of A) Wnt 3 a , B) Wnt 5 a , D) Fz 3 E) Fz 4 and F) Fz 10. C) is a sketch of a transverse section showing the expression of Wnt 7 a (purple) in the dorsal (d) ectoderm, with underlying mesenchymal expression of Lmx 1 (yellow) and engrailed (green). in ventral (v) ectoderm
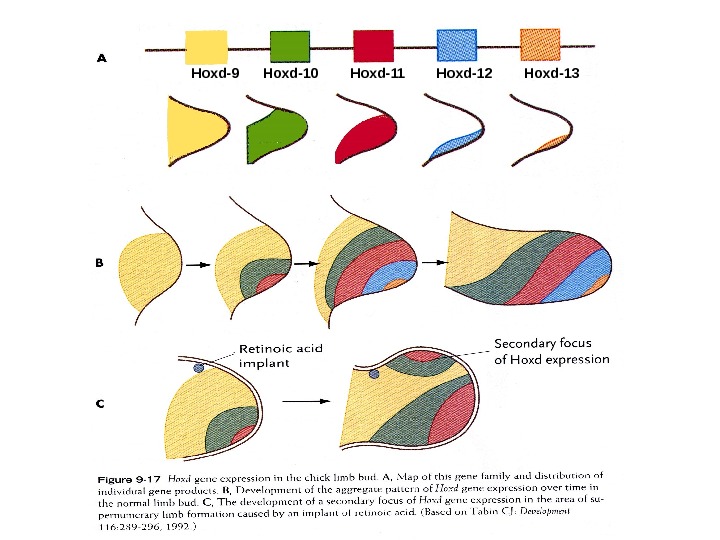
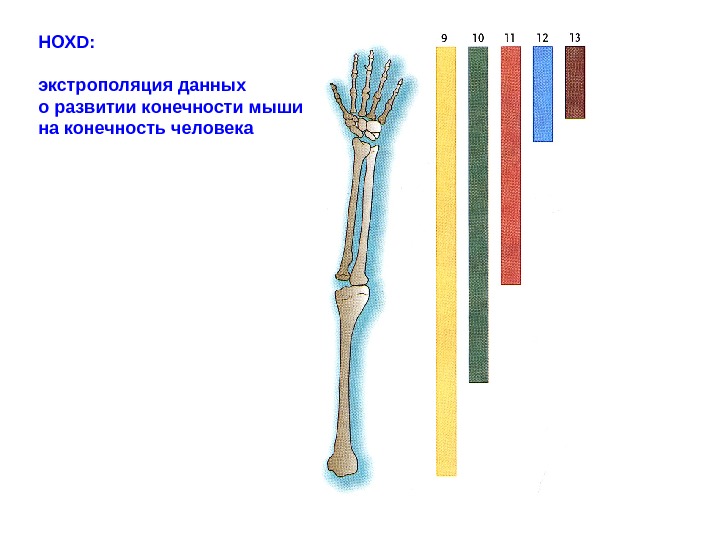
 Hoxd-9 Hoxd-10 Hoxd-11 Hoxd-12 Hoxd-
Hoxd-9 Hoxd-10 Hoxd-11 Hoxd-12 Hoxd-
 НОХ D : экстрополяция данных о развитии конечности мыши на конечность человека
НОХ D : экстрополяция данных о развитии конечности мыши на конечность человека
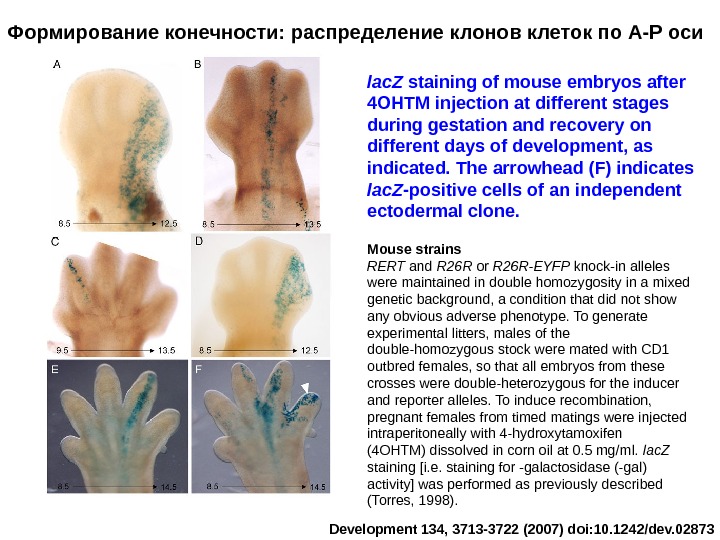
 Формирование конечности: распределение клонов клеток по А-Р оси lac. Z staining of mouse embryos after 4 OHTM injection at different stages during gestation and recovery on different days of development, as indicated. The arrowhead (F) indicates lac. Z -positive cells of an independent ectodermal clone. Development 134, 3713 -3722 (2007) doi: 10. 1242/dev. 02873 Mouse strains RERT and R 26 R or R 26 R-EYFP knock-in alleles were maintained in double homozygosity in a mixed genetic background, a condition that did not show any obvious adverse phenotype. To generate experimental litters, males of the double-homozygous stock were mated with CD 1 outbred females, so that all embryos from these crosses were double-heterozygous for the inducer and reporter alleles. To induce recombination, pregnant females from timed matings were injected intraperitoneally with 4 -hydroxytamoxifen (4 OHTM) dissolved in corn oil at 0. 5 mg/ml. lac. Z staining [i. e. staining for -galactosidase (-gal) activity] was performed as previously described (Torres, 1998).
Формирование конечности: распределение клонов клеток по А-Р оси lac. Z staining of mouse embryos after 4 OHTM injection at different stages during gestation and recovery on different days of development, as indicated. The arrowhead (F) indicates lac. Z -positive cells of an independent ectodermal clone. Development 134, 3713 -3722 (2007) doi: 10. 1242/dev. 02873 Mouse strains RERT and R 26 R or R 26 R-EYFP knock-in alleles were maintained in double homozygosity in a mixed genetic background, a condition that did not show any obvious adverse phenotype. To generate experimental litters, males of the double-homozygous stock were mated with CD 1 outbred females, so that all embryos from these crosses were double-heterozygous for the inducer and reporter alleles. To induce recombination, pregnant females from timed matings were injected intraperitoneally with 4 -hydroxytamoxifen (4 OHTM) dissolved in corn oil at 0. 5 mg/ml. lac. Z staining [i. e. staining for -galactosidase (-gal) activity] was performed as previously described (Torres, 1998).
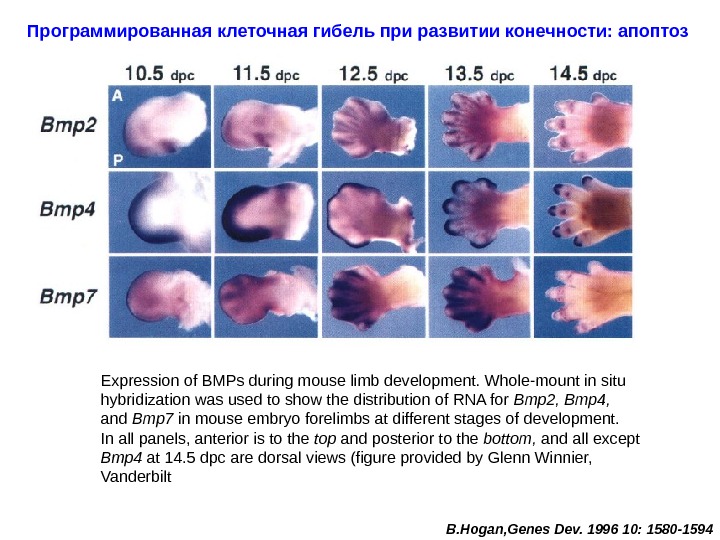
 Программированная клеточная гибель при развитии конечности: апоптоз Expression of BMPs during mouse limb development. Whole-mount in situ hybridization was used to show the distribution of RNA for Bmp 2, Bmp 4, and Bmp 7 in mouse embryo forelimbs at different stages of development. In all panels, anterior is to the top and posterior to the bottom, and all except Bmp 4 at 14. 5 dpc are dorsal views (figure provided by Glenn Winnier, Vanderbilt В. Hogan, Genes Dev. 1996 10: 1580 —
Программированная клеточная гибель при развитии конечности: апоптоз Expression of BMPs during mouse limb development. Whole-mount in situ hybridization was used to show the distribution of RNA for Bmp 2, Bmp 4, and Bmp 7 in mouse embryo forelimbs at different stages of development. In all panels, anterior is to the top and posterior to the bottom, and all except Bmp 4 at 14. 5 dpc are dorsal views (figure provided by Glenn Winnier, Vanderbilt В. Hogan, Genes Dev. 1996 10: 1580 —
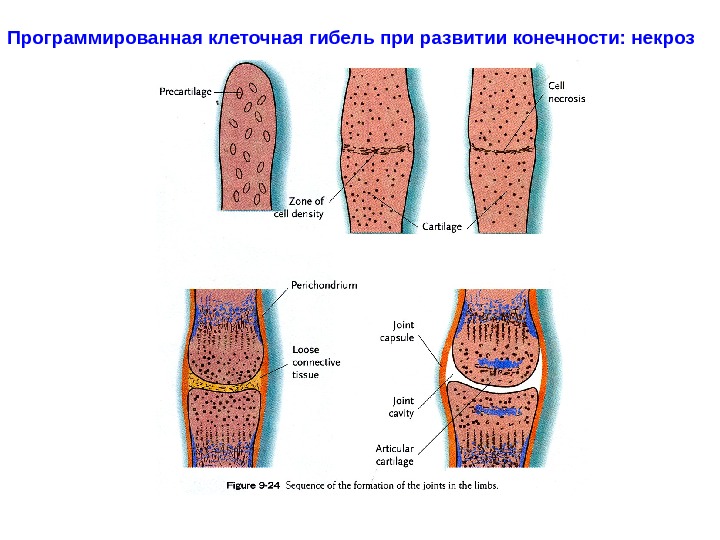
 Программированная клеточная гибель при развитии конечности: некроз
Программированная клеточная гибель при развитии конечности: некроз
 ЛИШНИЕ СЛАЙДЫ —
ЛИШНИЕ СЛАЙДЫ —

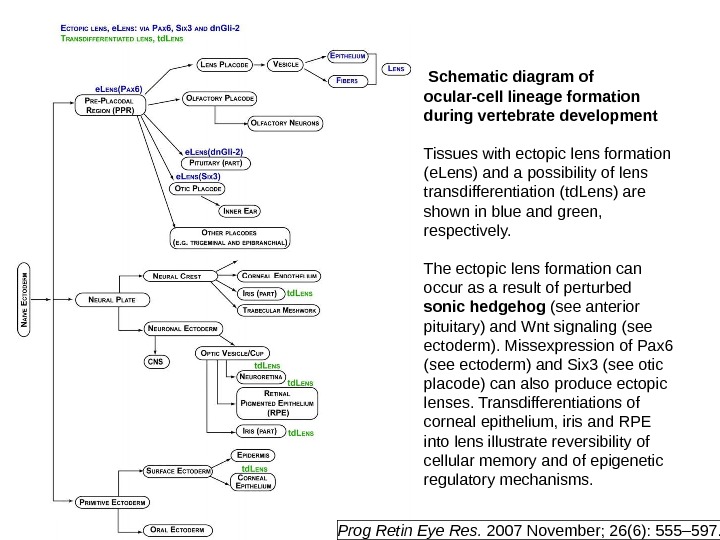
 Schematic diagram of ocular-cell lineage formation during vertebrate development Tissues with ectopic lens formation (e. Lens) and a possibility of lens transdifferentiation (td. Lens) are shown in blue and green, r espectively. The ectopic lens formation can occur as a result of perturbed sonic hedgehog (see anterior pituitary) and Wnt signaling (see ectoderm). Missexpression of Pax 6 (see ectoderm) and Six 3 (see otic placode) can also produce ectopic lenses. Transdifferentiations of corneal epithelium, iris and RPE into lens illustrate reversibility of cellular memory and of epigenetic regulatory mechanisms. Prog Retin Eye Res. 2007 November; 26(6): 555– 597.
Schematic diagram of ocular-cell lineage formation during vertebrate development Tissues with ectopic lens formation (e. Lens) and a possibility of lens transdifferentiation (td. Lens) are shown in blue and green, r espectively. The ectopic lens formation can occur as a result of perturbed sonic hedgehog (see anterior pituitary) and Wnt signaling (see ectoderm). Missexpression of Pax 6 (see ectoderm) and Six 3 (see otic placode) can also produce ectopic lenses. Transdifferentiations of corneal epithelium, iris and RPE into lens illustrate reversibility of cellular memory and of epigenetic regulatory mechanisms. Prog Retin Eye Res. 2007 November; 26(6): 555– 597.

 Int. J. Dev. Biol. 46: 927 -936 (2002)
Int. J. Dev. Biol. 46: 927 -936 (2002)

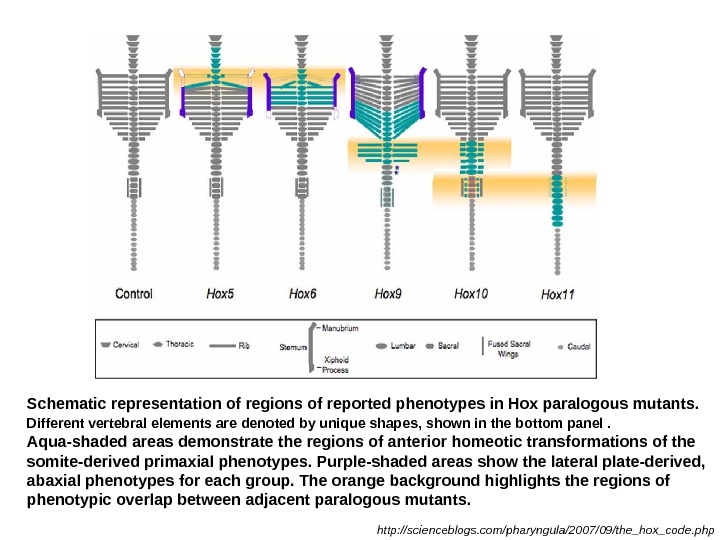
 Schematic representation of regions of reported phenotypes in Hox paralogous mutants. Different vertebral elements are denoted by unique shapes, shown in the bottom panel. Aqua-shaded areas demonstrate the regions of anterior homeotic transformations of the somite-derived primaxial phenotypes. Purple-shaded areas show the lateral plate-derived, abaxial phenotypes for each group. The orange background highlights the regions of phenotypic overlap between adjacent paralogous mutants. http: //scienceblogs. com/pharyngula/2007/09/the_hox_code. php
Schematic representation of regions of reported phenotypes in Hox paralogous mutants. Different vertebral elements are denoted by unique shapes, shown in the bottom panel. Aqua-shaded areas demonstrate the regions of anterior homeotic transformations of the somite-derived primaxial phenotypes. Purple-shaded areas show the lateral plate-derived, abaxial phenotypes for each group. The orange background highlights the regions of phenotypic overlap between adjacent paralogous mutants. http: //scienceblogs. com/pharyngula/2007/09/the_hox_code. php





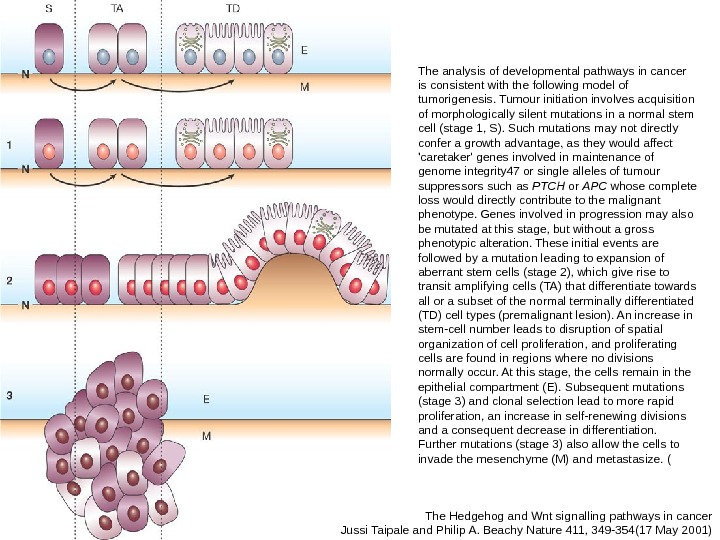
 The Hedgehog and Wnt signalling pathways in cancer Jussi Taipale and Philip A. Beachy Nature 411, 349 -354(17 May 2001) The analysis of developmental pathways in cancer is consistent with the following model of tumorigenesis. Tumour initiation involves acquisition of morphologically silent mutations in a normal stem cell (stage 1, S). Such mutations may not directly confer a growth advantage, as they would affect ‘caretaker’ genes involved in maintenance of genome integrity 47 or single alleles of tumour suppressors such as PTCH or APC whose complete loss would directly contribute to the malignant phenotype. Genes involved in progression may also be mutated at this stage, but without a gross phenotypic alteration. These initial events are followed by a mutation leading to expansion of aberrant stem cells (stage 2), which give rise to transit amplifying cells (TA) that differentiate towards all or a subset of the normal terminally differentiated (TD) cell types (premalignant lesion). An increase in stem-cell number leads to disruption of spatial organization of cell proliferation, and proliferating cells are found in regions where no divisions normally occur. At this stage, the cells remain in the epithelial compartment (E). Subsequent mutations (stage 3) and clonal selection lead to more rapid proliferation, an increase in self-renewing divisions and a consequent decrease in differentiation. Further mutations (stage 3) also allow the cells to invade the mesenchyme (M) and metastasize. (
The Hedgehog and Wnt signalling pathways in cancer Jussi Taipale and Philip A. Beachy Nature 411, 349 -354(17 May 2001) The analysis of developmental pathways in cancer is consistent with the following model of tumorigenesis. Tumour initiation involves acquisition of morphologically silent mutations in a normal stem cell (stage 1, S). Such mutations may not directly confer a growth advantage, as they would affect ‘caretaker’ genes involved in maintenance of genome integrity 47 or single alleles of tumour suppressors such as PTCH or APC whose complete loss would directly contribute to the malignant phenotype. Genes involved in progression may also be mutated at this stage, but without a gross phenotypic alteration. These initial events are followed by a mutation leading to expansion of aberrant stem cells (stage 2), which give rise to transit amplifying cells (TA) that differentiate towards all or a subset of the normal terminally differentiated (TD) cell types (premalignant lesion). An increase in stem-cell number leads to disruption of spatial organization of cell proliferation, and proliferating cells are found in regions where no divisions normally occur. At this stage, the cells remain in the epithelial compartment (E). Subsequent mutations (stage 3) and clonal selection lead to more rapid proliferation, an increase in self-renewing divisions and a consequent decrease in differentiation. Further mutations (stage 3) also allow the cells to invade the mesenchyme (M) and metastasize. (


