Большинство патогенных для людей грибов широко распространены в






























4_protivogribkovy_immunitet.ppt
- Размер: 3.1 Мб
- Автор:
- Количество слайдов: 41
Описание презентации Большинство патогенных для людей грибов широко распространены в по слайдам

 Большинство патогенных для людей грибов широко распространены в природе. Заражение происходит при попадании спор, разносимых воздухом, в легкие и придаточные пазухи носа, а также при внедрении спор или мицелия в кожу и роговицу.
Большинство патогенных для людей грибов широко распространены в природе. Заражение происходит при попадании спор, разносимых воздухом, в легкие и придаточные пазухи носа, а также при внедрении спор или мицелия в кожу и роговицу.
 Заражение от других лиц и животных наблюдается крайне редко. Для каждого из грибов характерны определенный путь внедрения и поражение определенных тканей. Дерматофитии, отрубевидный лишай и пьедра — это инфекции эпидермиса, ногтей и волос. Споротрихоз и мицетома развиваются при попадании возбудителя в подкожную клетчатку. Глубокие микозы — при попадании возбудителя в дыхательные пути.
Заражение от других лиц и животных наблюдается крайне редко. Для каждого из грибов характерны определенный путь внедрения и поражение определенных тканей. Дерматофитии, отрубевидный лишай и пьедра — это инфекции эпидермиса, ногтей и волос. Споротрихоз и мицетома развиваются при попадании возбудителя в подкожную клетчатку. Глубокие микозы — при попадании возбудителя в дыхательные пути.
 После контакта с грибами может сформироваться иммунитет , который впоследствии будет частично предохранять от заражения. Там, где распространены те или иные грибковые инфекции, местные жители болеют ими реже, чем приезжие. В патогенезе большинства других глубоких микозов первостепенную роль играет состояние клеточного иммунитета.
После контакта с грибами может сформироваться иммунитет , который впоследствии будет частично предохранять от заражения. Там, где распространены те или иные грибковые инфекции, местные жители болеют ими реже, чем приезжие. В патогенезе большинства других глубоких микозов первостепенную роль играет состояние клеточного иммунитета.
 Противогрибковый иммунитет характеризуется разнообразием проявлений, что связано с: 1. Сложностью антигенного состава гриба; 2. Изменчивостью гриба, зависящей от условий существования, формы и стадии микоза.
Противогрибковый иммунитет характеризуется разнообразием проявлений, что связано с: 1. Сложностью антигенного состава гриба; 2. Изменчивостью гриба, зависящей от условий существования, формы и стадии микоза.
 В случае контакта грибкового антигена с клеточными компонентами иммунной системы развивается гиперчувствительность замедленного типа (аллергическое состояние) , при этом иммунные реакции клеточного типа могут сохраняться длительное время, иногда на протяжении всей жизни. При микозах синтезируются антитела всех классов. Однако они не играют существенной роли в механизме защиты , а свидетельствуют лишь о наличии заболевания , хотя и принимают участие в патогенезе развития заболевания.
В случае контакта грибкового антигена с клеточными компонентами иммунной системы развивается гиперчувствительность замедленного типа (аллергическое состояние) , при этом иммунные реакции клеточного типа могут сохраняться длительное время, иногда на протяжении всей жизни. При микозах синтезируются антитела всех классов. Однако они не играют существенной роли в механизме защиты , а свидетельствуют лишь о наличии заболевания , хотя и принимают участие в патогенезе развития заболевания.
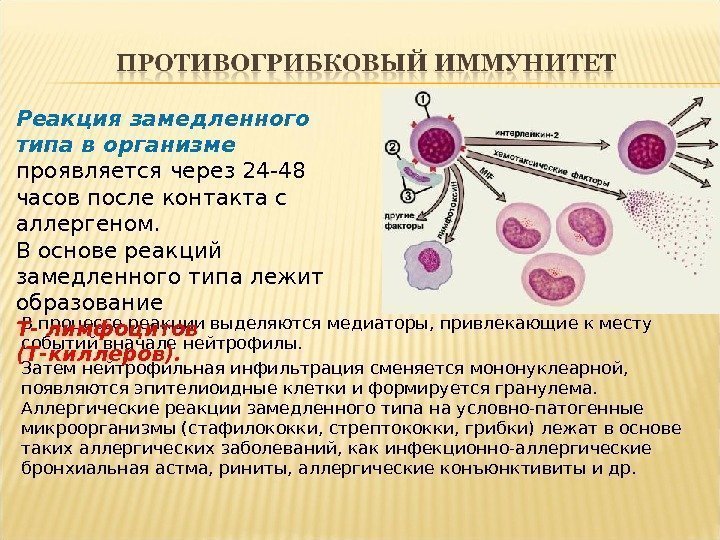
 В процессе реакции выделяются медиаторы, привлекающие к месту событий вначале нейтрофилы. Затем нейтрофильная инфильтрация сменяется мононуклеарной, появляются эпителиоидные клетки и формируется гранулема. Аллергические реакции замедленного типа на условно-патогенные микроорганизмы (стафилококки, стрептококки, грибки) лежат в основе таких аллергических заболеваний, как инфекционно-аллергические бронхиальная астма, риниты, аллергические конъюнктивиты и др. Реакция замедленного типа в организме проявляется через 24 -48 часов после контакта с аллергеном. В основе реакций замедленного типа лежит образование Т- лимфоцитов (Т-киллеров).
В процессе реакции выделяются медиаторы, привлекающие к месту событий вначале нейтрофилы. Затем нейтрофильная инфильтрация сменяется мононуклеарной, появляются эпителиоидные клетки и формируется гранулема. Аллергические реакции замедленного типа на условно-патогенные микроорганизмы (стафилококки, стрептококки, грибки) лежат в основе таких аллергических заболеваний, как инфекционно-аллергические бронхиальная астма, риниты, аллергические конъюнктивиты и др. Реакция замедленного типа в организме проявляется через 24 -48 часов после контакта с аллергеном. В основе реакций замедленного типа лежит образование Т- лимфоцитов (Т-киллеров).
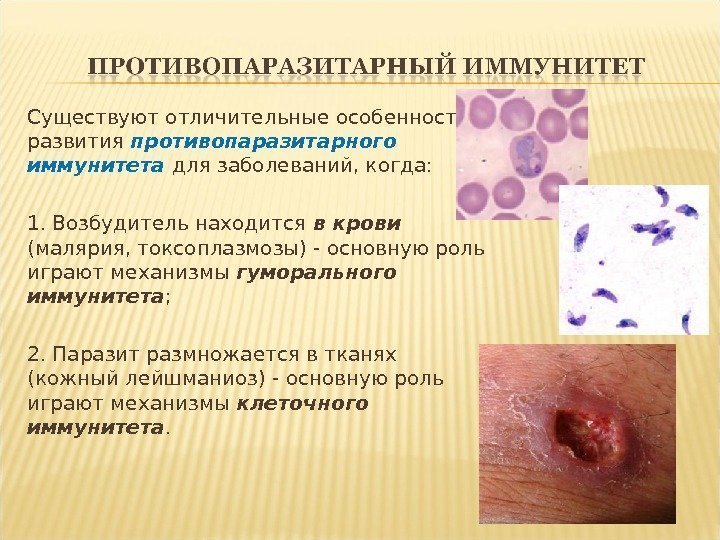
 Существуют отличительные особенности развития противопаразитарного иммунитета для заболеваний, когда: 1. Возбудитель находится в крови (малярия, токсоплазмозы) — основную роль играют механизмы гуморального иммунитета ; 2. Паразит размножается в тканях (кожный лейшманиоз) — основную роль играют механизмы клеточного иммунитета.
Существуют отличительные особенности развития противопаразитарного иммунитета для заболеваний, когда: 1. Возбудитель находится в крови (малярия, токсоплазмозы) — основную роль играют механизмы гуморального иммунитета ; 2. Паразит размножается в тканях (кожный лейшманиоз) — основную роль играют механизмы клеточного иммунитета.
 Гуморальный иммунитет Антитела, присутствующие в крови в достаточной концентрации, эффективно защищают организм хозяина от паразитов, живущих в крови. Эффекторными механизмами являются опсонизация, фагоцитоз и комплементзависимый лизис. Особенностью иммунного ответа на глистные инвазии служит высокий уровень Ig. E. Активизированные тучные клетки , поверхности которых нагружены данным классом иммуноглобулинов, привлекают к месту инфекции сывороточные белки (содержащие высокие концентрации иммуноглобулинов) и способствуют выделению хемотаксического фактора эозинофилов , который 1 высвобождается из гранул эозинофилов и убивает паразита.
Гуморальный иммунитет Антитела, присутствующие в крови в достаточной концентрации, эффективно защищают организм хозяина от паразитов, живущих в крови. Эффекторными механизмами являются опсонизация, фагоцитоз и комплементзависимый лизис. Особенностью иммунного ответа на глистные инвазии служит высокий уровень Ig. E. Активизированные тучные клетки , поверхности которых нагружены данным классом иммуноглобулинов, привлекают к месту инфекции сывороточные белки (содержащие высокие концентрации иммуноглобулинов) и способствуют выделению хемотаксического фактора эозинофилов , который 1 высвобождается из гранул эозинофилов и убивает паразита.
 В развитии клеточного иммунитета играют большую роль цитотоксические Т-лимфоциты , продуцирующие лимфокины. Они активируют макрофаги , придавая им способность убивать внутриклеточных паразитов (таких как токсоплазма, трипаносома, лейшмания), которые иначе могут избежать действия макрофагов. Большинство простейших оказывает подавляющее действие на фагоцитоз , поскольку их клетки имеют большие размеры. Лучше всего протозойные инфекции фагоцитируются эозинофилами , которые являются резервным и последним звеном иммунной защиты.
В развитии клеточного иммунитета играют большую роль цитотоксические Т-лимфоциты , продуцирующие лимфокины. Они активируют макрофаги , придавая им способность убивать внутриклеточных паразитов (таких как токсоплазма, трипаносома, лейшмания), которые иначе могут избежать действия макрофагов. Большинство простейших оказывает подавляющее действие на фагоцитоз , поскольку их клетки имеют большие размеры. Лучше всего протозойные инфекции фагоцитируются эозинофилами , которые являются резервным и последним звеном иммунной защиты.
 Свойства опухоли 1. Способность к бесконтрольному росту 2. Автономность (самоуправление в результате нарушения взаимодействия с организмом).
Свойства опухоли 1. Способность к бесконтрольному росту 2. Автономность (самоуправление в результате нарушения взаимодействия с организмом).
 Причины нарушения: 1. Геномные перестройки в опухолевой клетке, ведущие к изменению ее структуры и функции: а) количественные изменения хромосом; б) структурные изменения хромосом; в)нарушение репарации ДНК. 2. Местная гипоксия 3. Иммунодепрессия 4. Нарушение нормальных межклеточных взаимодействий
Причины нарушения: 1. Геномные перестройки в опухолевой клетке, ведущие к изменению ее структуры и функции: а) количественные изменения хромосом; б) структурные изменения хромосом; в)нарушение репарации ДНК. 2. Местная гипоксия 3. Иммунодепрессия 4. Нарушение нормальных межклеточных взаимодействий
 Рост опухолей зависит от развития в них сосудистой сети. В мелких новообразованиях отмечается низкий уровень питательных веществ и кислорода, поступающих в опухоль путем диффузии.
Рост опухолей зависит от развития в них сосудистой сети. В мелких новообразованиях отмечается низкий уровень питательных веществ и кислорода, поступающих в опухоль путем диффузии.
 Опухолевые клетки синтезируют онкобелки и факторы роста , которые стимулируют их деление и оказывают иммунодепрессивное действие. Данные факторы нормальными гистологическими предшественниками не выделяются. Гены, подавляющие деление клеток, в опухолевых клетках отсутствуют или заблокированы. Веществ, тормозящих деление клеток, опухолевые клетки не выделяют.
Опухолевые клетки синтезируют онкобелки и факторы роста , которые стимулируют их деление и оказывают иммунодепрессивное действие. Данные факторы нормальными гистологическими предшественниками не выделяются. Гены, подавляющие деление клеток, в опухолевых клетках отсутствуют или заблокированы. Веществ, тормозящих деление клеток, опухолевые клетки не выделяют.
 Автономность опухоли достигает максимума на стадии метастазирования, когда опухолевые клетки приобретают способность: — проникать в кровеносные или лимфатические сосуды; — мигрировать в них; — сохранять жизнеспособность; -приживаться на новом месте в новом микроокружении.
Автономность опухоли достигает максимума на стадии метастазирования, когда опухолевые клетки приобретают способность: — проникать в кровеносные или лимфатические сосуды; — мигрировать в них; — сохранять жизнеспособность; -приживаться на новом месте в новом микроокружении.
 Способность к метастазированию зависит также от синтеза опухолевыми клетками протеолитических ферментов. Существуют сложные взаимодействия между опухолевыми клетками и организмом-опухоленосителем , которые охватывают реакцию организма на опухолевый рост и воздействие самой опухоли на организм. Иммунная система способна реагировать на возникновение трансформированных клеток в организме, поскольку они продуцируют уникальные опухолевые антигены. При возникновении опухолевого процесса в организме начинают образовываться все классы антител (Ig. M, Ig. G, Ig. E; тормозится синтез Ig. A и Ig. D).
Способность к метастазированию зависит также от синтеза опухолевыми клетками протеолитических ферментов. Существуют сложные взаимодействия между опухолевыми клетками и организмом-опухоленосителем , которые охватывают реакцию организма на опухолевый рост и воздействие самой опухоли на организм. Иммунная система способна реагировать на возникновение трансформированных клеток в организме, поскольку они продуцируют уникальные опухолевые антигены. При возникновении опухолевого процесса в организме начинают образовываться все классы антител (Ig. M, Ig. G, Ig. E; тормозится синтез Ig. A и Ig. D).
 Характерной особенностью синтеза антител является длительный период задержки антителообразования (lag-период) , который наступает после первичного контакта с опухолевыми антигенами и в среднем составляет 3— 4 месяца. После того, как организм начинает синтез противоопухолевых антител, реализация их иммунной роли остается под вопросом вследствие образования, в свою очередь, на них аутоантител. Данные аутоантитела образуются к двум различным структурам иммуноглобулинов: Fab- и Fс-фрагментам
Характерной особенностью синтеза антител является длительный период задержки антителообразования (lag-период) , который наступает после первичного контакта с опухолевыми антигенами и в среднем составляет 3— 4 месяца. После того, как организм начинает синтез противоопухолевых антител, реализация их иммунной роли остается под вопросом вследствие образования, в свою очередь, на них аутоантител. Данные аутоантитела образуются к двум различным структурам иммуноглобулинов: Fab- и Fс-фрагментам
 В начале процесса аутоиммунизации происходит блокировка активности антител , синтезирующихся против антигенов опухоли. Увеличение аутоантител к Fc-фрагментам антител стимулирует опухолевый рост , способствует метастазированию процесса. Противоопухолевый иммунитет реализуется Т-киллерами, NK-клетками (нормальными киллерами) и макрофагами, прямыми межклеточными контактами иммунокомпетентных клеток с опухолевыми клетками.
В начале процесса аутоиммунизации происходит блокировка активности антител , синтезирующихся против антигенов опухоли. Увеличение аутоантител к Fc-фрагментам антител стимулирует опухолевый рост , способствует метастазированию процесса. Противоопухолевый иммунитет реализуется Т-киллерами, NK-клетками (нормальными киллерами) и макрофагами, прямыми межклеточными контактами иммунокомпетентных клеток с опухолевыми клетками.
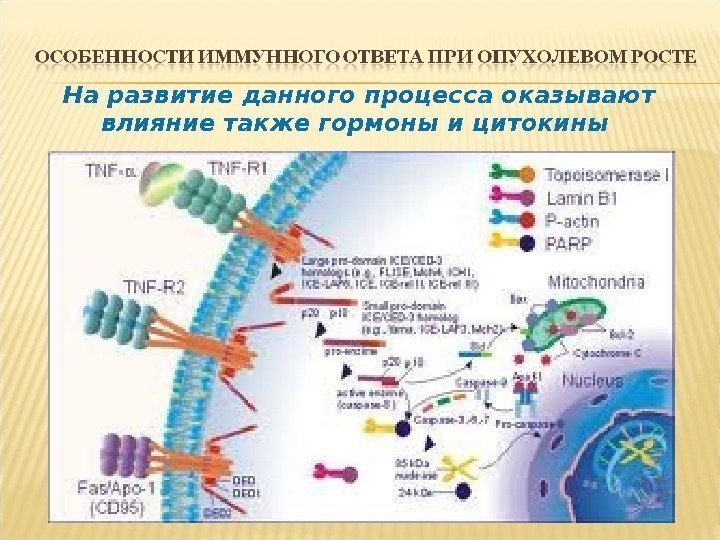
 На развитие данного процесса оказывают влияние также гормоны и цитокины
На развитие данного процесса оказывают влияние также гормоны и цитокины
 Т-киллеры — распознают опухолевые антигены, т. к. на мембране опухолевой клетки присутствуют антигены 1 -го класса. — синтезируют фактор некроза опухоли (ФНО) Среднее содержание Т-киллеров при развитии опухолевого процесса колеблется в пределах 3— 38%. Содержание Т- киллеров — до 30% вызывает спонтанный лизис опухоли в 0, 5% случаев — более 30% способствует лизису в 5% случаев. NK-клетки — вызывают деструкцию опухолевой ткани без предварительной сенсебилизации, — осуществляют лизис опухолевых клеток вне зависимости экспрессии генов HLA на их поверхности и связываются с опухолевыми клетками за счет Fc-фрагмента иммуноглобулинов и специфических рецепторов.
Т-киллеры — распознают опухолевые антигены, т. к. на мембране опухолевой клетки присутствуют антигены 1 -го класса. — синтезируют фактор некроза опухоли (ФНО) Среднее содержание Т-киллеров при развитии опухолевого процесса колеблется в пределах 3— 38%. Содержание Т- киллеров — до 30% вызывает спонтанный лизис опухоли в 0, 5% случаев — более 30% способствует лизису в 5% случаев. NK-клетки — вызывают деструкцию опухолевой ткани без предварительной сенсебилизации, — осуществляют лизис опухолевых клеток вне зависимости экспрессии генов HLA на их поверхности и связываются с опухолевыми клетками за счет Fc-фрагмента иммуноглобулинов и специфических рецепторов.
 Иммунные макрофаги оказывают более сильное действие на опухолевые клетки, чем Т-киллеры. Эффект проявляется в соотношении 1: 1 ( у Т-киллеров — в соотношении 100: 1 ). Среднее содержание макрофагов при развитии опухоли колеблется в пределах от 5 до 60%. Низкое содержание макрофагов (до 30%) присутствует при высоком уровне метастазирования — 97% Более высокое содержание (более 30%) уровень метастазирования падает до 8— 9%.
Иммунные макрофаги оказывают более сильное действие на опухолевые клетки, чем Т-киллеры. Эффект проявляется в соотношении 1: 1 ( у Т-киллеров — в соотношении 100: 1 ). Среднее содержание макрофагов при развитии опухоли колеблется в пределах от 5 до 60%. Низкое содержание макрофагов (до 30%) присутствует при высоком уровне метастазирования — 97% Более высокое содержание (более 30%) уровень метастазирования падает до 8— 9%.
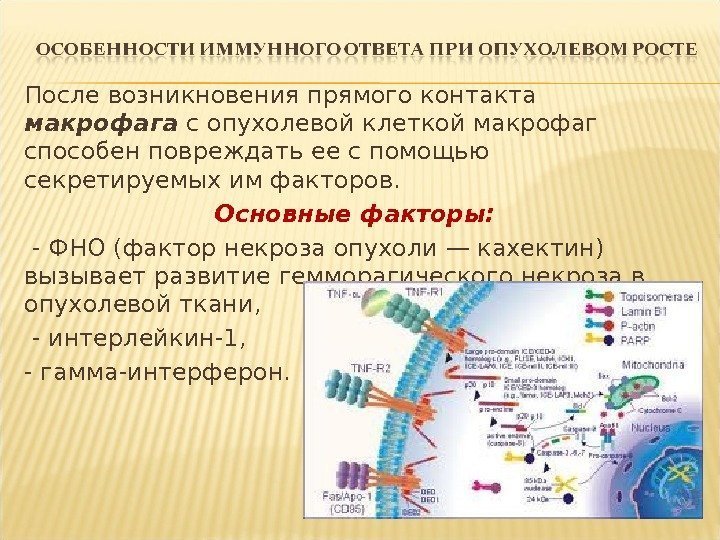
 После возникновения прямого контакта макрофага с опухолевой клеткой макрофаг способен повреждать ее с помощью секретируемых им факторов. Основные факторы: — ФНО (фактор некроза опухоли — кахектин) вызывает развитие гемморагического некроза в опухолевой ткани, — интерлейкин-1, — гамма-интерферон.
После возникновения прямого контакта макрофага с опухолевой клеткой макрофаг способен повреждать ее с помощью секретируемых им факторов. Основные факторы: — ФНО (фактор некроза опухоли — кахектин) вызывает развитие гемморагического некроза в опухолевой ткани, — интерлейкин-1, — гамма-интерферон.
 Сосудистый фактор приводит к тромбообразованию и распаду новообразования. Прямое действие макрофагов осуществляется в результате связывания фактора некроза опухоли с рецепторами опухолевой клетки. Иммуномодулирующее действие ФНО опосредуется путем стимуляции выработки макрофагами и Т-лимфоцитами интерлейкинов, гамма-интерферона, активации NK-клеток и нейтрофилов. Активация макрофагов с выбросом большого количества ФНО может привести к развитию коллапса и шока.
Сосудистый фактор приводит к тромбообразованию и распаду новообразования. Прямое действие макрофагов осуществляется в результате связывания фактора некроза опухоли с рецепторами опухолевой клетки. Иммуномодулирующее действие ФНО опосредуется путем стимуляции выработки макрофагами и Т-лимфоцитами интерлейкинов, гамма-интерферона, активации NK-клеток и нейтрофилов. Активация макрофагов с выбросом большого количества ФНО может привести к развитию коллапса и шока.
 Интерлейкины — оказывают прямое цитотоксическое действие на опухоль; — повышают активность цитотоксических макрофагов, Т-киллеров, NK-клеток; — усиливают продукцию интерферона; — стимулируют дифференцировку опухолевых клеток, действуя как фактор роста; — супрессируют противоопухолевые иммунные реакции.
Интерлейкины — оказывают прямое цитотоксическое действие на опухоль; — повышают активность цитотоксических макрофагов, Т-киллеров, NK-клеток; — усиливают продукцию интерферона; — стимулируют дифференцировку опухолевых клеток, действуя как фактор роста; — супрессируют противоопухолевые иммунные реакции.
 Гамма-интерферон — блокирует транскрипцию онковирусной РНК и белков в клетке; — способен на прямое цитотоксическое действие; — активизирует макрофаги, NK-клетки, Т- и В-лимфоциты. Человеческий гамма-интерферон
Гамма-интерферон — блокирует транскрипцию онковирусной РНК и белков в клетке; — способен на прямое цитотоксическое действие; — активизирует макрофаги, NK-клетки, Т- и В-лимфоциты. Человеческий гамма-интерферон
 Причины малой эффективности иммунного ответа на опухолевый процесс: — антигенность большинства опухолей низкая; — на многих опухолевых клетках нарушена экспрессия генов главного комплекса гистосовместимости, что отрицательно сказывается на цитотоксические свойства Т-киллеров; — при связывании с противоопухолевыми антителами рост опухоли усиливается; — в организме развивается общая и местная иммунодепрессия под влиянием выработки опухолевой тканью специфических факторов. Общее содержание лимфоцитов остается в пределах нормы , содержание Т- хелперов, Т-супрессоров, В-лимфоцитов (соответственно и антител классов Ig. M, Ig. G, Ig. E) может быть увеличено. Ниже физиологических нормативов обычно регистрируется общее содержание Т-лимфоцитов, Т-киллеров, а также иммуноглобулинов А и D.
Причины малой эффективности иммунного ответа на опухолевый процесс: — антигенность большинства опухолей низкая; — на многих опухолевых клетках нарушена экспрессия генов главного комплекса гистосовместимости, что отрицательно сказывается на цитотоксические свойства Т-киллеров; — при связывании с противоопухолевыми антителами рост опухоли усиливается; — в организме развивается общая и местная иммунодепрессия под влиянием выработки опухолевой тканью специфических факторов. Общее содержание лимфоцитов остается в пределах нормы , содержание Т- хелперов, Т-супрессоров, В-лимфоцитов (соответственно и антител классов Ig. M, Ig. G, Ig. E) может быть увеличено. Ниже физиологических нормативов обычно регистрируется общее содержание Т-лимфоцитов, Т-киллеров, а также иммуноглобулинов А и D.
 Основоположником экспериментальной трансплантации жизненно важных органов, в частности сердца, является французский ученый Алексис Каррель , удостоенный за это Нобелевской премии в 1912 г.
Основоположником экспериментальной трансплантации жизненно важных органов, в частности сердца, является французский ученый Алексис Каррель , удостоенный за это Нобелевской премии в 1912 г.
 Виды трансплантатов: — аутотрансплантат — собственная ткань донора, пересаженная ему же; — изотрансплантат — орган или ткань, пересаженные организму того же генотипа; при этом донор и реципиент могут быть однояйцевыми близнецами, а животные — принадлежать одной инбредной линии; — аллотрансплантат (гомотрансплантат) — орган или ткань, пересаженные между представителями одного и того же вида, например, от одного человека к другому (переливание крови, трансплантация органов и тканей); — ксенотрансплантат (гетеротрансплантат) — орган или ткань, пересаженные от представителя одного вида представителю другого вида, например, от животного к человеку. — ортотопическая трансплантация — пересадка органа на место удаленного; — гетеротопическая — пересадка органа на новое, не свойственное ему место.
Виды трансплантатов: — аутотрансплантат — собственная ткань донора, пересаженная ему же; — изотрансплантат — орган или ткань, пересаженные организму того же генотипа; при этом донор и реципиент могут быть однояйцевыми близнецами, а животные — принадлежать одной инбредной линии; — аллотрансплантат (гомотрансплантат) — орган или ткань, пересаженные между представителями одного и того же вида, например, от одного человека к другому (переливание крови, трансплантация органов и тканей); — ксенотрансплантат (гетеротрансплантат) — орган или ткань, пересаженные от представителя одного вида представителю другого вида, например, от животного к человеку. — ортотопическая трансплантация — пересадка органа на место удаленного; — гетеротопическая — пересадка органа на новое, не свойственное ему место.
 Специфичность антигенов, участвующих в реакции отторжения трансплантата, находится под генетическим контролем. Генетически идентичные однояйцевые близнецы имеют одинаковые трансплантационные антигены, и между ними легко осуществляется пересадка тканей. Антигены, вызывающие реакцию отторжения трансплантата, контролируются главным комплексом гистосовместимости. Значительная роль в подборе пары донор — реципиент принадлежит определению специфичности генов в системе HLA.
Специфичность антигенов, участвующих в реакции отторжения трансплантата, находится под генетическим контролем. Генетически идентичные однояйцевые близнецы имеют одинаковые трансплантационные антигены, и между ними легко осуществляется пересадка тканей. Антигены, вызывающие реакцию отторжения трансплантата, контролируются главным комплексом гистосовместимости. Значительная роль в подборе пары донор — реципиент принадлежит определению специфичности генов в системе HLA.
 Информация о фенотипах реципиентов хранится в банке данных, и при наличии необходимого трансплантата по его фенотипу подбирается наиболее подходящий реципиент. В первую очередь Т-лимфоциты реагируют на детерминанты 2 -го класса. Антигены 2 -го класса системы HLA активируют Т-хелперы к пролиферации. Т-хелперы оказывают помощь в генерации цитотоксических Т-лимфоцитов , специфичных к детерминантам гистосовместимости 1 -го класса.
Информация о фенотипах реципиентов хранится в банке данных, и при наличии необходимого трансплантата по его фенотипу подбирается наиболее подходящий реципиент. В первую очередь Т-лимфоциты реагируют на детерминанты 2 -го класса. Антигены 2 -го класса системы HLA активируют Т-хелперы к пролиферации. Т-хелперы оказывают помощь в генерации цитотоксических Т-лимфоцитов , специфичных к детерминантам гистосовместимости 1 -го класса.
 Перед проведением операции трансплантации органов или тканей проводится серия определяющих тестов, дающих ответ на вопрос о приживляемости тканей донора в организме реципиента (определяется взаимоотношение локусов А, В и D в системе главного комплекса гистосовместимости HLA). К основным тестам на совместимость тканей относятся: — реакция лейкоагглютинации; — реакция лимфоцитотоксичности; — РСК с тромбоцитами (тесты, определяющие совместимость по локусам А и В); — смешивание культур лимфоцитов (совместимость по всему локусу D). Совместимость антигенов по всему локусу D является наиболее важной для приживления трансплантата. Меньшее значение имеет совпадение по локусу В, что важнее совпадения по локусу А.
Перед проведением операции трансплантации органов или тканей проводится серия определяющих тестов, дающих ответ на вопрос о приживляемости тканей донора в организме реципиента (определяется взаимоотношение локусов А, В и D в системе главного комплекса гистосовместимости HLA). К основным тестам на совместимость тканей относятся: — реакция лейкоагглютинации; — реакция лимфоцитотоксичности; — РСК с тромбоцитами (тесты, определяющие совместимость по локусам А и В); — смешивание культур лимфоцитов (совместимость по всему локусу D). Совместимость антигенов по всему локусу D является наиболее важной для приживления трансплантата. Меньшее значение имеет совпадение по локусу В, что важнее совпадения по локусу А.
 При подборе пары донор — реципиент необходимыми условиями являются: — соответствие по системе крови АВО; — соответствие крови по Rh-фактору; — учет возможного образования антител в организме реципиента (например, при предшествующей трансплантации беременности или переливании крови). Отторжение предотвращается: — антимитотическими препаратами; — противовоспалительными стероидами; — антилимфоцитарным глобулином, который вызывает общую иммунодепрессию; — иммунодепрессанты (например, циклоспорина А), имеющие большую избирательность действия и способные вызвать антигенспецифическую супрессию.
При подборе пары донор — реципиент необходимыми условиями являются: — соответствие по системе крови АВО; — соответствие крови по Rh-фактору; — учет возможного образования антител в организме реципиента (например, при предшествующей трансплантации беременности или переливании крови). Отторжение предотвращается: — антимитотическими препаратами; — противовоспалительными стероидами; — антилимфоцитарным глобулином, который вызывает общую иммунодепрессию; — иммунодепрессанты (например, циклоспорина А), имеющие большую избирательность действия и способные вызвать антигенспецифическую супрессию.
 Реакция проявляется при наличии у реципиента хотя бы одного антигена, который отсутствует у донора или проведении трансплантации больным в состоянии иммунодепресии костного мозга. Сверхострая реакция развивается на 7— 14 -й день; Острая — на 20— 50 -й день; Хроническая — на 100— 500 -й день. Реакция включает в себя 2 фазы: — пролиферации; — цитолитическая.
Реакция проявляется при наличии у реципиента хотя бы одного антигена, который отсутствует у донора или проведении трансплантации больным в состоянии иммунодепресии костного мозга. Сверхострая реакция развивается на 7— 14 -й день; Острая — на 20— 50 -й день; Хроническая — на 100— 500 -й день. Реакция включает в себя 2 фазы: — пролиферации; — цитолитическая.
 Фаза пролиферации заключается в приживлении лимфоцитов трансплантата в организме реципиента. Иммунокомпетентные клетки трансплантата получают возможность реагировать на антигены реципиента. Если животным сделана трансплантация Т-лимфоцитов в раннем возрасте, то у них наблюдаются задержка роста (карликовость), увеличение селезенки, гемолитическая анемия вследствие образования антител к эритроцитам. При аналогичной трансплантации у человека обнаруживается иммуноагрессия активированных Т-клеток против лимфопоэтической и гемопоэтической систем хозяина. Появляются лихорадка, анемия, потеря веса, сыпь, диарея, увеличение селезенки. Если присутствуют различия по локусам 2 -го класса HLA , то реакция «трансплантат против хозяина» может вызвать гибель реципиента за счет дальнейших внутриклеточных нарушений. В цитолитическую фазу наступает некроз тканей различных органов, включая кожу, слизистые оболочки, печень, костный мозг, легкие.
Фаза пролиферации заключается в приживлении лимфоцитов трансплантата в организме реципиента. Иммунокомпетентные клетки трансплантата получают возможность реагировать на антигены реципиента. Если животным сделана трансплантация Т-лимфоцитов в раннем возрасте, то у них наблюдаются задержка роста (карликовость), увеличение селезенки, гемолитическая анемия вследствие образования антител к эритроцитам. При аналогичной трансплантации у человека обнаруживается иммуноагрессия активированных Т-клеток против лимфопоэтической и гемопоэтической систем хозяина. Появляются лихорадка, анемия, потеря веса, сыпь, диарея, увеличение селезенки. Если присутствуют различия по локусам 2 -го класса HLA , то реакция «трансплантат против хозяина» может вызвать гибель реципиента за счет дальнейших внутриклеточных нарушений. В цитолитическую фазу наступает некроз тканей различных органов, включая кожу, слизистые оболочки, печень, костный мозг, легкие.
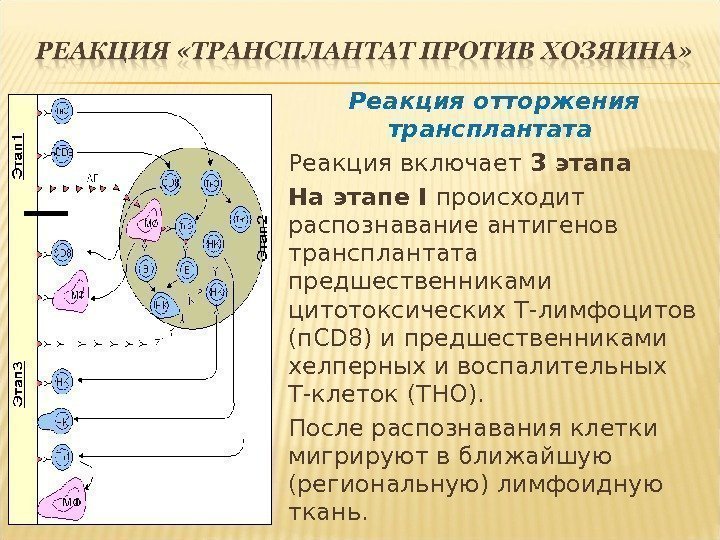
 Реакция отторжения трансплантата Реакция включает 3 этапа На этапе I происходит распознавание антигенов трансплантата предшественниками цитотоксических Т-лимфоцитов (п. CD 8) и предшественниками хелперных и воспалительных Т-клеток (ТНО). После распознавания клетки мигрируют в ближайшую (региональную) лимфоидную ткань.
Реакция отторжения трансплантата Реакция включает 3 этапа На этапе I происходит распознавание антигенов трансплантата предшественниками цитотоксических Т-лимфоцитов (п. CD 8) и предшественниками хелперных и воспалительных Т-клеток (ТНО). После распознавания клетки мигрируют в ближайшую (региональную) лимфоидную ткань.
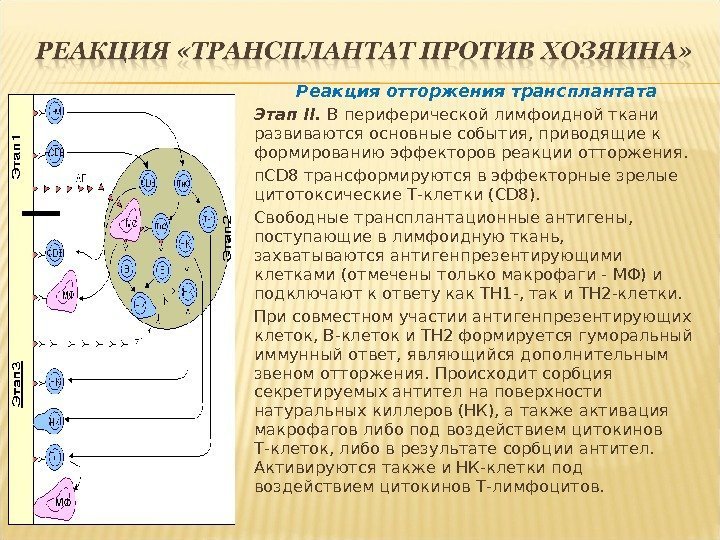
 Реакция отторжения трансплантата Этап II. В периферической лимфоидной ткани развиваются основные события, приводящие к формированию эффекторов реакции отторжения. п. CD 8 трансформируются в эффекторные зрелые цитотоксические Т-клетки (CD 8). Свободные трансплантационные антигены, поступающие в лимфоидную ткань, захватываются антигенпрезентирующими клетками (отмечены только макрофаги — МФ) и подключают к ответу как ТН 1 -, так и ТН 2 -клетки. При совместном участии антигенпрезентирующих клеток, В-клеток и ТН 2 формируется гуморальный иммунный ответ, являющийся дополнительным звеном отторжения. Происходит сорбция секретируемых антител на поверхности натуральных киллеров (НК), а также активация макрофагов либо под воздействием цитокинов Т-клеток, либо в результате сорбции антител. Активируются также и НК-клетки под воздействием цитокинов Т-лимфоцитов.
Реакция отторжения трансплантата Этап II. В периферической лимфоидной ткани развиваются основные события, приводящие к формированию эффекторов реакции отторжения. п. CD 8 трансформируются в эффекторные зрелые цитотоксические Т-клетки (CD 8). Свободные трансплантационные антигены, поступающие в лимфоидную ткань, захватываются антигенпрезентирующими клетками (отмечены только макрофаги — МФ) и подключают к ответу как ТН 1 -, так и ТН 2 -клетки. При совместном участии антигенпрезентирующих клеток, В-клеток и ТН 2 формируется гуморальный иммунный ответ, являющийся дополнительным звеном отторжения. Происходит сорбция секретируемых антител на поверхности натуральных киллеров (НК), а также активация макрофагов либо под воздействием цитокинов Т-клеток, либо в результате сорбции антител. Активируются также и НК-клетки под воздействием цитокинов Т-лимфоцитов.
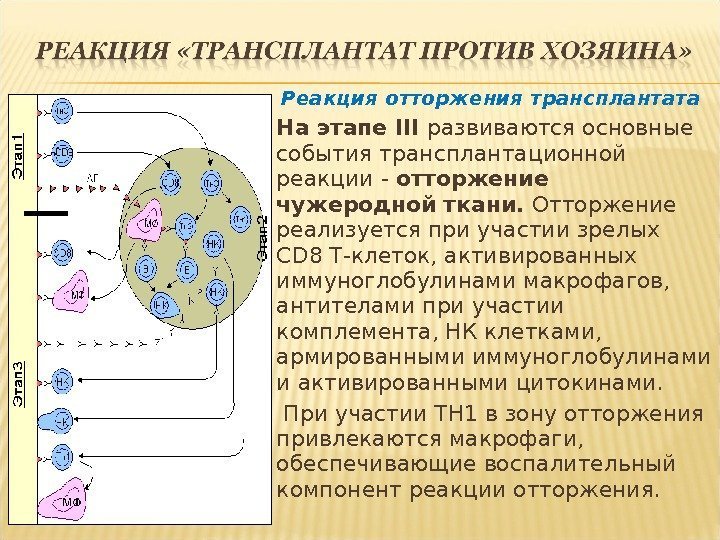
 Реакция отторжения трансплантата На этапе III развиваются основные события трансплантационной реакции — отторжение чужеродной ткани. Отторжение реализуется при участии зрелых CD 8 Т-клеток, активированных иммуноглобулинами макрофагов, антителами при участии комплемента, НК клетками, армированными иммуноглобулинами и активированными цитокинами. При участии ТН 1 в зону отторжения привлекаются макрофаги, обеспечивающие воспалительный компонент реакции отторжения.
Реакция отторжения трансплантата На этапе III развиваются основные события трансплантационной реакции — отторжение чужеродной ткани. Отторжение реализуется при участии зрелых CD 8 Т-клеток, активированных иммуноглобулинами макрофагов, антителами при участии комплемента, НК клетками, армированными иммуноглобулинами и активированными цитокинами. При участии ТН 1 в зону отторжения привлекаются макрофаги, обеспечивающие воспалительный компонент реакции отторжения.
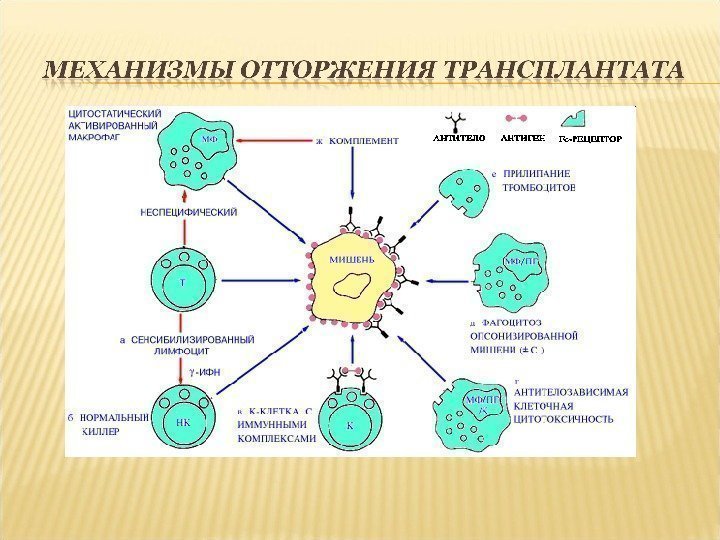
 Ведущая роль в первичной реакции отторжения принадлежит лимфоидным клеткам (Т-лимфоцитам). Т-хелперы привлекают цитотоксические Т-лимфоциты к клеткам-мишеням и образуют лимфокины, вызывающие реакцию гиперчувствительности замедленного типа.
Ведущая роль в первичной реакции отторжения принадлежит лимфоидным клеткам (Т-лимфоцитам). Т-хелперы привлекают цитотоксические Т-лимфоциты к клеткам-мишеням и образуют лимфокины, вызывающие реакцию гиперчувствительности замедленного типа.
 Роль гуморальных антител зависит от структуры трансплантируемого органа или ткани. Антитела могут разрушать лимфоциты , принадлежащие донору, оказывая на них цитотоксическое действие. Цитотоксические антитела вырабатываются к антигенам клеточных мембран , они реагируют с лимфоцитами в присутствии системы комплемента и вызывают цитолиз. В основе острой и сверхострой реакции отторжения трансплантата лежит реакция преципитации (антигены трансплантата соединяются с антителами реципиента), результатом которой являются тромбоз сосудов, нарушение кровоснабжения и некроз тканей.
Роль гуморальных антител зависит от структуры трансплантируемого органа или ткани. Антитела могут разрушать лимфоциты , принадлежащие донору, оказывая на них цитотоксическое действие. Цитотоксические антитела вырабатываются к антигенам клеточных мембран , они реагируют с лимфоцитами в присутствии системы комплемента и вызывают цитолиз. В основе острой и сверхострой реакции отторжения трансплантата лежит реакция преципитации (антигены трансплантата соединяются с антителами реципиента), результатом которой являются тромбоз сосудов, нарушение кровоснабжения и некроз тканей.
 Трансплантаты, не содержащие сосудов, приживаются без иммунодепрессии (роговица, хрящ). Отторжение трансплантата можно предотвращать с помощью агентов , не специфически подавляющих иммунный ответ. Метод интракорпорального облучение крови вызывает образование лимфоцитов, лишенных маркеров Т- и В-популяций и макрофагов , подавляющих цитолитические иммунные реакции и стимулирующих образование супрессоров. После операции трансплантации органов и тканей используются иммунодепрессанты, подавляющие Т-клеточные реакции, синтез лимфокинов и ход иммунных реакций.
Трансплантаты, не содержащие сосудов, приживаются без иммунодепрессии (роговица, хрящ). Отторжение трансплантата можно предотвращать с помощью агентов , не специфически подавляющих иммунный ответ. Метод интракорпорального облучение крови вызывает образование лимфоцитов, лишенных маркеров Т- и В-популяций и макрофагов , подавляющих цитолитические иммунные реакции и стимулирующих образование супрессоров. После операции трансплантации органов и тканей используются иммунодепрессанты, подавляющие Т-клеточные реакции, синтез лимфокинов и ход иммунных реакций.


