Химия белков.ppt
- Количество слайдов: 77

БИОХИМИЯ БЕЛКОВ

БЕЛКИ • высокомолекулярные азотсодержащие органические вещества, молекулы которых построены из остатков аминокислот, соединенных пептидной связью • являются молекулярными инструментами для реализации генетической информации • составляют основу и структуры и функции живых организмов

Все белки содержат: • • • углерод (50, 6 – 54, 5%) кислород (21, 5 – 23, 5%) азот (15, 0 – 17, 6%) водород (6, % - 7, 3%) серу (0, 3 – 2, 5%) Сложные белки могут включать в себя и другие элементы.

Размеры белков зависят от количества аминокислотных остатков • • небольшие - 50 -150 средние - несколько сотен крупные - свыше тысячи олигомеры - несколько тысяч

Функции белков • • • пластическая каталитическая регуляторная защитная транспортная дыхательная энергетическая сократительная гормональная питательная (резервная)

Методы выделения и очистки • гомогенизация биологического материала • экстракция • фракционирование и очистка - высаливание - хроматография (абсорбционная, распределительная, ионообменная, аффинная, гельхроматография) - электрофорез - кристаллизация - распределение в двухфазных системах

Классификация аминокислот современная рациональная классификация основана на характере боковой цепи (R-групп) R H-C-NH 2 COOH • неполярные (гидрофобные) • полярные (гидрофильные) • нейтральные: кислые или отрицательно заряженные основные или положительно заряженные • циклические • ациклические

По наличию определенных структур в радикалах • • серосодержащие ароматические гидрооксиаминокислоты иминокислоты
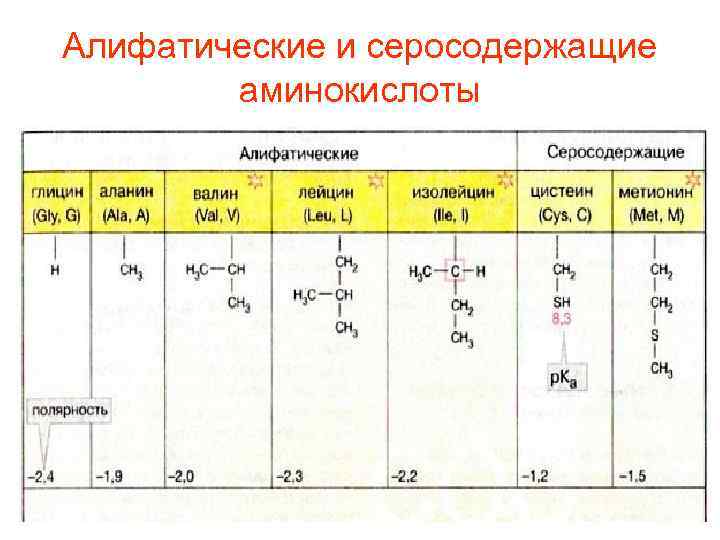
Алифатические и серосодержащие аминокислоты
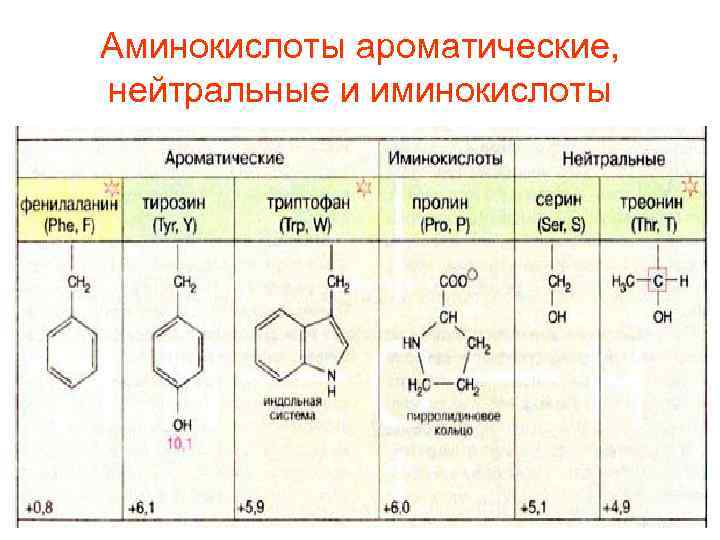
Аминокислоты ароматические, нейтральные и иминокислоты

Нейтральные, кислые и основные аминокислоты

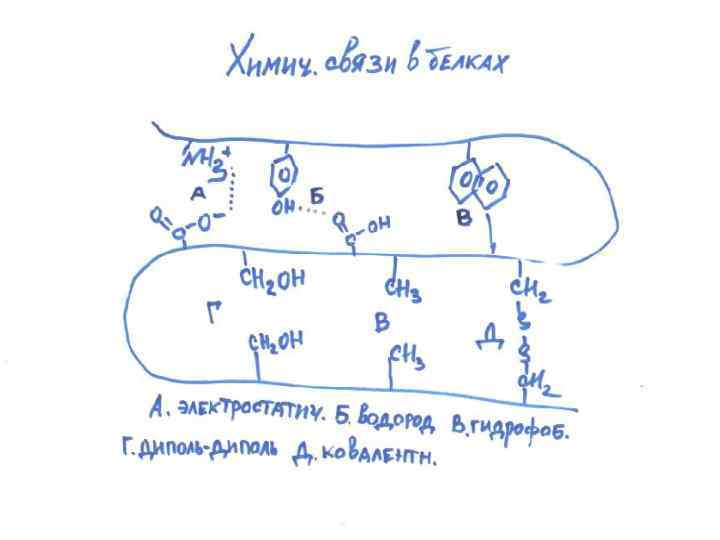
Связи • • • пептидные водородные дисульфидные солеобразные (ионные) гидрофобные взаимодействия
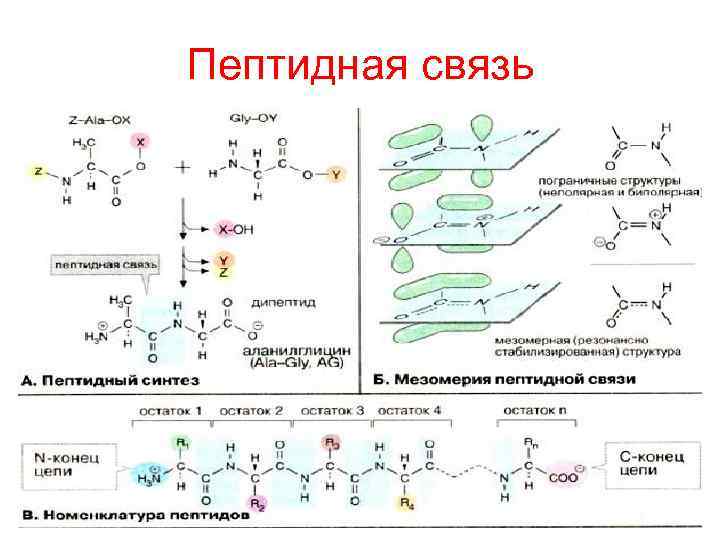
Пептидная связь

Физиологические эффекты пептидов • Антиоксиданты (глютатион, карнозин) • Обезболивающие(энкефалины и эндорфины) • Регулирующие(тонус сосудов, аппетит, пищеварение, рост) • Гормональные(окситоцин, вазопрессин) • Антибиотики( грамицидин, циклоспорин)

Пептиды Это низкомолекулярные полимеры, построенные из аминокислот, соединенных пептидной связью, содержат от 2 -х аминокислот до 4 -х десятков аминокислотных остатков. Конец полипептидной цепи, содержащий свободную аминогруппу – N-конец, другой конец со свободной карбоксильной группой – С-конец

Структура белков • • первичная вторичная третичная четвертичная

Первичная структура уникальная последовательность аминокислотных возникающей при взаимодействии остатков в полипептидных цепях, формирующаяся с помощью пептидной связи, карбоксильной и аминогрупп
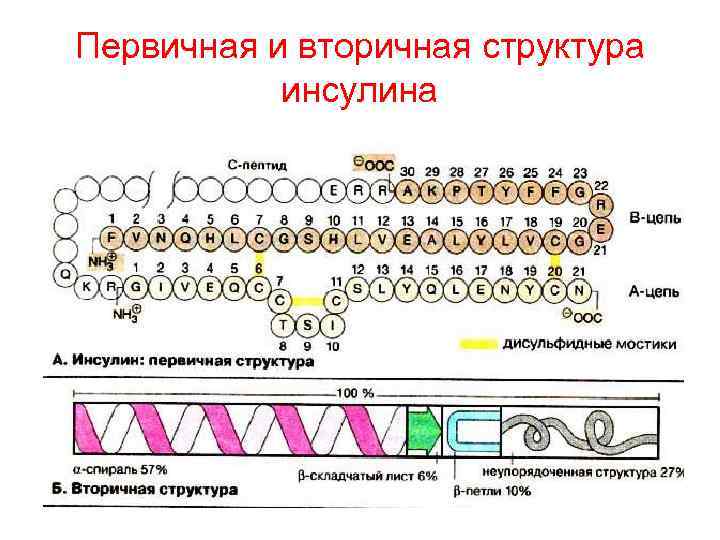
Первичная и вторичная структура инсулина

Вторичная структура • α – спираль • β – структура (складчатый лист) Формируются они с помощью водородных связей, возникающих между С=О и N-H
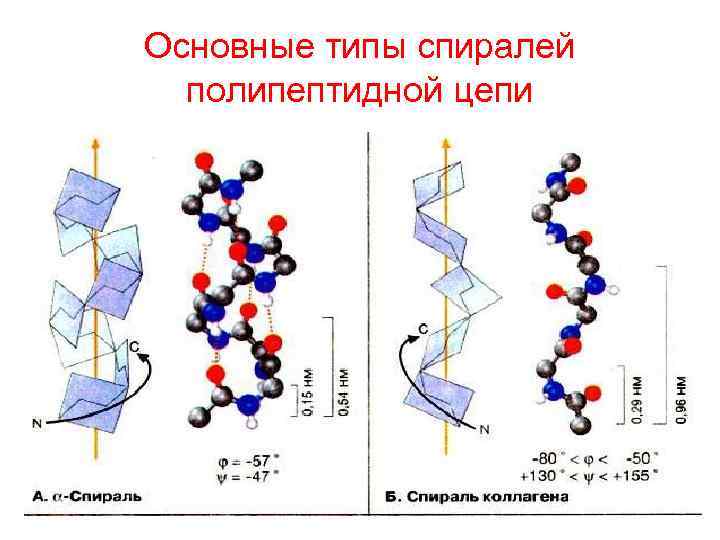
Основные типы спиралей полипептидной цепи
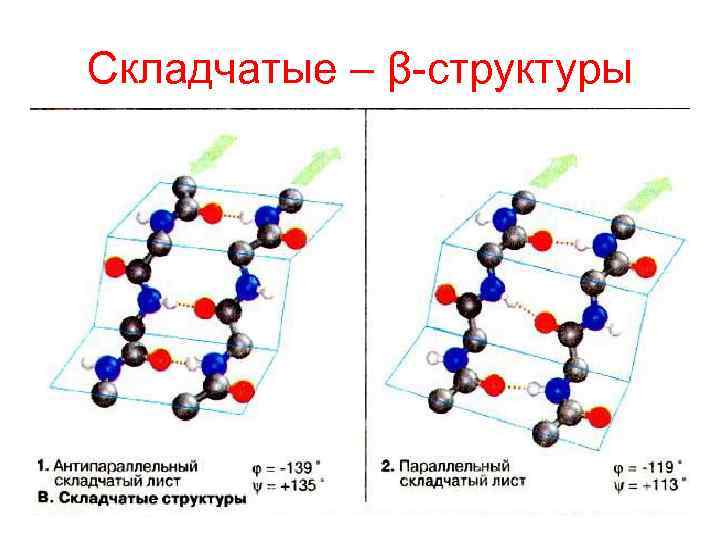
Складчатые – β-структуры

Третичная структура пространственная организация молекул белков, формируется при участии связей: • пептидных • водородных • ионных или электровалентных • гидрофобных Стабилизируется третичная структура дисульфидными связями
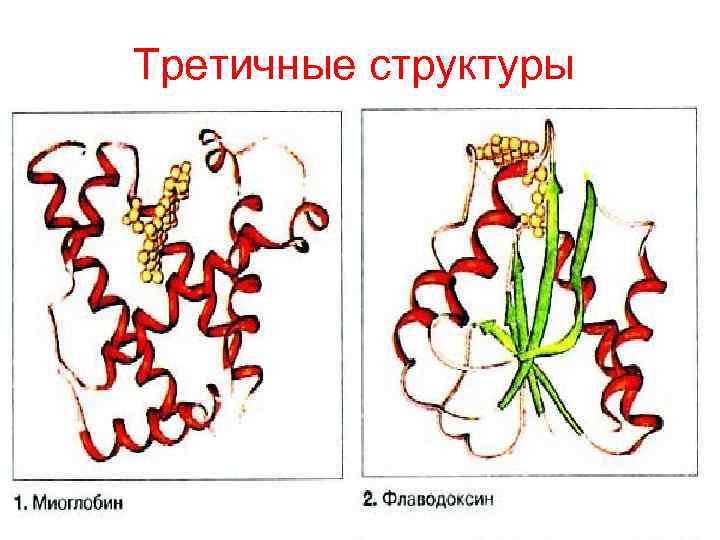
Третичные структуры

Четвертичная структура Это агрегация мономерных белковых субъединиц с образованием функционально активной структуры. Формируется при участии связей водородных, ионных, дисульфидных, а также гидрофобных взаимодействий.
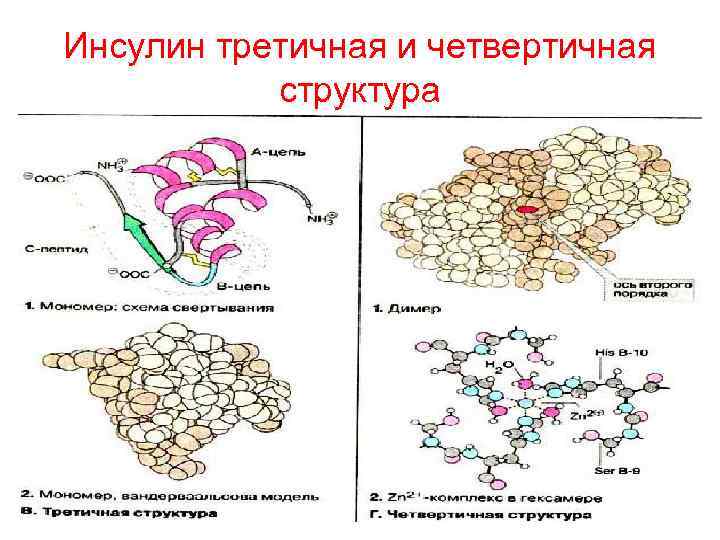
Инсулин третичная и четвертичная структура
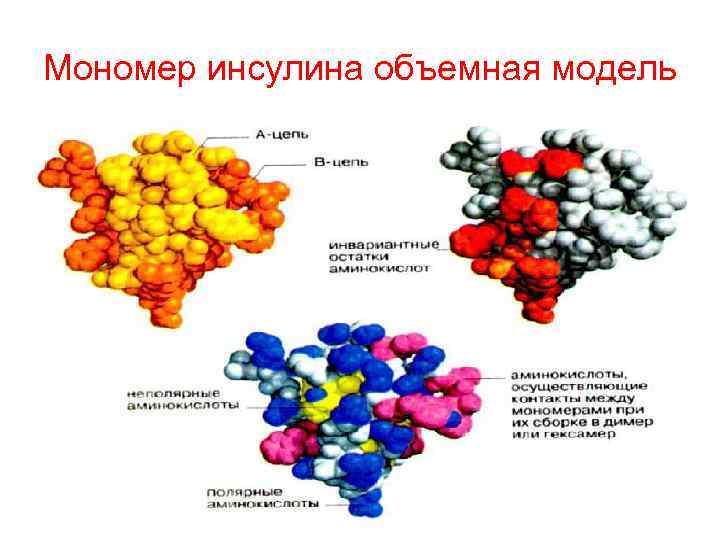
Мономер инсулина объемная модель

Форма молекул белков • фибриллярные (длинная ось молекулы во много раз превышает ось поперечную) • глобулярные (сферические или эллипсоидные)

Фибриллярные белки • белки α-кератиновой структуры (кератин волос и шерсти, фибрин), их полипептидные цепи в виде α–спирали образуют структуру типа многожильного кабеля, при этом формируется суперспираль • белки β–кератиновой структуры (фиброин шелка и паутины) вытянутые полипептидные цепи, соединенные водородными связями, образуют слоистую структуру

Белки коллагенового типа Их три спирализованные полипептидные цепи (спирализация отлична от α спирали) образуют канатовидный пучок. Структура стабилизирована водородными связями.
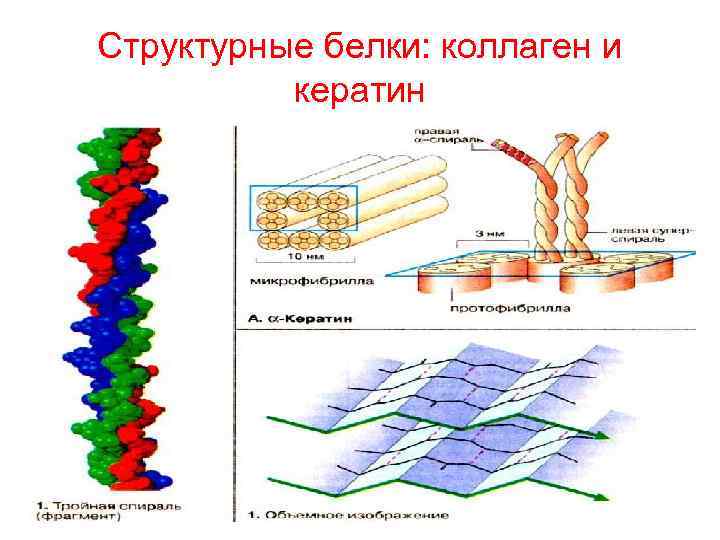
Структурные белки: коллаген и кератин

Общие свойства аминокислот • кислотно-основные, проявляющиеся при растворении в воде • оптическая активность правовращающие «+» (Ала, Иле, Глу, Лиз и др. ) левовращающие «-» (Фен, Трп, Лей и др)
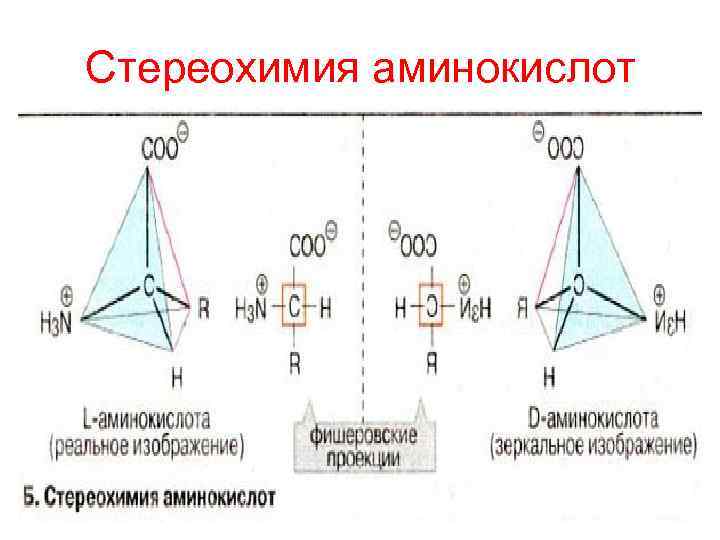
Стереохимия аминокислот

Денатурация белков Нарушение общего плана уникальной структуры нативной молекулы белка, преимущественно ее третичной структуры, приводящих к потери характерных для нее свойств (растворимость, электрофоретическая подвижность, биологическая активность и др. ). Большинство белков денатурирует при нагревании их растворов выше 50 -60 о С

Содержание белков в тканях (от сухой массы) • • Мышцы Почки Сердце Кожа Зубы Жировая ткань Все тело Печень 80 %: 72 60 63 18 14 45 57


ЭЛАСТИН • Основной белок эластических веществ • Отличается от коллагена по составу и структуре (больше валина, аланина, меньше аргинина) • Как и в коллагене много глицина и пролина, мало метионина, нет совсем триптофана и цистеина • Только у эластина обнаружен десмозин, который сообщает ему эластичность во всех направлениях • Синтезируется сначала тропоэластин – предшественник, без поперечных связей

Альбумины и глобулины • Широко распространены (кровь, молоко, яйца, мышцы) • Много (7% в составе крови) • Альбумины – масса - 40 -70 тыс. , глобулины – 150 тыс. и более • Кислый характер их растворов • Отрицательный заряд молекул • Функции: осмос крови, транспорт других веществ (липидов, железа, меди), иммунитет (антитела)

ПРОТАМИНЫ И ГИСТОНЫ • • Небольшая молекулярная масса Выраженные основные свойства Хорошая растворимость в воде Много лизина и аргинина в составе Много в ядерном материале Источники – икра рыб и проч. Представители – сальмин (из семги).

Природные пептиды • Гормональная активность (окситоцин, глюкагон, вазопрессин и др. ) • Пишеварение (гастрин, секретин) • Пептиды крови (брадикинин, ангиотензин, каллидин) • Нейропептиды (пептид сна, эндорфины) Часто синтезируются сначала как неактивные предшественники. • Искусственный пептид – аспартам – заменитель сахара

КОЛЛАГЕН • • • Пример нерастворимого белка Много (6% массы тела, 30% общего белка) Крупный (виден в микроскоп) Фибриллярен ( 1: 20) Из многих волокон, структурная единица – тропоколлаген (289 тыс. ) • Треть аминокислот – глицин, еще треть – пролин, много гидроксилизина • Внеклеточный белок • Содержится: кожа, кости, роговица, сосуды, стекловидное тело
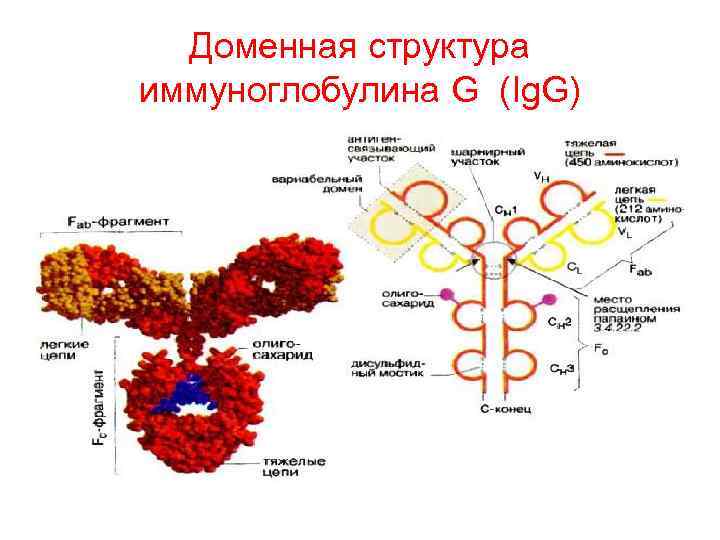
Доменная структура иммуноглобулина G (Ig. G)

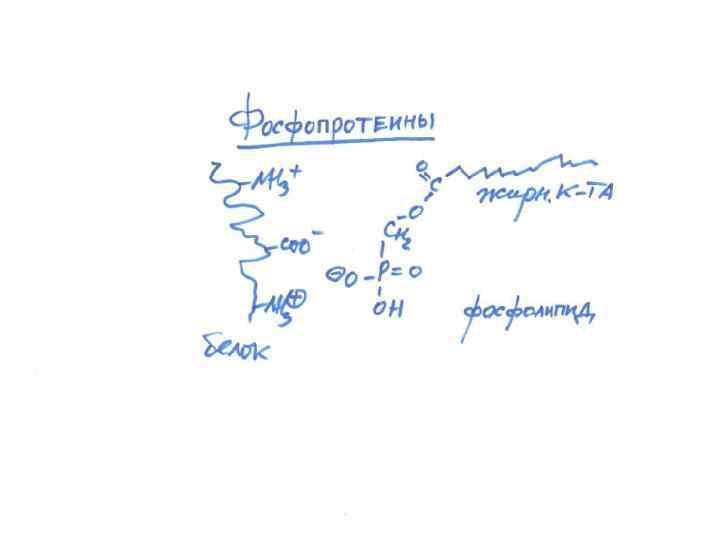
СЛОЖНЫЕ БЕЛКИ • • • Липопротеины Гликопротеины Фосфопротеины Металлопротеины Нуклеопротеины Хромопротеины

МЕТАЛЛОПРОТЕИНЫ • Белки с негемовым железом (феритин, трансферитин, гемосидерин). Содержание железа соответственно 20%, 43% и 30% соответственно. Трансферин одновременно и металло- и гликопротеин сыворотки крови. Гемосидерин – металло-, нуклео- и гликопротеин. • Металлоферменты (цитохромоксидаза – медь, аргиназа, декарбоксилазы – марганец, пептидазы, фосфатазы – магний, кальций, пероксидаза железо

МЕТАЛЛОПРОТЕИНЫ • Феритин – в селезенке, печени, мозге. Масса 400 тыс. , содержит 20% железа, белковая часть – апоферитин, водорастворим, депо железа • Трасферин – белок крови, глобулин, гликопротеин, 0, 13% железа, водорастворим • Гемосидерин – в печени, селезенке, масса 400 тыс. , содержит 37% железа, нерастворим. Накапливается в тканях (гемахроматоз) – причина цирроза, диабета, сердечной недостаточности. Лечат кровопусканием, связыванием железа (фарм. )

• Металлоферменты – там металл не временный, не адсорбированный, не отщепляется при выделении. Без металла – нет каталитической функции • Марганец – в аргиназе, декарбоксилазах, фосфотрансферазах • Магний, кальций, цинк – пептидазы, фосфотазы • Калий, натрий, магний – Атфаза, фосфокиназа (транспорт фосфатных групп) • Кобальт - трансферазы

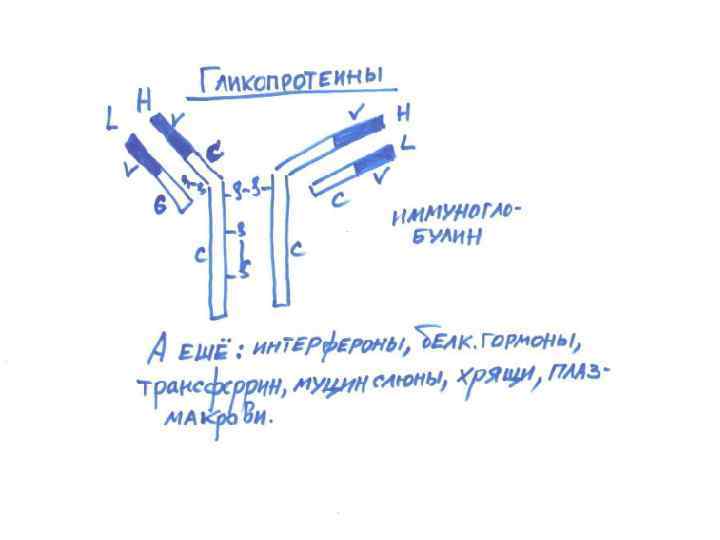
ГЛИКОПРОТЕИНЫ • Имеют отношение к развитию рака, артритов, астмы, иммунодефицита … • Сложно и неоднотипно построены. Часто включают еще и аминосахара, и серную кислоту • Разновидности: иммуноглобулины, гормоны, мембранные белки, интерфероны, белки крови, молока, рецепторные, некоторые ферменты, муцин слюны, овомукоид, гликопротеины хрящей и костной ткани • Углеводные компоненты (галактоза, фукоза, манноза, ксилоза) • Синтезируются на рибосомах, гликозилируются, затем в аппарат Гольджи и транспорт к месту назначения

ГЛИКОПРОТЕИНЫ И ПРОТЕОПЛИКАНЫ • Белка от 5% до 95% • Иммуноглобулины, интерфероны, гормоны, ферменты, структурные белки • Кроме того: формируют тургор тканей, межклеточные фильтры (препятствуют распространению микробов), рессорная функция (в хрящах), прозрачность роговицы, стекловидного тела, антикоагуляция (гепарин), рецепторы и другие функции

О БЕЛКАХ ПЛАЗМЫ КРОВИ • Кроме альбумина почти все белки плазмы крови являются гликопротеинами. Они включают олигосахариды • Концентрация белков плазмы в норме поддерживается на постоянном уровне • При заболеваниях органов меняется концентрация этих белков. Например, повреждение тканей цитокинами увеличивает образование белков острой фазы, в частности С-реактивного белка, гаптоглобина, фибриногена
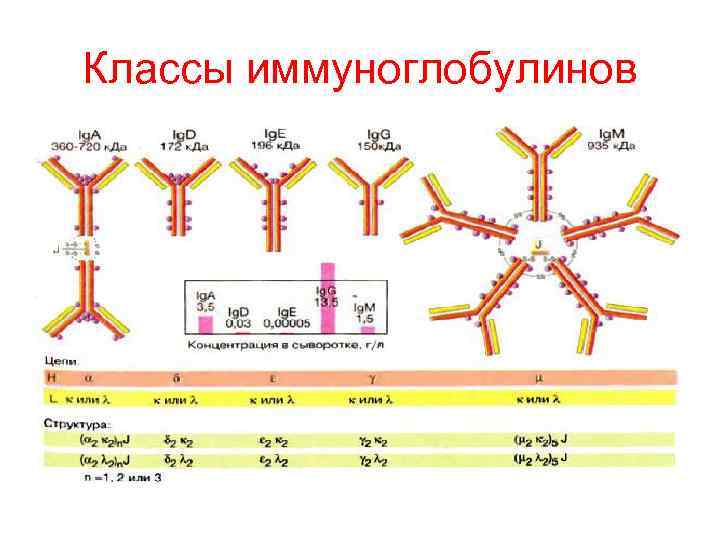
Классы иммуноглобулинов

КЛАССЫ ИММУНОГЛОБУЛИНОВ • Иммуноглобулины всех 5 классов являются секретируемыми белками. Антитела имеют различные функции. • Иммуноглобулины М образуются первыми при контакте с чужеродным антигеном. Эти антитела особенно активны против микроорганизмов. • Иммуноглобулинов G (джи) в количественном отношении больше всех. Они могут переходить в плаценту, т. Е. от матери к плоду.

• Иммуноглобулины А обнаруживаются преимущественно в кишечном тракта и секретах • Иммуноглобулины Е присутствуют в плазме здорового человека лишь в незначительных концентрациях и возрастают при аллергичесих реакциях и паразитарных инфекциях • Иммуноглобулинов Д очень мало, функция их не выяснена

ЛИПОПРОТЕИНЫ • Состав: белок и простетическая группа (жир, жирные кислоты, фосфолипиды, холестериды) • Распространение: растения, ткани челевека, кровь, молоко, белок яиц, структура митохондрий, микросом, ядер, сетчатка • Структура: гидрофобное липидное ядро и оболочка из белков • Место синтеза: печень и слизистая кишечника • Основные группы: хиломикроны, липопротеины крови (ЛПОНП, ЛПВП). Чем больше белка, тем выше плотность фракции) • Часто включают и углевод (глюкозу, галактозу, гексозамин, фукозу) • Участвуют в развитии склероза и др. патологии

СОСТАВ ЛИПОПРОИНОВЫХ КОМПЛЕКСОВ • Это шаровидные агрегаты, состоящие из ядра (неполярные липиды, ацилхолестерин) и оболочки толщиной 2 нм. Наружняя сторона оболочки полярна и потому липопротеин растворим. • Комплексы делятся на 5 групп: - хиломикроны – самые легкие и крупныеобеспечивают транспорт пищевых липидов от кишечника к тканям. Разрушаются липазой мышц и жировой ткани.

• Липопротеиды очень низкой плотности, липопротеиды промежуточной плотности и липопротеиды низкой плотности транспортируют жиры, холестерин и фосфолипиды от печени к тканям • Различие плотности в этих группах объясняется разным соотношением белка и липидов: чем выше содержание белка, тем выше плотность этой группы. • Липопротеиды высокой плотности возвращают избыточный холестерин, образующийся в тканях, обратно в печень. В процессе транспорта холестерин ацилируется жирными кислотами

НУКЛЕОПРОТЕИНЫ • Именно с белками и нуклеиновыми кислотами связано многообразие форм жизни • С ними связаны митоз, эмбриональный рост, злокачественный рост, функции ферментов и другие • Широкий диапазон соотношений нуклеинового компонента и белка (от 2% до 65% нуклеиновой кислоты) • Белковый компонент: гистоны(много лизина, аргинина, глицина), негистоновые белки • Всегда положительный заряд • Конкретные представители: хромосома, рибосома, ферменты (ЛДГ, дегидрогеназы), вирусы
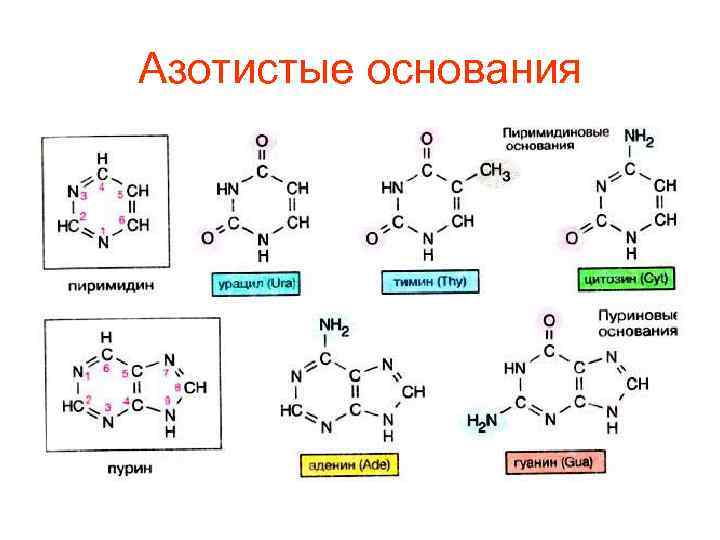
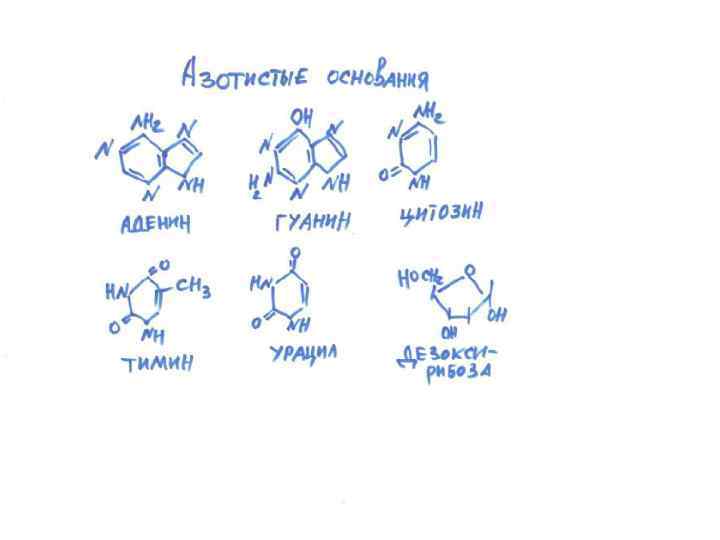
Азотистые основания
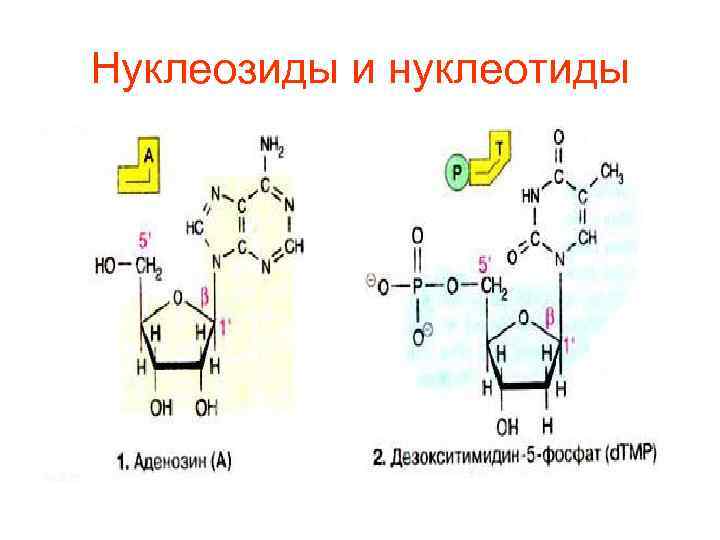
Нуклеозиды и нуклеотиды
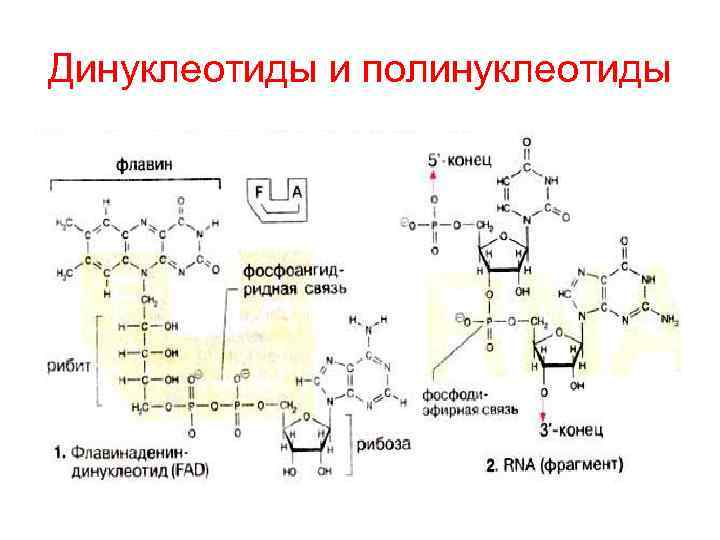
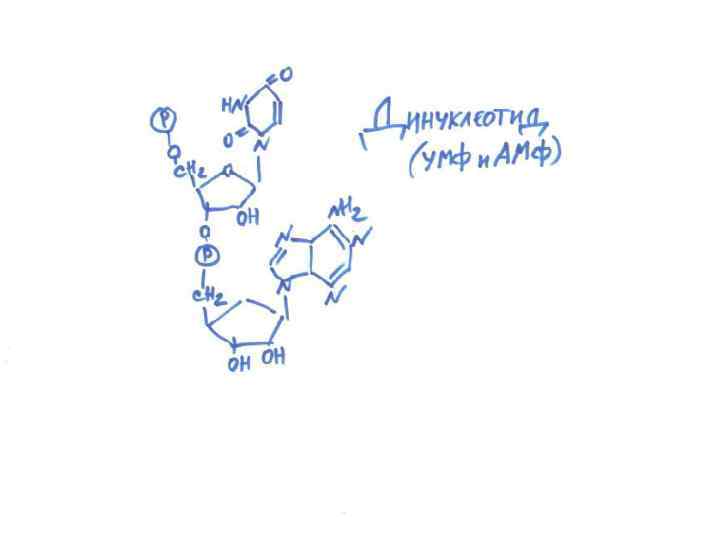
Динуклеотиды и полинуклеотиды
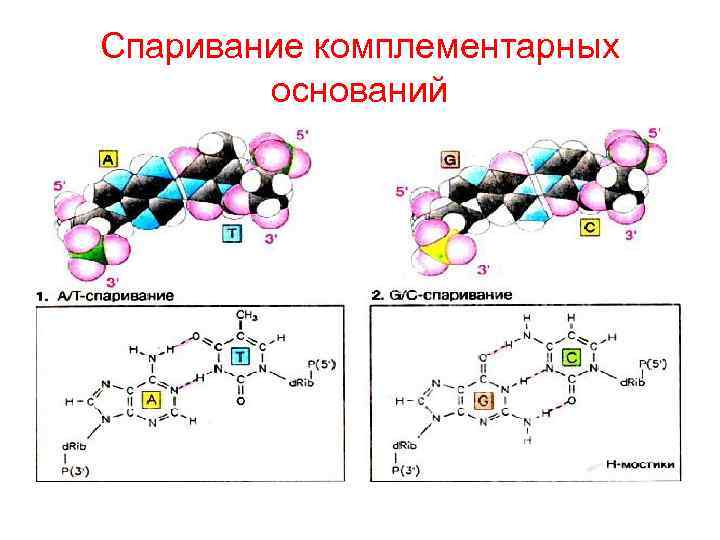
Спаривание комплементарных оснований
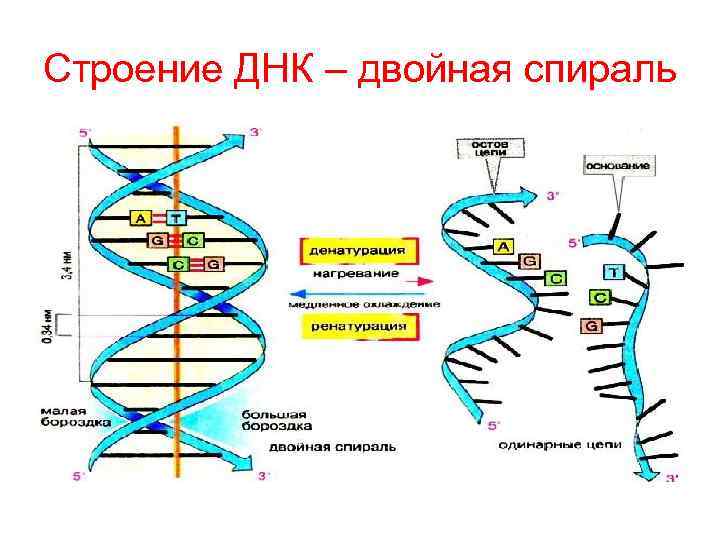
Строение ДНК – двойная спираль
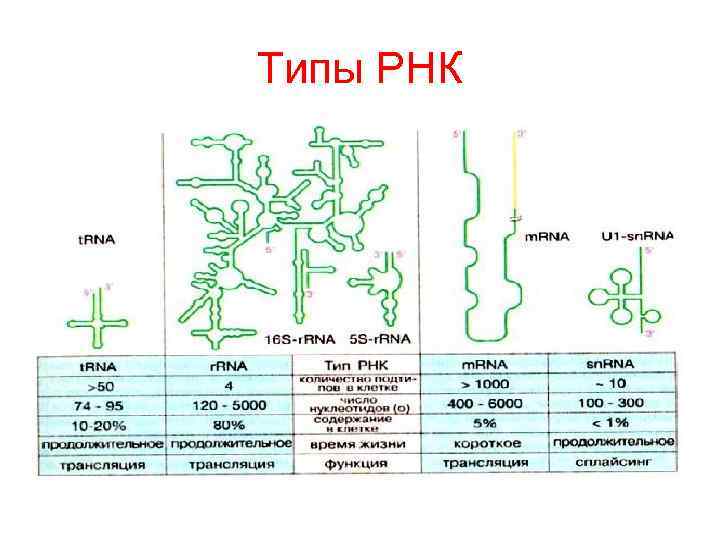
Типы РНК
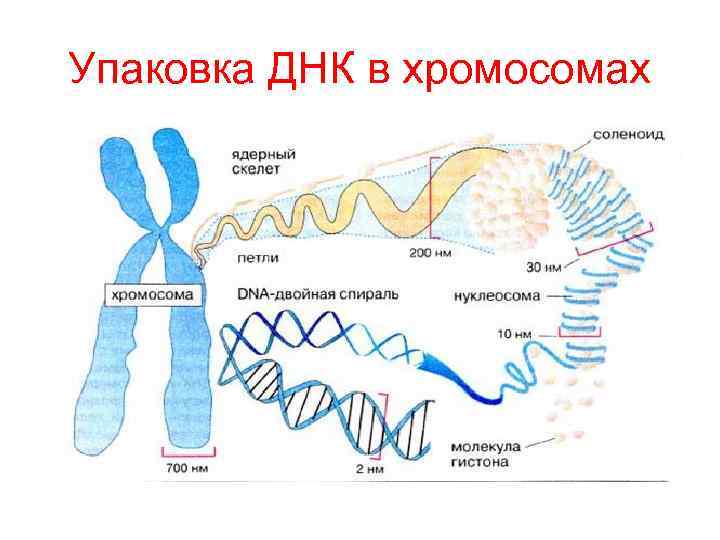
Упаковка ДНК в хромосомах
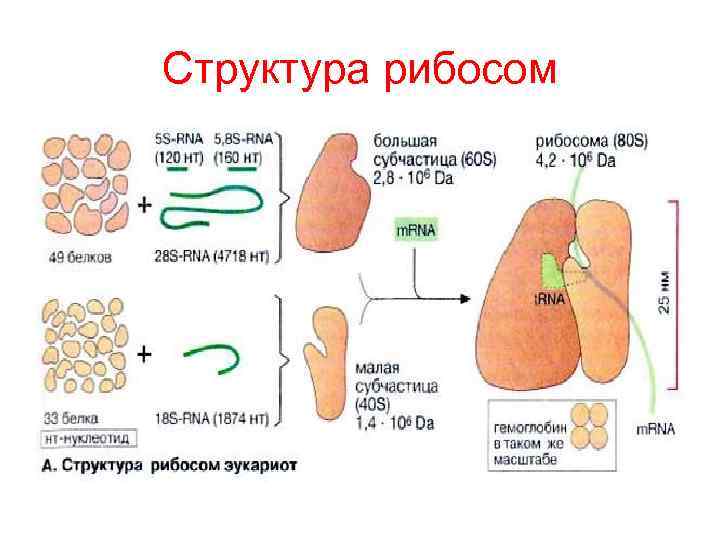
Структура рибосом
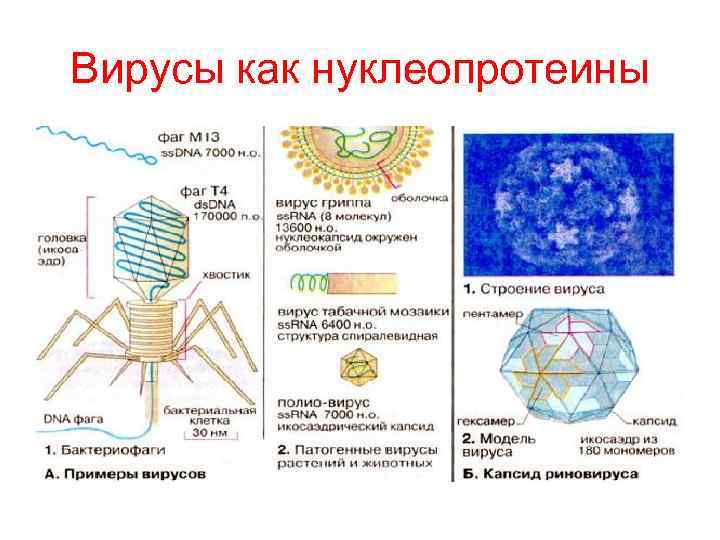
Вирусы как нуклеопротеины

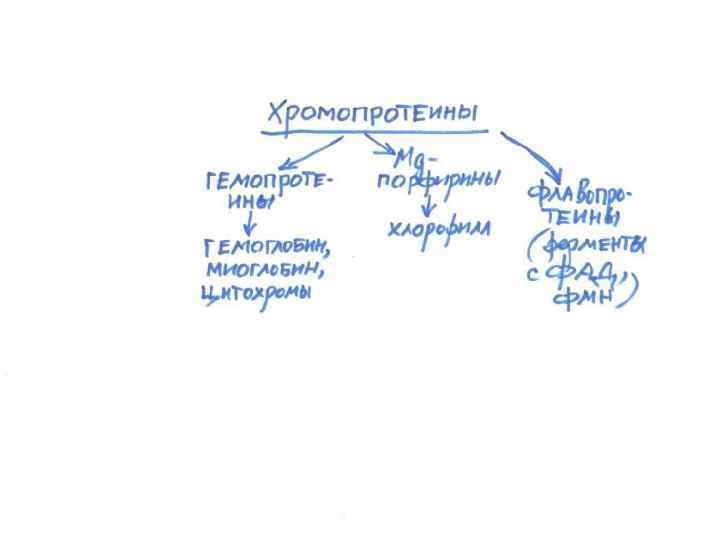
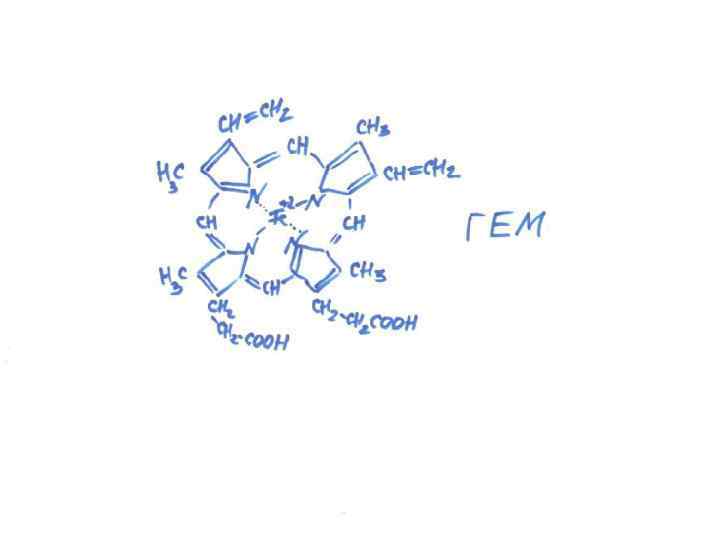
ХРОМОПРОТЕИНЫ окрашенные белки • Гемопротеины (гем, железо) – гемоглобин, каталаза, пероксидаза, миоглобин • Магнийпорфирины – хлорофилл, растения берут лишь 1% энергии падающего света • Флавопротеины, входят в состав оксиредуктаз, участвуют в биоэнергетике, входят в состав ФАД, ФМН

Реакции определения аминокислот и белков реакция Ксантопротеиновая реактив Кислота HNO 3 на что? Фенилалан Тирозин окраска Желтая
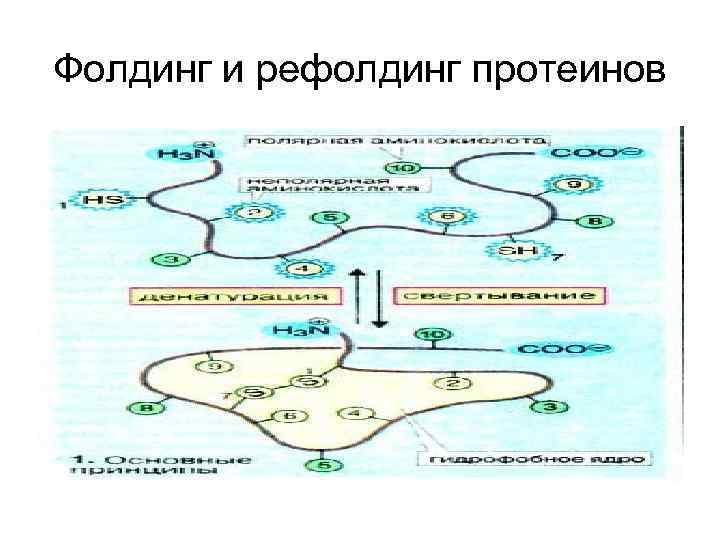
Фолдинг и рефолдинг протеинов

Заболевания, связанные с незаменимыми аминокислотами • Гистидин – анемия, дерматиты, снижение умственных способностей • Изолейцин- поражение почек, анемия, функции щитовидной железы • Лейцин – сходные патологии • Лизин – анемия, миодистрофия, остеопороз • Аргинин – снижение сперматогенеза

• Метионин – ожирение, некрозы, облысения, атеросклероз, анемия (то же для цистеина) • Фенилаланин и тирозин – нарушение функции щитовидной железы и надпочечников • Триптофан – катаракта, помутнение роговицы. Облысение, анемия, атрофия семенников • Валин – нарушение координации движения

Химия белков.ppt