БЕЛКИ

l l Белки, или протеины, – важнейший класс биологически активных веществ (БАВ) Они играют ключевую роль в клетке, присутствуют в виде главных компонентов в любых формах живой материи Без белков невозможно представить себе жизнь «Жизнь есть способ существования белковых тел» (Ф. Энгельс) Ф. Энгельс

Белки… l Биополимеры, которые при гидролизе дают набор -аминокислот L-ряда

Особенности белков 1. Разнообразие структур и высокая видовая специфичность 2. Способность к различным внутримолекулярным взаимодействиям, обеспечивающим динамичность структур молекул 3. Способность вступать в разнообразные химические и физические взаимодействия как друг с другом, так и с другими соединениями (липидами, нуклеиновыми кислотами, полисахаридами и др. ), образуя надмолекулярные комплексы 4. Способность под влиянием воздействий обратимо и закономерно изменять конфигурацию молекул 5. Способность ряда белков ускорять химические реакции в организме 6. Наличие биологической активности, способность выполнять различные функции

Белки (протеины) содержат (%): l l l l С – 50– 55 Н – 6, 5– 7, 3 N – 15– 18 O – 21– 24 S – до 2, 4 золы – до 0, 5 Cu, I, Fe, Zn, Ca, Mg, Br и др.
Классификация белков

По степени сложности l простые белки (протеины) дают при гидролизе только аминокислоты l l l l Альбумины Глобулины Проламины Глютелины Гистоны Склеропротеины Протамины Протеиноиды

По степени сложности l сложные белки (протеиды) состоят из протеина и добавочной группы, по составу которой: l l l l Хромопротеины (гемоглобин, цитохромы, каталаза, хлорофилл) Липопротеины (компонент мембран, липопротеины крови, сфинголипиды в сером веществе мозга) Гликопротеины (кутикулярный гликопротеин – структурный материал покровных тканей насекомых, муцин – компонент слюны, протеогликановые агрегаты в хрящевых тканях) Нуклеопротеины (вирусы, хроматин, рибосомы) Металлопротеины (цитохромоксидаза, церулоплазмин крови – Cu; лактоферрин молока, трансферрин крови, ферритин селезенки – Fe) Фосфопротеины (казеин молока, вителлин и фосфитин яичного желтка, ихтулин икры рыб) Флавопротеины, добавочная группа – ФАД или ФМН (компонент дыхательной цепи)

По форме частиц l l фибриллярные (волокнистые) белки (фиброин шелка, кератин волос, коллаген кожи) глобулярные (корпускулярные) белки

По выполняемым функциям l l l структурные белки – компоненты клеточных мембран, органелл; коллаген соединительной ткани; кератин волос, ногтей; эластин в сосудистых стенках и др. каталитически активные белки (ферменты) сократительные белки: миксомиозин; белки микротрубочек; миозино- и актомиозиноподобные белки фибриллярного аппарата амебы; белки микрофибрилл, жгутиков и ресничек простейших, жгутиков сперматозоидов транспортные белки – сывороточный альбумин; церулоплазмин; трансферрин; -липопротеин; гемоглобин; транспортные белки мембран защитные белки: антитела (иммуноглобулины); белки системы свертывания крови (фибриноген, тромбин, фибрин, факторы свертывания); интерфероны и др.

По выполняемым функциям l l l токсические белки: токсины змей, скорпионов, пчел, ос и др. – в основном нейротоксины; токсины микроорганизмов и растений (дифтерийный, холерный, токсин шигеллы и др. ); белки-гормоны (инсулин, глюкагон, АКТГ и др. ) регуляторные белки (гистоны; негистоновые белки хроматина; белковые факторы репликации ДНК, транскрипции РНК, синтеза белка; стрессовые белки и др. )

По выполняемым функциям l l l резервные белки (овальбумины яиц, белки молока – казеин) рецепторные белки: рецептор ацетилхолина; фоторецепторный белок опсин; сладкочувствительный белок вкусовых рецепторов; обонятельный белок дубового шелкопряда; холинорецепторные белки звуковых рецепторов белки-ингибиторы ферментов белки вирусных оболочек (вирус табачной мозаики, бактериофаги и др. ) белки с иными функциями (гемоглобины, фибриллярные белки, рибосомальные белки и т. п. )

По выполняемым функциям l l Все белки выполняют энергетическую функцию: при окислении 1 г белка выделяется 17, 2 к. Дж энергии

По растворимости l l протеиноиды (склеропротеины) – нерастворимы в обычных растворителях – почти все фибриллярные белки альбумины – хорошо растворимы в воде и крепких растворах солей (50%-ном сульфате аммония), содержат, как правило, много гли – альбумины крови, яиц, молока глобулины – нерастворимы в воде, но растворимы в солевых растворах умеренных концентраций – белки семян (легумин гороха, фазеолин фасоли), антитела, фибрин проламины – растворимы в 60– 80%-ном растворе этанола, содержат, как правило, много глу и про – семена злаков (глиадин ржи и пшеницы, гордеин ячменя, зеин кукурузы)

По аминокислотному составу l l l протамины – содержат 80– 90% арг и ограниченный набор других аминокислот, простейшие белки, растворяются в слабых кислотах – белки половых клеток (сальмин молок семги) гистоны – высокое содержание основных аминокислот арг, лиз и гис (не < 30%), растворяются в слабых кислотах, 0, 2 н. HCl, осаждаются спиртом и аммиаком – содержатся в ядрах клеток глютелины – много глу, растворяются в щелочных растворах (0, 2– 2%-ном Na. OH) – содержатся в семенах злаков (клейковина), зеленых частях растений
Свойства белков

1. Амфотерные свойства белков l l l Кислотно-основные свойства белков определяются амино- и карбоксильными группами: НООС–R–NН 2 ⇄ –ООС–R–NН 3+ Большая часть полярных гидрофильных групп находится на поверхности белковых глобул Они определяют кислотно-основные свойства белковой молекулы Кислотные свойства – остатки глу и асп Основные свойства – остатки лиз, арг, гис, орн Если кислотные радикалы преобладают, то молекула оказывается электроотрицательной; если преобладают основные радикалы, – электроположительной

1. Амфотерные свойства белков l l l l Заряды по поверхности глобулы распределяются неравномерно Различные участки белковой молекулы могут иметь различные заряды и могут стабилизироваться диполями воды Изменение р. Н приводит к перераспределению электрических зарядов на поверхности молекул Это сказывается на свойствах, пространственной структуре, биологической активности белка Для каждого белка существует такое значение р. Н, при котором положительные и отрицательные заряды скомпенсированы (? ). Изоэлектрическая точка (ИЭТ, р. I) р. I – характерная константа белков l ИЭТ большинства белков животных тканей – от 5, 5 до 7, 0 (частичное преобладание кислых аминокислот l Однако в природе имеются белки, у которых ИЭТ – при крайних значениях р. Н (р. I пепсина – 1, р. I сальмина – около 12

1. Амфотерные свойства белков l l l Суммарный заряд белковой молекулы положителен при р. Н < р. I Суммарный заряд белковой молекулы отрицателен, если р. Н > р. I Белки легко осаждаются, если р. Н = р. I

2. Растворимость белков l l l Подавляющее большинство белков гидрофильны Растворимость их определяется природой тех групп, которые оказываются на поверхности молекулы при нативной пространственной конформации Большая часть поверхности белковой молекулы образована группами, способными гидратироваться Гидратная оболочка предохраняет молекулы белка от склеивания и выпадения в осадок Величина ее зависит от структуры белка

2. Растворимость белков l Устойчивость водного раствора белка определяется: l l наличием электрического заряда молекул белка находящейся вокруг нее водной оболочкой При удалении этих факторов белок выпадает в осадок Данный процесс может быть обратимым и необратимым

2. Растворимость белков l Обратимое осаждение белков (высаливание) – выпадение белка в осадок под действием веществ, после удаления которых он вновь возвращается в свое исходное состояние l l l соли щелочных, щелочноземельных металлов и аммония (чаще – Na 2 SO 4, (NH 4)2 SO 4) Эти соли удаляют водную оболочку и снимают заряд Чем меньше гидратная оболочка, тем меньше требуется соли (различие глобулинов и альбуминов)

2. Растворимость белков l l l Необратимое осаждение связано с глубокими внутримолекулярными изменениями структуры белка, что приводит к потере ими нативных свойств Денатурированный белок Денатурация

3. Денатурация белка l l l существенное изменение третичной и вторичной структуры белка, т. е. нарушение, разупорядочение системы нековалентных взаимодействий, не затрагивающее его ковалентной (первичной) структуры Денатурация, как правило, сопровождается утратой белком функциональных свойств, его инактивацией Денатурация может быть вызвана рядом факторов

3. Денатурация белка l l Повышение температуры приводит к возрастанию вклада энтропийного фактора, что обусловливает тепловую денатурацию, происходящую, как правило, скачкообразно Температура денатурации может быть различной l термолизин до 80 С сохраняет активность

3. Денатурация белка l Воздействие реагентов, нарушающих нековалентные взаимодействия, прежде всего систему водородных связей
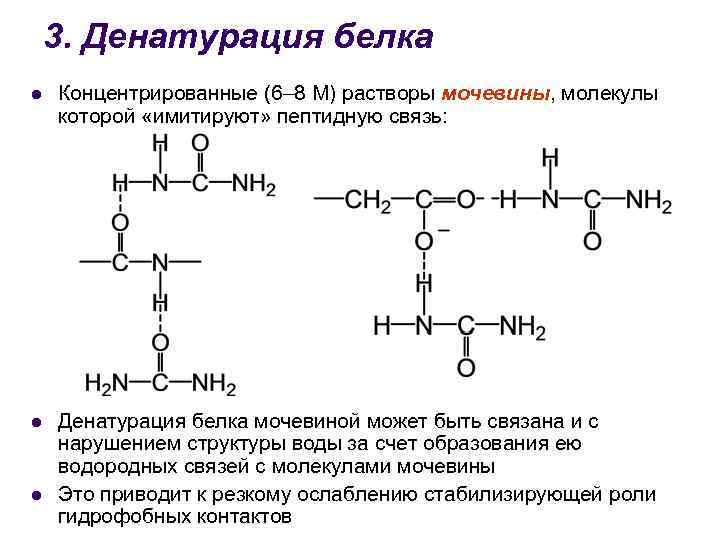
3. Денатурация белка l Концентрированные (6– 8 М) растворы мочевины, молекулы которой «имитируют» пептидную связь: l l Денатурация белка мочевиной может быть связана и с нарушением структуры воды за счет образования ею водородных связей с молекулами мочевины Это приводит к резкому ослаблению стабилизирующей роли гидрофобных контактов

3. Денатурация белка l l Еще более сильный денатурирующий агент – солянокислый гуанидин [Н 2 N=С(NН 2)2]+Сl– (обычно 6 М) В дополнение к перечисленным факторам сказывается и очень высокая ионная сила (гуанидин – очень сильное основание, практически полностью протонирован), что исключает внутрибелковые электростатические взаимодействия

3. Денатурация белка l l l Органические растворители способны устанавливать контакты с гидрофобными аминокислотными остатками белка, лишая гидрофобное ядро его стабилизирующей роли Одновременно многие растворители (спирты, формамид, муравьиная кислота) «переключают» на себя водородные связи, поддерживающие третичную структуру При повышении концентрации растворителя может нарушаться и структура воды

3. Денатурация белка l l Эффективные денатурирующие агенты – ионные детергенты (часто – додецилсульфат натрия [СН 3–(СН 2)11–ОSО 3]– Nа+ Гидрофобная цепь его образует контакты с гидрофобными остатками белка, приводящие при концентрации детергента 0, 5 м. М к полному развертыванию третичной структуры

3. Денатурация белка l l l При экстремальных значениях р. Н В сильно кислых растворах полностью протонируются отрицательно заряженные карбоксильные группы, сохраняются только положительные заряды, взаимное отталкивание которых приводит к развертыванию глобулы В щелочных растворах утрачивают положительные заряды аминогруппы и приобретают отрицательные заряды фенольные группы тир, что также ведет к развертыванию глобулы

3. Денатурация белка l l В определенных условиях может быть обратимой – ренатурация Явление денатурации белка можно наблюдать: l l l при варке яиц при свертывании молока при гниении (хранении семян, уменьшается процесс набухания и интенсивность прорастания) приготовлении консервов и т. д.

4. Коллоидные свойства растворов белка l l l Размер белковых частиц – от 1 мкм до 1 нм, поэтому растворы белков проявляют коллоидные свойства (? ), но не являются истинно коллоидными, т. к. гомогенны Растворы белков могут при определенных условиях терять свою текучесть и образовывать гели Гели возникают в результате объединения молекул в виде сетки, внутреннее пространство которой заполнено большим количеством растворителя, при этом разделения на жидкую и твердую фазы не происходит (в протоплазме клеток, хрусталике глаза, соединительных тканях и т. д. ) В состояние геля растворы белков могут переходить под действием ферментов микроорганизмов (образование кефира, простокваши из молока) При подготовке растений к зиме происходит переход части белков в состояние геля Гели со временем стареют, отслаивают воду и делятся на 2 фазы – уплотненный гель и разведенный золь – синерезис (образование творога при стоянии кефира)

5. Белки-эмульгаторы l l l Благодаря гидрофильным и гидрофобным группировкам белки могут влиять на растворимость других веществ, выступая в роли эмульгаторов В организме человека и животных в эмульгированном состоянии находятся жиры в крови и лимфе Белок образует на поверхности капелек жира тонкую пленку, притягивающую воду и препятствующую слипанию жировых частичек (молоко – эмульгированные казеиногеном капельки жира в воде)

6. Оптические свойства растворов белков l l l l Белки поглощают свет в УФ части спектра (спектрофотометрия) Окрашенные белки (хромопротеины) способны поглощать свет в видимом диапазоне Все белки поглощают свет в ИК области (ИКспектроскопия для определения относительного содержания -, - и аморфных участков в молекуле белка) Белки являются оптически активными обладают оптической анизотропией обладают способностью флуоресцировать рассеивают свет – эффект Тиндаля

7. Гидролиз белков l При гидролизе белков образуется набор соответствующих аминокислот

8. Цветные реакции на белки l l l l Биуретовая реакция Нингидриновая реакция Ксантопротеиновая реакция Реакция Сакагучи Реакция Миллона Реакция Адамкевича Реакция Паули Реакция Фоля

Литература l l l Березов Т. Т. , Коровкин Б. Ф. Биологическая химия. – М. : Медицина, 1983 Грин Н. , Стаут У. , Тейлор Д. Биология. В 3 -х т. – Т. 1. – М. : Мир, 1990 Ермолаев М. В. , Ильичева Л. П. Биологическая химия. – М. : Медицина, 1989 Основы биохимии / Пол ред. А. А. Анисимова. – М. : Высшая школа, 1986 Степанов В. М. Молекулярная биология. Структура и функции белков. – М. : Высшая школа, 1996 Филиппович Ю. Б. Основы биохимии. – М. : Высшая школа, 1993