АТМОСФЕРА ЗЕМЛИ.pptx
- Количество слайдов: 18

АТМОСФЕРА ЗЕМЛИ Атмосфера представляет собой тонкую газообразную оболочку, укрывающую Землю. В ней содержатся необходимый для фотосинтеза в растениях диоксид углерода и необходимый для дыхания животных кислород. Также атмосфера является неограниченным источником азота, необходимого для растений. Пресная вода попадает на Землю в виде росы, дождя и снега. Атмосфера защищает нас от канцерогенного солнечного УФ-излучения, смягчает климат на планете. Без атмосферы Земля испытывала бы предельные жару и холод. Атмосфера необходима для существования людей, тем не менее мы загрязняем ее в течение многих лет.

Основные слои атмосферы АТМОСФЕРА ЗЕМЛИ Тропосфера. Её верхняя граница находится на высоте 8— 10 км в полярных, 10— 12 км в умеренных и 16— 18 км в тропических широтах; зимой ниже, чем летом. Нижний, основной слой атмосферы содержит более 80 % всей массы атмосферного воздуха и около 90 % всего имеющегося в атмосфере водяного пара. В тропосфере сильно развиты турбулентность и конвекция, возникают облака, развиваются циклоны и антициклоны. Нижняя часть тропосферы (от 0 до 3000 м), контактирующая непосредственно с земной поверхностью, называется пограничным слоем. Здесь накапливаются загрязняющие вещества, выделяемые вблизи поверхности Земли. Температура воздуха в этом слое реагирует на изменение температуры поверхности за время, не превышающее 1 часа. Температура убывает с ростом высоты со средним вертикальным градиентом 0, 65°/100 м. Тропопауза - переходный слой от тропосферы к стратосфере, слой атмосферы, в котором прекращается снижение температуры с высотой (-57°С). Низкая температура этой области служит барьером, замораживающим пары воды в ледяные кристаллы, выпадающие обратно на Землю. Стратосфера - слой атмосферы, располагающийся на высоте от 11 до 50 км. Характерно незначительное изменение температуры в слое 11— 25 км (нижний слой стратосферы) и повышение её в слое 25— 40 км от − 56, 5 до 0, 8 °С (верхний слой стратосферы или область инверсии). Достигнув на высоте около 40 км значения около 273 К (почти 0 °C), температура остаётся постоянной до высоты около 55 км. Эта область постоянной температуры называется стратопаузой и является границей между стратосферой и мезосферой. Мезосфера начинается на высоте 50 км и простирается до 80— 90 км. Температура с высотой понижается со средним вертикальным градиентом (0, 25— 0, 3)°/100 м. Основным энергетическим процессом является лучистый теплообмен. Сложные фотохимические процессы с участием свободных радикалов, колебательно возбуждённых молекул и т. д. обусловливают свечение атмосферы. Линия Кармана: высота над уровнем моря, которая условно принимается в качестве границы между атмосферой Земли и космосом. Линия Кармана находится на высоте 100 км над уровнем моря. Граница атмосферы Земли. Принято считать, что граница атмосферы Земли и ионосферы находится на высоте 118 километров. Это показывает анализ параметров движения высокоэнергетических частиц, перемещающихся в атмосфере и ионосфере. Термосфера. Верхний предел — около 800 км. Температура растёт до высот 200— 300 км, где достигает значений порядка 1500 К, после чего остаётся почти постоянной до больших высот. Под действием ультрафиолетовой и рентгеновской солнечной радиации и космического излучения происходит ионизация воздуха ( «полярные сияния» ) — основные области ионосферы лежат внутри термосферы. На высотах свыше 300 км преобладает атомарный кислород. Верхний предел термосферы в значительной степени определяется текущей активностью Солнца. В периоды низкой активности происходит заметное уменьшение размеров этого слоя.

АТМОСФЕРА ЗЕМЛИ Состав атмосферы Основными компонентами А. являются азот (N 2, 78 об. %), кислород (20. 94 об. %). В значительно меньших количествах в атмосфере содержится инертный газ аргон (0. 93 об. %), диоксид углерода (0. 04 об. %). Еще меньше содержание других инертных газов (неон, гелий и криптон) и метана. Содержание диоксида углерода в А. предельно низкое, но CO 2 – очень важный материал для фотосинтеза! Содержание водяного пара варьируется от 0. 1% до 5 % в зависимости от температуры, осадков, скорости испарения и других факторов. Обычно оно колеблется между 1% и 3%. Количество воды в атмосфере зависит от температуры, т. к. давление водяного пара увеличивается с температурой. Помимо пара воды и газов в атмосфере также содержатся пылинки, которые выступают центрами кристаллизации льда и конденсации капель воды. Мельчайшие частицы с диаметром менее 10 мкм образуют аэрозоли. Большие по размерам частицы называются макрочастицами. Оба вида частиц могут быть жидкими и твердыми. Малые частицы имеют несравнимую с их размером, очень большую площадь поверхности, на которой происходят химические взаимодействия, вследствие абсорбции или адсорбции.

ХИМИЯ ТРОПОСФЕРЫ АТМОСФЕРА ЗЕМЛИ Тропосфера является неравновесной, химически-активной системой. Большинство газообразных примесей, выделяемых с поверхности планеты в тропосферу в результате геохимических и биохимических процессов, находится в восстановленной форме или в виде оксидов с низкой степенью окисления (H 2 S, NH 3, CH 4, N 2 O и т. д ). Анализ атмосферных осадков показывает, что возвращаемые на поверхность планеты примеси представлены в основном соединениями с высокой степенью окисления (H 2 SO 4 и сульфаты, HNO 3 и нитраты, диоксиды углерода и серы). Таким образом, тропосфера играет на планете роль глобального окислительного резервуара. Процессы окисления примесей в тропосфере могут протекать: 1) непосредственно в газовой фазе; 2) в растворе, когда окислению предшествует абсорбция частицами воды; 3) на поверхности твердых частиц, взвешенных в воздухе, когда стадии окисления предшествует адсорбция примесей. Окислительная способность атмосферного воздуха подтверждается термодинамическими расчетами. Однако, скорость окисления примесей непосредственно молекулой кислорода в газовой фазе при характерных для тропосферы температурах и давлениях мала. Исследования последних десятилетий показали, что основную роль в процессах окисления, протекающих в газовой фазе, играют свободные радикалы, образующиеся под действием солнечного излучения. Свободные радикалы - незаряженные фрагменты молекул, которые в отличие от обычных химических веществ содержат неспаренные электроны на внешней свободной орбитали. Радикалы обладают высокой химической активностью и существуют очень короткое время. С радикалами связаны многие сложные, часто малоизученные реакции, которые протекают в обычной и загрязненной атмосфере.

АТМОСФЕРА ЗЕМЛИ Наиболее важным в химии атмосферы является гидроксильный радикал (ОН ). Радикал ОН может образовываться в целом ряде процессов. В верхних слоях атмосферы возможна диссоциация паров воды под действием УФ-излучения солнца: H 2 Oпар + h OH. + H. . Этот процесс не реализуется в нижних слоях атмосферы из-за отсутствия УФ-излучения необходимой длины волны (менее 175 нм), так как оно поглощается в верхних слоях. В тропосфере образование ОН происходит с участием метастабильных атомов кислорода, в основном в состоянии (1 D). Образование атомов О в состоянии (1 D) происходит в разнообразных процессах, определяющими из которых являются: O 2 + h O (1 D) + O (3 P), < 175 нм, O 3 + h O (1 D) + O 2, < 310 нм, N 2 O + h O (1 D) + N 2, < 340 нм, NO 2 + h O (1 D) + NO, < 245 нм. Наибольшее значение среди процессов, ведущих к образованию ОН с участием атомов О в состоянии (1 D), являются реакции с молекулами паров воды, метана и водорода, константы скорости которых близки и составляют порядка К=(1 -4) 10 -4 шт/см 3 с. O (1 D) + H 2 O 2 OH , O (1 D) + CH 4 CH 3 + OH , O (1 D) + H 2 H + OH. Кроме указанных, определенный вклад в появление гидроксильных радикалов могут давать и указанные ниже реакции: HNO 2 + h NO + OH , < 344 нм, HNO 3 + h NO 2 + OH , < 335 нм, H 2 O 2 + h 2 OH , < 300 нм. Атомарный водород может реагировать с молекулярным кислородом с образованием гидропероксидного радикала: H + O 2 HO 2. Этот радикал появляется в качестве продукта и при взаимодействии озона или перекиси водорода с гидроксильным радикалом: O 3 + OH HO 2 + O 2, H 2 O 2 + OH H 2 O + HO 2. В свою очередь гидропероксидный радикал, реагируя с оксидом азота или озоном, вновь приводит к появлению гидроксильного радикала в тропосфере: HO 2 + NO NO 2 + OH , HO 2 + O 3 2 O 2 + OH. Гидроксильный радикал способен и замкнуть цепочку превращений радикалов в тропосфере: HO 2 + OH H 2 O + O 2, HO 2 + HO 2 H 2 O + O 3. Концентрации радикалов на различных высотах и средние времена жизни в тропосфере. Радикал Общее число молекул ОН НО 2 Концентрация, см-3 5 км 20 км 35 км 1, 6 1019 1, 9 1018 1, 6 1017 8, 5 106 3 107 108 Время жизни, с 1 240

ХИМИЧЕСКИЕ ПРЕВРАЩЕНИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ В ТРОПОСФЕРЕ. 1. ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. Основные источники поступления СН 4 в атмосферу даны ниже цифры - млн. т СН 4/год): АТМОСФЕРА ЗЕМЛИ позвоночные животные (в основном крупный рогатый скот): 70 -100; рисовые поля: 70 -170; насекомые и термиты: 20 -80; сжигание биомассы: 20 -110; болота, озера: 20 -70; захоронение твердых отходов: 30 -60; тундра (северные марши): 40 -110; угледобыча: 12 -40; утечки природного газа: 20 -50. Фотохимическое окисление метана и его гомологов в тропосфере протекает преимущественно по радикальному механизму. Процесс окисления инициируется главным образом гидроксильным радикалом: RCH 3 + OH RCH 2 + H 2 O. Константы скорости для этой реакции составляют для метана - 8 10 -15 см 3/с, для этана - 3 10 -13 см 3/с, для пропана - 2 10 -12 см 3/с и при дальнейшем увеличении числа атомов углерода в цепи практически не изменяются. Образовавшийся в первичной реакции алкильный радикал реагирует с молекулой кислорода с образованием пероксидного радикала: RCH 2 + O 2 + M RCOO + M. Пероксидный радикал чрезвычайно реакционно способен, поэтому направления дальнейшей трансформации его разнообразны, но чаще всего ведут к росту цепи (образованию алкоксильного радикала): RCOO + NO RCO + NO 2, 2 RCOO 2 RCO + O 2 , RCOO + HO 2 (RH) RCOOH + O 2 (R ), RCOOH RCO + OH. Взаимодействие алкоксильного радикала с молекулой кислорода приводит к образованию альдегидов, в частности формальдегида: RCO + O 2 R(CO)H + HO 2 , CH 3' + O 2 CH 2 O + HO 2 O. Молекулы формальдегида подвергаются фотолизу: CH 2 O + h HCO + H , CH 2 O + h CO + H 2, причем сумма квантовых выходов обеих реакций близка к 1 при облучении светом с < 350 нм.

АТМОСФЕРА ЗЕМЛИ Формильный радикал может образоваться и при взаимодействии формальдегида с гидроксильным радикалом: CH 2 O + OH CHO + H 2 O. Последующее взаимодействие формильного и гидроксильного радикалов приводит к образованию конечных продуктов реакции: HCO + OH CO + H 2 O. Таким образом, общую схему окисления метана можно представить следующим образом: Гомологи метана окисляются по аналогичной схеме (без учета побочных реакций), например с оксидами азота, что иллюстрирует следующая схема: RCH 2 + O 2 RCH 2 OO , RCH 2 OO + HO 2 RCH 2 OOH + O 2, RCH 2 OOH R 1 CH 3 + CO 2, то есть произошло укорочение длины цепи на 1 углеродный атом и процесс продолжается вновь. В качестве побочных продуктов накапливаются альдегиды и кетоны, как было показано выше. Альдегиды и кетоны, образующиеся при фотоокислении углеводородов или непосредственно выделенные в тропосферу из естественных и антропогенных источников, при взаимодействии с атомами кислорода или гидроксильными радикалами порождают цепной процесс их окисления: R 1 -C(O)-R 2 + h R 1 + R 2 C=O, RC(O)H + OH R 1 C=O + H 2 O, RC(O)H + O (3 P) R C=O + OH. Реакции атомарного кислорода с альдегидами и кетонами протекают с меньшей скоростью, чем с радикалом ОН (k = 5 10 -13 см 3/с для атомов кислорода и k = 10 -11 см 3/с для радикалов OH ), поэтому вклад атомарного кислорода в фотохимическое превращение карбонильных соединений менее значителен, чем гидроксильных радикалов. Образующиеся в процессах фотодиссоциации и в реакциях с гидроксильным радикалом промежуточные радикальные продукты включаются в длинную цепь превращений, в общем случае аналогичных рассмотренным ранее, например: R C=O + O 2 RC(O)OO , RC(O)OO + NO RC(O)O + NO 2, RC(O)O + O 2 R 1 OO + CO 2. Образующийся пероксидный радикал претерпевает превращения, описанные ранее. В общем виде уравнение разложения альдегидов и кетонов при инициировании процесса УФ-излучением или гидроксильным радикалом может быть записано: RCHO + OH* + O 2 + NO CO 2 + CO + NO 2 + H 2 O, RCHO + h + O 2 + NO CO + NO 2 + H 2 O + OH.

АТМОСФЕРА ЗЕМЛИ 2. АРОМАТИЧЕСКИЕ УГЛЕВОДОРОДЫ. Таким образом, в процессе трансформации алканов, алифатических альдегидов и кетонов происходит увеличение концентрации диоксида азота в атмосфере, что оказывает огромное влияние на атмосферный цикл соединений азота. Напротив, как показали эксперименты, фотохимическое окисление бензальдегида и других ароматических соединений приводит к связыванию части оксидов азота. Реакции начинаются с образования бензольного радикала, который в дальнейшем трансформируется в пероксибензоилнитрат, нитрофенол, фенол и его эфиры с азотной кислотой: + NO С 6 H 5 C(O)O* + NO 2 С 6 H 5 C (O) + O 2 С 6 H 5 C(O)OO + NO 2 С 6 H 5 C(O)OONO 2, С 6 H 5 C(O)O* С 6 H 5* + CO 2, С 6 H 5 * + O 2 + NO С 6 H 5 ONO 2 С 6 H 5 OO* + NO С 6 H 5 O* + NO 2, С 6 H 5 O* + NO 2 C 6 H 4(OH)NO 2, С 6 H 5 O* + HO 2 С 6 H 5 OH + O 2. В качестве побочных продуктов фотохимического окисления образуются токсичные пероксиацетилнитраты (C 6 H 5 C(O)OONO 2), являющиеся одним из основных компонентов фотохимического смога. Реакционная способность ароматических углеводородов в значительной степени определяется их строением. Наименее реакционно способным из них является бензол. При облучении светом с = 300 нм в смоговой камере в присутствии NO при T = 20 °C в течение 5 часов в реакцию вступило около 10 % бензола и 25 толуола, а в продуктах реакции обнаруживалось большое количество нитросоединений. Последние, например нитрофенол, регистрируются и в атмосферном воздухе. Поэтому, можно предположить, что эмиссия в приземные слои воздуха бензола и его гомологов приводит к уменьшению относительного содержания оксидов азота в атмосфере.

АТМОСФЕРА ЗЕМЛИ 3. НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ. Если инициирование разложения предельных углеводородов и их производных в тропосфере осуществляется как УФ- квантами света, так и гидроксильными радикалами, то для непредельных углеводородов характерны реакции с атомарным кислородом, гидроксильным радикалом и озоном. 1. Реакции с атомами О. Наиболее вероятно в первичной реакции атомов О с пропиленом образование мостиковой структуры, стабилизация которой дает пропиленоксид или пропионовый альдегид, а взаимодействие с молекулой кислорода - к разрыву углерод-углеродной связи: Дальнейшие превращения пероксидного радикала мы уже рассмотрели (слайд 6), а радикал типа CH 3 C(O)OO· реагирует чаще всего с оксидами азота: CH 3 C(O)OO + H 2 O CH 3 C(O)OH + HO 2 , CH 3 C(O)OO + NO CH 3 + CO 2 + NO 2, CH 3 C(O)OO + NO 2 CH 3 C(O)OONO 2. Пропиленоксид, пропионовый альдегид, пропионовая кислота и пероксиацетилнитрат обнаруживаются в продуктах окисления пропилена атомарным кислородом в смоговых камерах. Среди продуктов окисления также регистрируются формальдегид, метанол, диэтиловый эфир, метилнитрат. Все они образуются, вероятно, в результате процессов дальнейшей трансформации метилпероксидного радикала. Отметим, что вклад атомов О в окисление непредельных углеводородов меньше, чем радикалов ОН и озона из-за низкой концентрации атомарного кислорода в тропосфере.

2. Реакции с гидроксильным радикалом. Гидроксильный радикал главным образом присоединяется по двойной связи: АТМОСФЕРА ЗЕМЛИ CH 3 -CH=CH 2 + OH CH 3 CH CH 2 OH (1), CH 3 -CH=CH 2 + OH СH 3 CH(OH)CH 2 (2). Константа скорости первой реакции в 2 раза больше, чем второй, поэтому выход продуктов в 1 реакции больше. Образующиеся гидроксилалкильные радикалы быстро реагируют с кислородом и оксидом азота: CH 3 CH CH 2 OH + O 2 CH 3 CHOO + CH 2 OH, CH 3 CHOO + NO CH 3 CHO + NO 2. В дальнейшем может происходить или стабилизация радикалов CH 3 CHO CH 3 C(O)H (уксусный альдегид) или реакция с молекулами кислорода CH 2 OH + O 2 H 2 C=O +HO 2. В качестве основного продукта превращения регистрируется и муравьиная кислота, образование которой схематично можно представить: CH 2 OH + O 2 OOCH 2 OH; OOCH 2 OH + NO 2, OCH 2 OH + O 2 HC(O)OH + HO 2. Таким образом, основными продуктами, образующимися при взаимодействии алкенов с гидроксильным радикалом являются CO, CO 2, уксусный и муравьиный альдегиды, муравьиная кислота и вода.

АТМОСФЕРА ЗЕМЛИ 3. Реакции с озоном. Константа скорости взаимодействия озона с непредельными углеводородами примерно в миллион раз меньше, чем для реакции присоединения ОН или атомарного кислорода. Однако, концентрация озона даже в незагрязненном воздухе в средних слоях тропосферы примерно в 10 7 раз выше, чем концентрации ОН и атомов О, поэтому озон должен вносить заметный вклад в окисление непредельных углеводородов. Общепринято, что взаимодействие озона с алкенами происходит по механизму Криге с образованием в качестве промежуточных продуктов неустойчивых соединений озонидов: Дальнейшая судьба вторичных озонидов, обладающих избыточной энергией, известна лишь для небольшого числа соединений, например бирадикал типа CH 3 CH OO в примерно 80 % случаев претерпевают перегруппировку с дальнейшим распадом: Конечными продуктами трансформации бирадикала рассмотренного типа являются СО, СО 2, СН 4, НСО·, СН 3 О и пары воды. Значительное влияние на скорость процесса и состав образующихся продуктов фотохимического окисления органических соединений в тропосфере оказывает присутствие аэрозолей. Например, в присутствии мелко дисперсного оксида цинка в составе продуктов превращения алкенов появляются цианиды типа HCN и CH 3 CN. Высокой скоростью окисления в тропосфере обладают непредельные углеводороды, выделяемые растениями (изопрен и углеводороды терпенового ряда: , -пинен, карен, лимонен и др. ). Изопрен в значительных количествах выделяется лиственными породами (дубом, платаном, эвкалиптом); - пинен выделяют в основном хвойные леса (сосна, пихта). Механизмы превращений терпенов в газофазных реакциях, инициируемых гидроксильным радикалом или озоном, изучены недостаточно подробно. Среди продуктов взаимодействия изопрена с озоном обнаружены формальдегид, муравьиная кислота и СО. Поэтому полагают, что фотоокисление изопрена протекает через те же стадии, характерные для фотоокисления олефинов. Оценки показывают, что время пребывания этих соединений в атмосфере до распада не должно превышать 4 -5 часов, иногда, в зависимости от реакционной способности терпенов, это время может составлять несколько минут.

4. ТРАНСФОРМАЦИЯ СОЕДИНЕНИЙ СЕРЫ В ТРОПОСФЕРЕ. Основные потоки соединений серы в атмосферу связаны с антропогенной деятельностью: АТМОСФЕРА ЗЕМЛИ Процессы окисления соединений серы в тропосфере инициируются в основном свободными радикалами. Например, H 2 S последовательно окисляется до диоксида серы по следующему наиболее вероятному механизму: H 2 S + OH H 2 O + HS ; HS + O 2 OH + SO; SO + HO 2 SO 2 + OH. Получающийся SO 2, как и SO 2, выделяемый из антропогенных источников, подвергается дальнейшему окислению. Анализ возможных каналов трансформации диоксида серы показал, что наибольший вклад в газофазное окисление дают радикалы ОН и НО 2 : SO 2 + OH + M HSO 3 + M; HSO 3 + HO 2 SO 3 + 2 OH , SO 2 + HO 2 SO 3 + OH. Некоторый вклад в суммарное окисление диоксида серы могут давать и органические радикалы: SO 2 + CH 3 OO SO 3 + CH 3 O. Преимущественное значение в процессах окисления диоксида серы имеет первая реакция среди перечисленных выше.
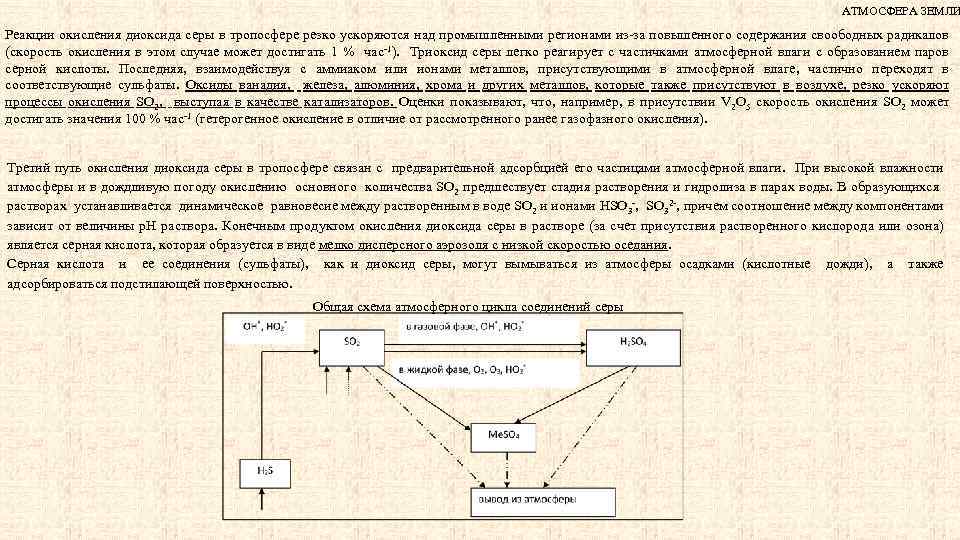
АТМОСФЕРА ЗЕМЛИ Реакции окисления диоксида серы в тропосфере резко ускоряютcя над промышленными регионами из-за повышенного содержания своободных радикалов (скорость окисления в этом случае может достигать 1 % час-1). Триоксид серы легко реагирует с частичками атмосферной влаги с образованием паров серной кислоты. Последняя, взаимодействуя с аммиаком или ионами металлов, присутствующими в атмосферной влаге, частично переходят в соответствующие сульфаты. Оксиды ванадия, железа, алюминия, хрома и других металлов, которые также присутствуют в воздухе, резко ускоряют процессы окисления SO 2, выступая в качестве катализаторов. Оценки показывают, что, например, в присутствии V 2 O 5 скорость окисления SO 2 может достигать значения 100 % час-1 (гетерогенное окисление в отличие от рассмотренного ранее газофазного окисления). Третий путь окисления диоксида серы в тропосфере связан с предварительной адсорбцией его частицами атмосферной влаги. При высокой влажности атмосферы и в дождливую погоду окислению основного количества SO 2 предшествует стадия растворения и гидролиза в парах воды. В образующихся растворах устанавливается динамическое равновесие между растворенным в воде SO 2 и ионами HSO 3 -, SO 32 -, причем соотношение между компонентами зависит от величины р. Н раствора. Конечным продуктом окисления диоксида серы в растворе (за счет присутствия растворенного кислорода или озона) является серная кислота, которая образуется в виде мелко дисперсного аэрозоля с низкой скоростью оседания. Серная кислота и ее соединения (сульфаты), как и диоксид серы, могут вымываться из атмосферы осадками (кислотные дожди), а также адсорбироваться подстилающей поверхностью. Общая схема атмосферного цикла соединений серы

АТМОСФЕРА ЗЕМЛИ 5. ТРАНСФОРМАЦИЯ СОЕДИНЕНИЙ АЗОТА В ТРОПОСФЕРЕ. Соединения азота в тропосфере представлены в основном оксидами азота, аммиаком, а также солями аммония, азотной кислотой и нитратами. Среди оксидов азота следует выделить гемиоксид (закись азота, N 2 O), оксид и диоксид азота. Другие известные соединения азота с кислородом (N 2 O 3, N 2 O 4, N 2 O 5) в условиях тропосферы неустойчивы. Естественные и антропогенные источники соединений азота, содержащихся в тропосфере. Источники Естественные: 1) почвенная эмиссия (NH 3) 2) грозовые разряды (NO, NO 2) 3) горение биомассы (NO, NO 2) 4) прочие Антропогенные: 1) сжигание топлива 2) транспорт 3) промышленность Мощность выбросов млн. т N/год % 8 14 12 21 2 - 12 4 – 21 12 21 21 14 1 2 Основные каналы трансформации N 2 O в тропосфере приходятся на фотодиссоциацию N 2 O + h ( < 250 нм) N 2 + O, или взаимодействие с метастабильным атомом О: N 2 O + O (1 D) N 2 + O 2; N 2 O + O (1 D) 2 NO. Последние реакции протекают примерно с одинаковыми скоростями (k = 8 10 -11 cм 3/c). Так концентрация атомов кислорода в состоянии (1 D), как и доля квантов света с длиной волны меньше 250 нм, в тропосфере незначительны, поэтому и столь велико время жизни для N 2 О по отношению к процессам выведения. В стратосфере, по мере увеличения концентрации атомарного кислорода и потока коротковолнового излучения скорость процессов разрушения молекул гемиоксида азота резко возрастает. Поэтому концентрация его на высоте 35 км примерно в 10 раз меньше, чем в тропосфере.

АТМОСФЕРА ЗЕМЛИ Измерения последних лет показали, что отношение концентраций NO к NO 2 в тропосфере близко к 1. Окисление NO до NO 2 происходит преимущественно в 2 основных процессах: NO + HO 2 NO 2 + OH· (k 1), NO + O 3 NO 2 + O 2 (k 2). При 298 К константы скорости этих реакций равны: k 1 = 8, 4 10 -12 см 3/с и k 2 =1, 8 10 -14 см 3/с. В тропосфере под действием излучения с длиной волны короче 398 нм диоксид азота разлагается: NO 2 + h ( < 398 нм) NO + O(3 P). Образующийся NO вновь подвергается окислению, а атомарный кислород приводит к образованию озона в тропосфере. Важной составной частью атмосферного цикла азота является образование азотной кислоты. Примерно половина (44 %) её образуется в результате взаимодействия NO 2 c гидроксильным радикалом: NO 2 + OH + M HNO 3 + M, около 24 % азотной кислоты от общего её количества появляется в атмосфере в результате растворения пентаоксида азота в парах воды: N 2 O 5 + H 2 O 2 HNO 3. Остальное количество азотной кислоты образуется преимущественно при взаимодействии диоксида азота с органическими кислородсодержащими радикалами. Часть азотной кислоты разлагается под действием света с образованием оксидов азота: HNO 3 + h ( < 355 нм) NO 2 + OH , которые вновь вовлекаются в атмосферный цикл. Основное количество азотной кислоты выводится из тропосферы с осадками в виде растворов кислоты или ее солей, что способствует закислению природной среды, и в первую очередь поверхностных водоемов. Среди нитратов, присутствующих в атмосфере, основную массу составляет нитрат аммония, который, как и в случае сульфата аммония, образуется при взаимодействии аэрозолей соответствующих кислот с NH 3 и его аэрозолями. Часть газообразного аммиака вступает в реакцию с гидроксильным радикалом с образованием в качестве промежуточного продукта гидразина: NH 3 + OH NH 2 + H 2 O, который легко окисляется далее: NH 2 + O 2 HNO + OH ; HNO + O 2 NO + HO 2

7. ДИСПЕРСНЫЕ СИСТЕМЫ В АТМОСФЕРЕ. АТМОСФЕРА ЗЕМЛИ Аэрозоль - это дисперсная система с газообразной дисперсной средой и твердой или жидкой диспергированными фазами, частицы которых могут достаточно долго находиться во взвешенном состоянии. Атмосфера вблизи поверхности Земли содержит частицы во взвешенном состоянии. Обычно они имеют сложную форму, но упрощенно их представляют в виде эквивалентных сфер, радиусом R, величина которого лежит в диапазоне от 10 -3 до 102 мкм. По агрегатному состоянию и размерам частиц дисперсной фазы аэрозоли делят на туманы – системы с жидкой дисперсной пыли – системы с твердыми частицами дымы – системы, размеры твердых частиц в фазой в виде капель размером 0, 1 -10 мкм; размером более 10 мкм; которых находятся в пределах 0, 001 -10 мкм. Источники образования аэрозолей (цифры - млн. т/год) Естественные источники - частицы почвы и пород (100 -150); - лесные пожары и очистка вырубок (3 -150); - морская соль (200); - вулканическая пыль (25 -150); - сульфаты, образующиеся из H 2 S (130 -200); - аммонивые соли (80 -250); - нитраты из оксидов азота (60); - углеводороды растительного происхождения (75 -200) Антропогенные источники - непосредственная эмиссия частиц (взвешенные; 450); - аэрозоли, образующиеся из газовых выбросов, или вторичный аэрозоль: а) сульфаты из SO 2 (130 -200); б) нитраты из NO 2 (30 -60); в) углеводороды (30 -90). Пребывание аэрозолей в тропосфере является динамическим процессом, в течение которого они находятся в равновесии между образованием в первоначальной форме и выведением в конечной форме. Аэрозольные частицы в тропосфере образуются из газов (окисление углеводородов, NO 2 и SO 2), механизмы образования которых см. слайды выше (сульфаты, нитраты, серная и азотная кислоты). Скорость окисления определяется как скоростью диффузии газа к поверхности частицы, так и скоростью диффузии реагирующего газа внутри частицы (гетерогенный процесс). Верхний предел скорости гетерогенного процесса может быть оценен как частота столкновений молекул газа с частицей на единицу поверхности в единицу времени, в предположении, что каждое столкновение ведет к взаимодействию.

Выведение примесей из атмосферы АТМОСФЕРА ЗЕМЛИ Мелкодисперсные аэрозоли (R 20 мкм) удаляются из атмосферы главным образом в результате их вымывания осадками (до 80 % от общего количества) и непосредственно в процессе осаждения на землю ("сухое" осаждение, около 20 %) - седиментация. Снежные хлопья и дождевые капли выносят примеси из облака, а также захватывают частицы из столба воздуха под облаком. Процесс "мокрого" очищения атмосферного воздуха зависит от размеров капель дождя (кристаллов снега), плотности и скорости их падения. Снежные хлопья из-за развитости поверхности являются более эффективными с точки зрения выведения аэрозольных частиц, по сравнению с дождевыми осадками. Дождь интенсивностью 2 мм/час в течение 15 минут вымывает из атмосферы 28 % частиц размером до 10 мкм. Лучше всего промывает атмосферу мелкий моросящий дождь. "Самоочищение" атмосферы может происходить и при вымораживании загрязняющих веществ. Так при температуре ниже 263 К в полярных областях происходит вымораживание SO 2. От скорости осаждения аэрозольных частиц зависит их продолжительность пребывания в атмосфере. В целом эта величина колеблется от нескольких суток до нескольких недель, составляя в среднем около одной недели. Наиболее мелкие частицы могут оставаться в атмосфере во взвешенном состоянии более года. Время жизни капель невелико – от нескольких минут в случае больших дождевых капель и примерно до одного часа для капель облаков. Время жизни частиц смога размером ˂1 мкм достигает недели. Скорость "сухого" осаждения зависит и от рода подстилающей поверхности. Наибольшая величина скорости наблюдается для воды, наименьшая - для травы в осенний период. Так скорость осаждения SO 2 на воде составляет 2, 2 см/с, а на траве осенью - 0, 3 см/с, на траве летом - 0, 8 см/с. Экспериментально установлено, что на деревьях, кустарниках и траве оседает до 70 % взвешенных частиц. Листья с шероховатой поверхностью удерживают пыли в 3 -6 раз эффективнее, чем с гладкой. Следовательно, в запыленных районах предпочтительнее высаживать вязы, по сравнению с осиной и тополем. По эффективности поглощения SO 2 из атмосферного воздуха древесные породы следует расположить в следующей последовательности: тополь бальзамический (1) ясень зеленый (0, 9) липа (0, 5) клен остролистный (0, 1). В течение года листья растений могут усваивать из воздуха до 2 т/км 2 NH 3. В процессах очищения атмосферного воздуха большая роль отводится почвенным микроорганизмам. Микроорганизмы превращают на 1 км 2 около 80 т СО в СО 2. В припочвенном слое воздуха за счет деятельности почвенных бактерий концентрация СО в течение 3 часов может снизиться со 140 мг/м 3 практически до нуля, содержание SO 2 за 15 минут уменьшается более, чем в 100 раз.

АТМОСФЕРА ЗЕМЛИ
АТМОСФЕРА ЗЕМЛИ.pptx