1 Шкала р. НКафедра общей и медицинской химии
























![37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11 37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_36.jpg)
![38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH 38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_37.jpg)
![39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0, 39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0,](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_38.jpg)



03-1_shkala_rn.ppt
- Размер: 12.8 Мб
- Автор:
- Количество слайдов: 42
Описание презентации 1 Шкала р. НКафедра общей и медицинской химии по слайдам
 1 Шкала р. НКафедра общей и медицинской химии
1 Шкала р. НКафедра общей и медицинской химии
 2 Основные функции воды в организме Обеспечение процессов всасывания и механического передвижения питательных веществ Поддержание оптимального осмотического давления в крови и тканях Обеспечение функционирования белков, нуклеиновых кислот, полисахаридов Участие в процессах биосинтеза, ферментативного катализа, гидролиза Поддержание температуры тела
2 Основные функции воды в организме Обеспечение процессов всасывания и механического передвижения питательных веществ Поддержание оптимального осмотического давления в крови и тканях Обеспечение функционирования белков, нуклеиновых кислот, полисахаридов Участие в процессах биосинтеза, ферментативного катализа, гидролиза Поддержание температуры тела
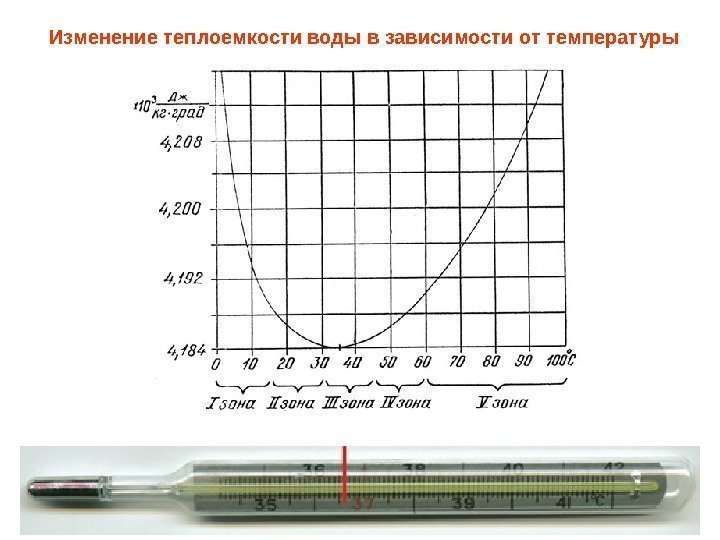
 3 Изменение теплоемкости воды в зависимости от температуры
3 Изменение теплоемкости воды в зависимости от температуры
 4 Значение растворов в жизнедеятельности организмов. Важнейшие биологические жидкости — кровь, лимфа моча, слюна, пот являются растворами солей, белков, углеводов, липидов в воде. Усвоение пищи связано с переходом питательных веществ в растворенное состояние. Биохимические реакции в живых организмах протекают в растворах. Биожидкости участвуют в транспорте: — кислорода, питательных веществ (жиров, аминокислот), — лекарственных препаратов к органам и тканям, — выведении из организма метаболитов: мочевины, билирубина, углекислого газа Плазма крови является средой для клеток — лимфоцитов, эритроцитов, тромбоцитов.
4 Значение растворов в жизнедеятельности организмов. Важнейшие биологические жидкости — кровь, лимфа моча, слюна, пот являются растворами солей, белков, углеводов, липидов в воде. Усвоение пищи связано с переходом питательных веществ в растворенное состояние. Биохимические реакции в живых организмах протекают в растворах. Биожидкости участвуют в транспорте: — кислорода, питательных веществ (жиров, аминокислот), — лекарственных препаратов к органам и тканям, — выведении из организма метаболитов: мочевины, билирубина, углекислого газа Плазма крови является средой для клеток — лимфоцитов, эритроцитов, тромбоцитов.
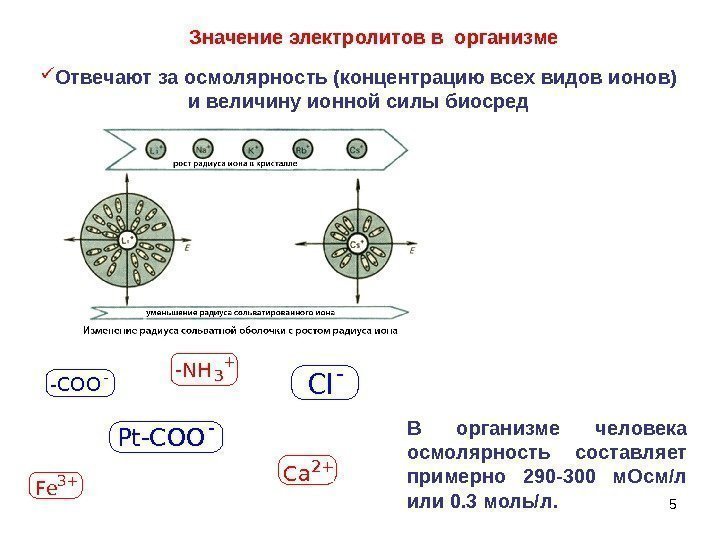
 5 Отвечают за осмолярность (концентрацию всех видов ионов) и величину ионной силы биосред Значение электролитов в организме. Ca 2 + -COO— N H 3 + Cl — Fe 3+ Pt-COO — В организме человека осмолярность составляет примерно 290 -300 м. Осм/л или 0. 3 моль/л.
5 Отвечают за осмолярность (концентрацию всех видов ионов) и величину ионной силы биосред Значение электролитов в организме. Ca 2 + -COO— N H 3 + Cl — Fe 3+ Pt-COO — В организме человека осмолярность составляет примерно 290 -300 м. Осм/л или 0. 3 моль/л.
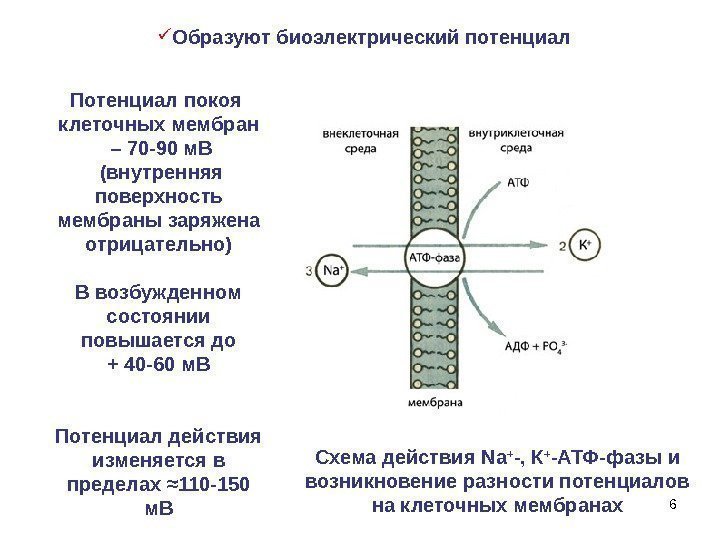
 6 Схема действия Na + -, К + -АТФ-фазы и возникновение разности потенциалов на клеточных мембранах. Потенциал покоя клеточных мембран – 70 -90 м. В (внутренняя поверхность мембраны заряжена отрицательно) В возбужденном состоянии повышается до + 40 -60 м. В Потенциал действия изменяется в пределах ≈ 110 -150 м. В Образуют биоэлектрический потенциал
6 Схема действия Na + -, К + -АТФ-фазы и возникновение разности потенциалов на клеточных мембранах. Потенциал покоя клеточных мембран – 70 -90 м. В (внутренняя поверхность мембраны заряжена отрицательно) В возбужденном состоянии повышается до + 40 -60 м. В Потенциал действия изменяется в пределах ≈ 110 -150 м. В Образуют биоэлектрический потенциал
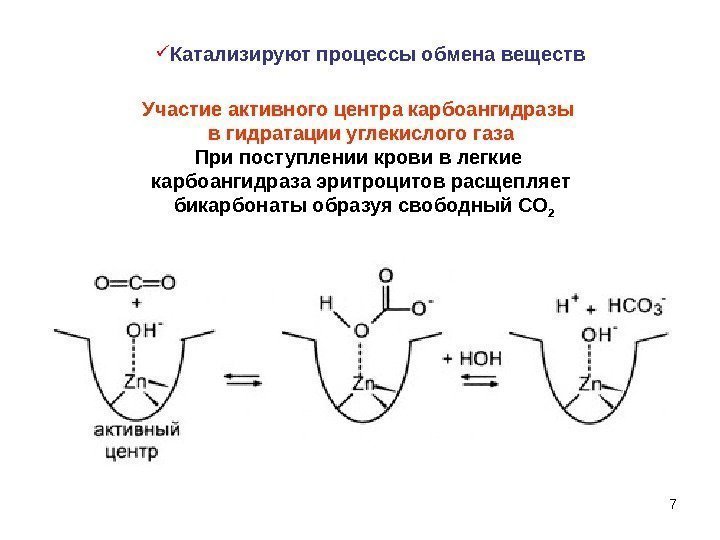
 7 Участие активного центра карбоангидразы в гидратации углекислого газа При поступлении крови в легкие карбоангидраза эритроцитов расщепляет бикарбонаты образуя свободный СО 2 Катализируют процессы обмена веществ
7 Участие активного центра карбоангидразы в гидратации углекислого газа При поступлении крови в легкие карбоангидраза эритроцитов расщепляет бикарбонаты образуя свободный СО 2 Катализируют процессы обмена веществ
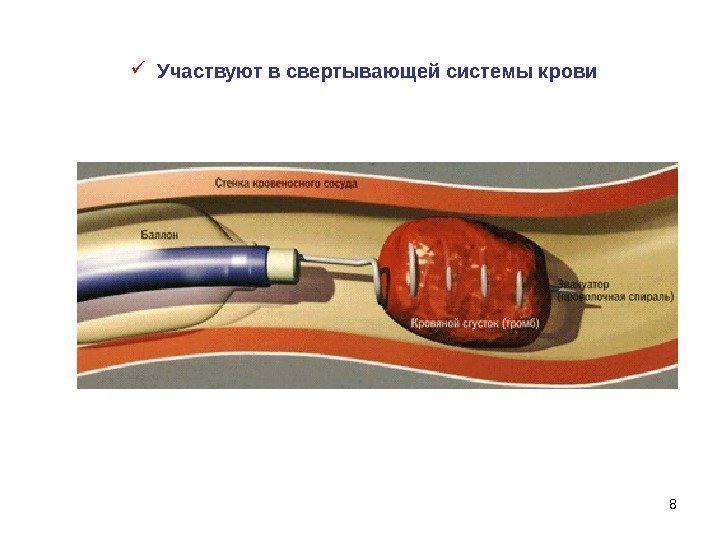
 8 Участвуют в свертывающей системы крови
8 Участвуют в свертывающей системы крови
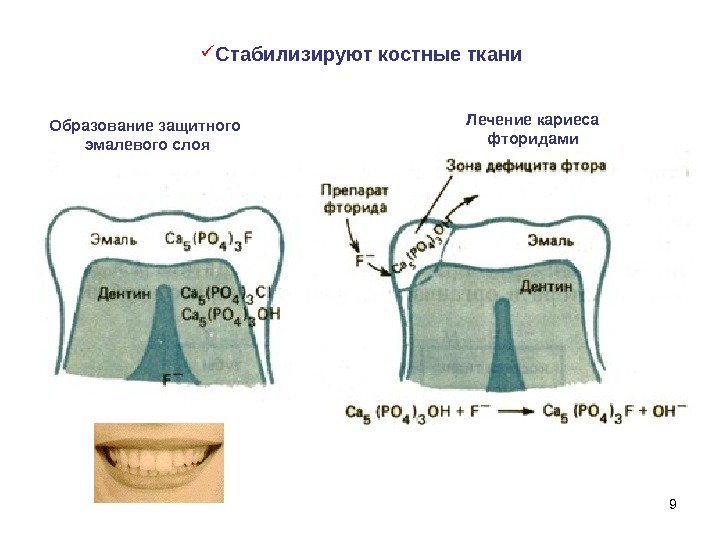
 9 Образование защитного эмалевого слоя Лечение кариеса фторидами Стабилизируют костные ткани
9 Образование защитного эмалевого слоя Лечение кариеса фторидами Стабилизируют костные ткани
 10 Какие б чувства не таились Тогда во мне — теперь их нет: Они прошли иль изменились. . . Мир вам, тревоги прошлых лет! В ту пору мне казались нужны Пустыни, волн края жемчужны, И моря шум, и груды скал, И гордой девы идеал, И безыменные страданья. . . Другие дни, другие сны; Смирились вы, моей весны Высокопарные мечтанья, И в поэтический бокал Воды я много подмешал
10 Какие б чувства не таились Тогда во мне — теперь их нет: Они прошли иль изменились. . . Мир вам, тревоги прошлых лет! В ту пору мне казались нужны Пустыни, волн края жемчужны, И моря шум, и груды скал, И гордой девы идеал, И безыменные страданья. . . Другие дни, другие сны; Смирились вы, моей весны Высокопарные мечтанья, И в поэтический бокал Воды я много подмешал
 11 КИСЛОТНО-ОСНОВНОЕ РАВНОВЕСИЕ Имеющую огромное значение для химии чистую воду. . . можно рассматривать как слабую кислоту или слабое основание. С. Аррениус Ионное произведение воды Вода в малой степени ионизирована по уравнению: H 2 O H + + OH –. Константа диссоциации К дисс , в соответствии с законом действующих масс, выразится уравнением: ][ ]]·[[ 2 OH OHH К д
11 КИСЛОТНО-ОСНОВНОЕ РАВНОВЕСИЕ Имеющую огромное значение для химии чистую воду. . . можно рассматривать как слабую кислоту или слабое основание. С. Аррениус Ионное произведение воды Вода в малой степени ионизирована по уравнению: H 2 O H + + OH –. Константа диссоциации К дисс , в соответствии с законом действующих масс, выразится уравнением: ][ ]]·[[ 2 OH OHH К д
 12 При 25 °С К д =1. 8· 10 -16 Концентрацию молекул воды как в чистой воде, так и в разбавленных водных растворах можно считать величиной постоянной и равной: . [Н 2 О] =1000/18=55. 56 моль/л [Н + ][ОН – ] = К д ·[Н 2 О] = 1. 8· 10 – 16 · 55. 56 = 10 – 14. К д ·[Н 2 О] = K w Ионное произведение воды: K w =[Н + ][ОН – ] = 10 – 14 ( 25° С ) В чистой воде при температуре 25 °С: 7 w 10 K][OH][H Моль-экв/л.
12 При 25 °С К д =1. 8· 10 -16 Концентрацию молекул воды как в чистой воде, так и в разбавленных водных растворах можно считать величиной постоянной и равной: . [Н 2 О] =1000/18=55. 56 моль/л [Н + ][ОН – ] = К д ·[Н 2 О] = 1. 8· 10 – 16 · 55. 56 = 10 – 14. К д ·[Н 2 О] = K w Ионное произведение воды: K w =[Н + ][ОН – ] = 10 – 14 ( 25° С ) В чистой воде при температуре 25 °С: 7 w 10 K][OH][H Моль-экв/л.
 13 В соответствии с принципом Ле Шателье при добавлении кислот или оснований равновесие H 2 O H + + OH – смещается: В кислой среде: [Н + ] >10 – 7 , [ОН ‑ ] < 10 – 7 , В щелочной среде зависимость обратная
13 В соответствии с принципом Ле Шателье при добавлении кислот или оснований равновесие H 2 O H + + OH – смещается: В кислой среде: [Н + ] >10 – 7 , [ОН ‑ ] < 10 – 7 , В щелочной среде зависимость обратная
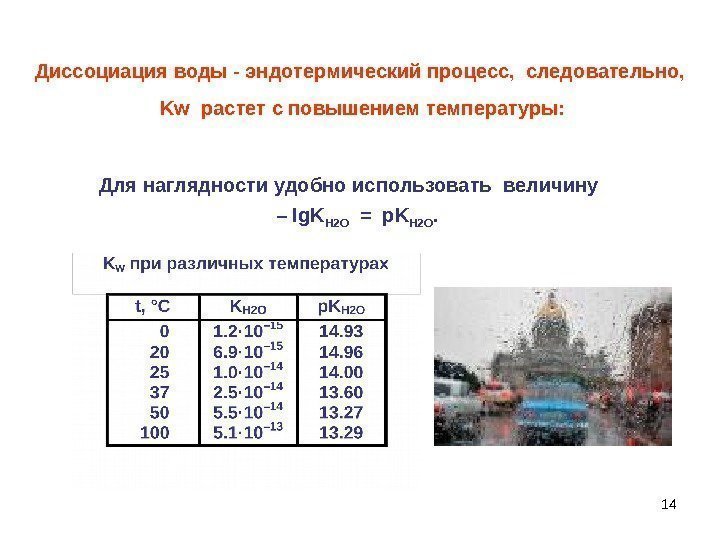
 14 Диссоциация воды — эндотермический процесс, следовательно, Kw растет с повышением температуры: Для наглядности удобно использовать величину – lg. K Н 2 О = p. K Н 2 О.
14 Диссоциация воды — эндотермический процесс, следовательно, Kw растет с повышением температуры: Для наглядности удобно использовать величину – lg. K Н 2 О = p. K Н 2 О.
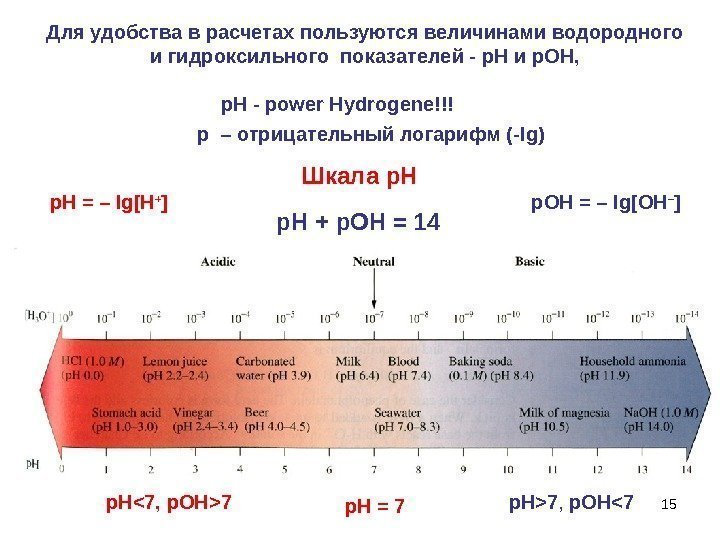
 15 Для удобства в расчетах пользуются величинами водородного и гидроксильного показателей — р H и р. ОН, p. H — power Hydrogene!!! р. Н = 7 р. Н7 р. Н>7 , р. ОН<7 р. Н + р. ОН = 14 р. Н = – lg [ H + ] Шкала р. Н р. ОН = – lg [ OH – ]р – отрицательный логарифм (- lg )
15 Для удобства в расчетах пользуются величинами водородного и гидроксильного показателей — р H и р. ОН, p. H — power Hydrogene!!! р. Н = 7 р. Н7 р. Н>7 , р. ОН<7 р. Н + р. ОН = 14 р. Н = – lg [ H + ] Шкала р. Н р. ОН = – lg [ OH – ]р – отрицательный логарифм (- lg )

 17 Для чистой воды р. Н=7 Дождевая вода за счет растворенного СО 2 имеет р. Н ~ 5. 5 – 6.
17 Для чистой воды р. Н=7 Дождевая вода за счет растворенного СО 2 имеет р. Н ~ 5. 5 – 6.
 18 Памятник Джорджу Вашингтону в Нью-Йорке в момент открытия и через 60 лет. Мрамор Са. СО 3 под действием слабокислой дождевой среды переходит в растворимый гидрокарбонат Са(НСО 3 )
18 Памятник Джорджу Вашингтону в Нью-Йорке в момент открытия и через 60 лет. Мрамор Са. СО 3 под действием слабокислой дождевой среды переходит в растворимый гидрокарбонат Са(НСО 3 )
 19 Бронзовый памятник во влажном воздухе медленно покрывается налетом основного карбоната меди (Сu. OH) 2 CO
19 Бронзовый памятник во влажном воздухе медленно покрывается налетом основного карбоната меди (Сu. OH) 2 CO
 20 Александр Федорович Тур (1894– 1974) 1930 -1934 -заведующий кафедрой физиологии, гигиены и диететики ребенка 1934 -1939 — заведующий кафедрой пропедевтики детских болезней 1939 -1974 — заведующий кафедрой госпитальной педиатрии А. Ф. Тур разрабатывал следующие научные проблемы: физиологические особенности и воспитание здоровых детей гематология и диететика здорового и больного ребенка физиология и патология здорового и больного ребенка выхаживание новорожденных и недоношенных детей дистрофия у детей в годы блокады рахит и его профилактика, детская эндокринология Лауреат Ленинской премии (1970 г. )
20 Александр Федорович Тур (1894– 1974) 1930 -1934 -заведующий кафедрой физиологии, гигиены и диететики ребенка 1934 -1939 — заведующий кафедрой пропедевтики детских болезней 1939 -1974 — заведующий кафедрой госпитальной педиатрии А. Ф. Тур разрабатывал следующие научные проблемы: физиологические особенности и воспитание здоровых детей гематология и диететика здорового и больного ребенка физиология и патология здорового и больного ребенка выхаживание новорожденных и недоношенных детей дистрофия у детей в годы блокады рахит и его профилактика, детская эндокринология Лауреат Ленинской премии (1970 г. )
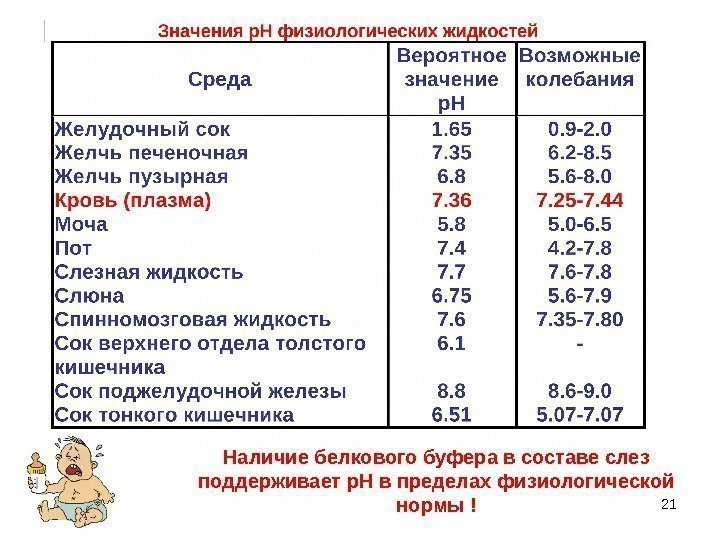
 21 Наличие белкового буфера в составе слез поддерживает р. Н в пределах физиологической нормы !
21 Наличие белкового буфера в составе слез поддерживает р. Н в пределах физиологической нормы !
 22 Электролиты – вещества, растворы и расплавы которых проводят электрический ток вследствие диссоциации на ионы. Расчет р. Н в растворах сильных и слабых электролитах
22 Электролиты – вещества, растворы и расплавы которых проводят электрический ток вследствие диссоциации на ионы. Расчет р. Н в растворах сильных и слабых электролитах
 23 Сильные электролиты диссоциируют полностью, необратимо, в одну ступень. 2 4 3 32 SOAl , Cl. HHCl 342)(SOAl c a 0)(c 1 im 1 0 ·c, a f ff a – активность иона f – коэффициент активности, учитывающий межионное взаимодействие
23 Сильные электролиты диссоциируют полностью, необратимо, в одну ступень. 2 4 3 32 SOAl , Cl. HHCl 342)(SOAl c a 0)(c 1 im 1 0 ·c, a f ff a – активность иона f – коэффициент активности, учитывающий межионное взаимодействие

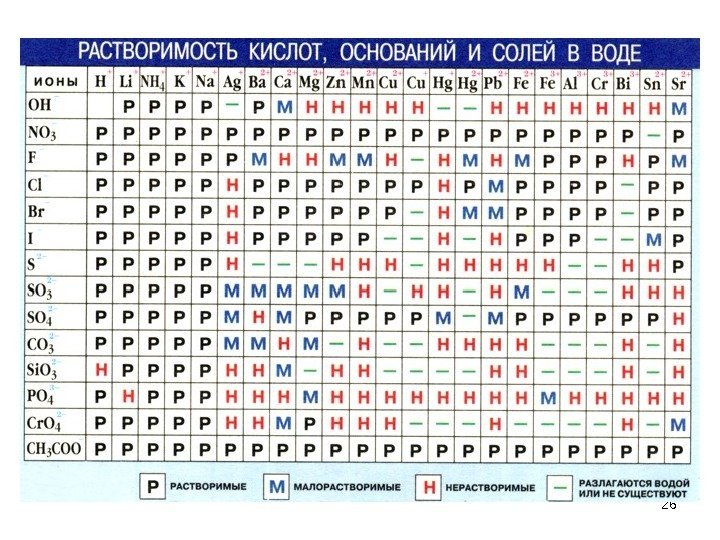
 25 К сильным электролитам относятся: 1. Кислоты — НС I , НВг , HI , H 2 S О 4 , H 2 S 2 O 7 , HN О 3 , HCI О 4 , HCI О 3 , H М n О 4 , H 2 Cr О 4 H 2 Cr 2 О 7 2. Щелочи: I группа — Li. OH, Na. OH , KOH , Rb. OH , Cs. OH II группа — Ca ( OH ) 2 Sr ( OH ) 2 Ba ( OH ) 2 3. Все растворимые соли (см. таблицу растворимости)
25 К сильным электролитам относятся: 1. Кислоты — НС I , НВг , HI , H 2 S О 4 , H 2 S 2 O 7 , HN О 3 , HCI О 4 , HCI О 3 , H М n О 4 , H 2 Cr О 4 H 2 Cr 2 О 7 2. Щелочи: I группа — Li. OH, Na. OH , KOH , Rb. OH , Cs. OH II группа — Ca ( OH ) 2 Sr ( OH ) 2 Ba ( OH ) 2 3. Все растворимые соли (см. таблицу растворимости)

 27 Ионная сила растворов — величина, измеряемая полусуммой произведений концентраций всех находящихся в растворе ионов на квадрат их заряда (понятие введено Г. Льюисом ) 2 nn 2 222 11 z. C. . . z. CI 21 Ионная сила – удобная характеристика раствора, учитывающая взаимодействие ионов, что важно для изучения биологических систем и физиологических растворов, ионная сила которых, в том числе и 0. 9% (0. 15 м) Na. CI равна, как правило, 0. 15. Ионная сила характеризует общее число ионных зарядов в единице объема, независимо от их знаков. Размерность — обратна размерности объема.
27 Ионная сила растворов — величина, измеряемая полусуммой произведений концентраций всех находящихся в растворе ионов на квадрат их заряда (понятие введено Г. Льюисом ) 2 nn 2 222 11 z. C. . . z. CI 21 Ионная сила – удобная характеристика раствора, учитывающая взаимодействие ионов, что важно для изучения биологических систем и физиологических растворов, ионная сила которых, в том числе и 0. 9% (0. 15 м) Na. CI равна, как правило, 0. 15. Ионная сила характеризует общее число ионных зарядов в единице объема, независимо от их знаков. Размерность — обратна размерности объема.
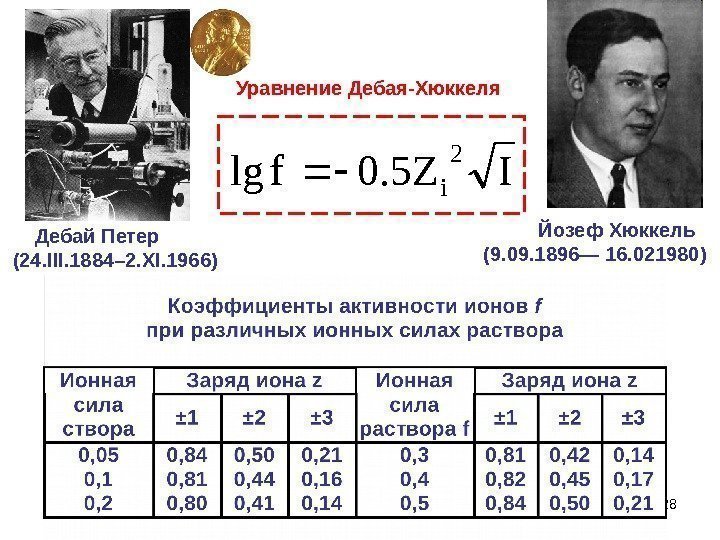
 28 Уравнение Дебая-Хюккеля. IZ 5. 0 flg 2 i Дебай Петер (24. III. 1884– 2. XI. 1966) Йозеф Хюккель (9. 09. 1896— 16. 021980)
28 Уравнение Дебая-Хюккеля. IZ 5. 0 flg 2 i Дебай Петер (24. III. 1884– 2. XI. 1966) Йозеф Хюккель (9. 09. 1896— 16. 021980)
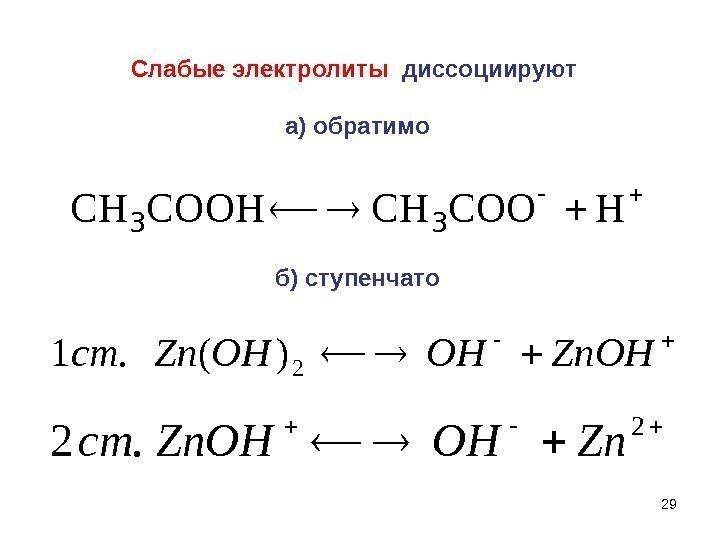
 29 Слабые электролиты диссоциируют а) обратимо HCOOCHCOOHCH 33 2. 2 Zn. OHст б) ступенчато Zn. OHOHOHZncт 2 )(.
29 Слабые электролиты диссоциируют а) обратимо HCOOCHCOOHCH 33 2. 2 Zn. OHст б) ступенчато Zn. OHOHOHZncт 2 )(.
 30 Степень диссоциации (ионизации) — отношение числа молекул, распавшихся на ионы, к общему числу молекул в растворе. α зависит от: Природы вещества и растворителя; Концентрации; Температуры; Присутствия одноименного иона. 10 общ. диссоц. , n n
30 Степень диссоциации (ионизации) — отношение числа молекул, распавшихся на ионы, к общему числу молекул в растворе. α зависит от: Природы вещества и растворителя; Концентрации; Температуры; Присутствия одноименного иона. 10 общ. диссоц. , n n
 31 Закон разведения Оствальда Нобелевская премия (1909 г) « в знак признания работ по катализу, а также за исследования основных принципов управления химическим равновесием и скоростями реакций» (02. 09. 1853 – 4. 06. 1932)α 1 α 2 C Кд В 1887 г. – Лейпцигском университете создал первую в истории науки кафедру физической химии, где работали более 60 химиков многих стран: нобелевские лауреаты С. Аррениус, В. Нернст, У. Рамзай, Ф. Габер и русские ученые И. А. Каблуков, П. И. Вальден, Н. Д. Зелинский и другие. Ученики Оствальда говорили: «Стоит только поговорить с Оствальдом полчаса, и ты будешь иметь работу на полгода» 10 , общ. диссоц. С С
31 Закон разведения Оствальда Нобелевская премия (1909 г) « в знак признания работ по катализу, а также за исследования основных принципов управления химическим равновесием и скоростями реакций» (02. 09. 1853 – 4. 06. 1932)α 1 α 2 C Кд В 1887 г. – Лейпцигском университете создал первую в истории науки кафедру физической химии, где работали более 60 химиков многих стран: нобелевские лауреаты С. Аррениус, В. Нернст, У. Рамзай, Ф. Габер и русские ученые И. А. Каблуков, П. И. Вальден, Н. Д. Зелинский и другие. Ученики Оствальда говорили: «Стоит только поговорить с Оствальдом полчаса, и ты будешь иметь работу на полгода» 10 , общ. диссоц. С С
 32 CC — 3 СС 3 H COOHC COOHHC 1α α 1 α α αα 2 3 3 , C CC CC COOH][CH ]][HCOO[CH Кд 2 д C·αКПри <<1 /СКα д ·СК][Hд ·СК/СКC·C][Hддд 2 αВывод закона разведения Оствальда
32 CC — 3 СС 3 H COOHC COOHHC 1α α 1 α α αα 2 3 3 , C CC CC COOH][CH ]][HCOO[CH Кд 2 д C·αКПри <<1 /СКα д ·СК][Hд ·СК/СКC·C][Hддд 2 αВывод закона разведения Оствальда
 332. Степень диссоциации кислоты HX равна 0, 25. Какое суммарное число ионов H + и X — приходится в ее растворе на каждые 100 нераспавшихся молекул (ответ округлите до целого числа)? 1) 16 2) 33 3) 67 4) 8510 , общ. диссоц. С С 1. На каждые 20 нераспавшихся молекул кислоты HX приходится 5 ионов H + и 5 ионов X -. Укажите степень диссоциации кислоты: 1) 0, 05 2) 0, 10 3) 0, 15 4) 0,
332. Степень диссоциации кислоты HX равна 0, 25. Какое суммарное число ионов H + и X — приходится в ее растворе на каждые 100 нераспавшихся молекул (ответ округлите до целого числа)? 1) 16 2) 33 3) 67 4) 8510 , общ. диссоц. С С 1. На каждые 20 нераспавшихся молекул кислоты HX приходится 5 ионов H + и 5 ионов X -. Укажите степень диссоциации кислоты: 1) 0, 05 2) 0, 10 3) 0, 15 4) 0,
 34 Расчет р. Н в растворах сильных электролитах Рассчитать р. Н, р. ОН, [ OH — ] для 0, 001 м Н NO 3 11 p. OH 3 33 1010][OH 113– 14 p. OH 310 lgp. H NO H HNO p. H 14 p. OH p. H 10][OH ; 10][H р. Н = 14 — р. ОН = 14 — р. Н ][2 OН К Н ОН ][ 2 НК ОН ОН
34 Расчет р. Н в растворах сильных электролитах Рассчитать р. Н, р. ОН, [ OH — ] для 0, 001 м Н NO 3 11 p. OH 3 33 1010][OH 113– 14 p. OH 310 lgp. H NO H HNO p. H 14 p. OH p. H 10][OH ; 10][H р. Н = 14 — р. ОН = 14 — р. Н ][2 OН К Н ОН ][ 2 НК ОН ОН
 35 Задача 1. р. Н яблочного сока равен 4, 57. Найти [Н + ] и [ OH — ] (моль/л). экв/л-моль1072. 3 1069. 2 10 ][ 10 514 2 Н К ОН ОН p. OH 10][OH р. ОН = 14 — р. Н экв/л-моль1069. 2 1010 5 43. 05 4. 57 -p. H 1010][H
35 Задача 1. р. Н яблочного сока равен 4, 57. Найти [Н + ] и [ OH — ] (моль/л). экв/л-моль1072. 3 1069. 2 10 ][ 10 514 2 Н К ОН ОН p. OH 10][OH р. ОН = 14 — р. Н экв/л-моль1069. 2 1010 5 43. 05 4. 57 -p. H 1010][H

![37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11 37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_36.jpg) 37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11 ][H кдкд KCКС Расчет [ Н + ] и р. Н для растворов слабых электролитов Кислоты Смесь кислот
37)(кд(к) ·CК][H ) lg 2 1 (кд (к) Cp. Кp. H )(22)( 11 ][H кдкд KCКС Расчет [ Н + ] и р. Н для растворов слабых электролитов Кислоты Смесь кислот
![38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH 38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_37.jpg) 38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH . )( lg 142 1 оснд (осн. ) Cp. Кp. H . )( 22. )( 11 — ][OH осн. Д KCКC Для смеси оснований Основания
38. )(оснд (осн. ) ·CК] [OH. )(lg 2 1 оснд(осн. ) Cp Кp. OH . )( lg 142 1 оснд (осн. ) Cp. Кp. H . )( 22. )( 11 — ][OH осн. Д KCКC Для смеси оснований Основания
![39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0, 39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0,](http://present5.com/presentforday2/20170109/03-1_shkala_rn_images/03-1_shkala_rn_38.jpg) 39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0, 3 м раствора муравьиной кислоты (Кд=1. 8 · 10 -4 )экв/л-моль 103. 73. 0108. 1 34 ) (кд(к)·CК][H р. Н = – lg [ H + ] = – lg 7. 3 · 10 -3 = – lg 7. 3 – lg 10 -3 = = 3 – lg 7. 3=3 -0. 86 = 2.
39 Задача 2. Найти р. Н, [Н+] и [ OH -] 0, 3 м раствора муравьиной кислоты (Кд=1. 8 · 10 -4 )экв/л-моль 103. 73. 0108. 1 34 ) (кд(к)·CК][H р. Н = – lg [ H + ] = – lg 7. 3 · 10 -3 = – lg 7. 3 – lg 10 -3 = = 3 – lg 7. 3=3 -0. 86 = 2.
 40 Общая, активная и потенциальная кислотность Активная кислотность – концентрация свободных катионов Н + , имеющихся в растворе при данных условиях. Мерой активной кислотности является значение р. Н раствора: p. H = -lg[H + ] Потенциальная кислотность – концентрация катионов Н+, связанных в молекулы или ионы слабых кислот, имеющихся в растворе. Сильные кислоты: [H + ] акт = [H + ] общ, [H + ] пот =0. Слабые кислоты: [H + ] общ = [H + ] пот + [H + ] акт [H + ] пот > > [H + ] акт H COOHH 33 — CC Cl. HHCl
40 Общая, активная и потенциальная кислотность Активная кислотность – концентрация свободных катионов Н + , имеющихся в растворе при данных условиях. Мерой активной кислотности является значение р. Н раствора: p. H = -lg[H + ] Потенциальная кислотность – концентрация катионов Н+, связанных в молекулы или ионы слабых кислот, имеющихся в растворе. Сильные кислоты: [H + ] акт = [H + ] общ, [H + ] пот =0. Слабые кислоты: [H + ] общ = [H + ] пот + [H + ] акт [H + ] пот > > [H + ] акт H COOHH 33 — CC Cl. HHCl

 42 Спасибо за внимание!
42 Спасибо за внимание!

