Копия Лекция IIБ.ppt
- Количество слайдов: 48

1. Общая характеристика d-элементов IIБ группы n n n Строение внешних электронных оболочек атомов d -элементов описывается общей формулой (n-1)dansb, a=1 10, b=1 2. Предпоследний электронный слой d-элементов II группы состоит из 18 электронов, что определяет его высокую стабильность и особенности химических свойств этих элементов Металлические свойства ослабевают от цинка к ртути. Комплексообразование возможно за счет свободных орбиталей ионов металлов и за счет неподеленных пар dэлектронов (n-1)слоя. q Координационное число цинка 4 (очень редко – 6) K 2 Zn(OH)4 q Кадмия – 4 и 6 - Cd(NH 3)6 Cl 2 q Ртути - 4 - K 2 Hg. J 4

1. 1. БИОЛОГИЧЕСКАЯ РОЛЬ Hg Cd Zn n n В ряду: Hg>Cd>Zn уменьшается токсичность. Ртуть и кадмий не являются необходимыми элементами для человека. Источники кадмиевой интоксикации: q промышленные загрязнения (риск развития онкозаболеваний) q сигаретный дым (в 20 сигаретах содержится 15 -18 мг кадмия) q употребление в пищу продуктов моря, особенно устриц (В Японии заболевание, вызванное отравлением кадмием, известно под названием «itai-itai). n В некоторых странах соли кадмия используются как антигельминтные и антисептические препараты в ветеринарии. n Ртуть - это единственный металл, представляющий собой при комнатной температуре жидкость. n Применялись: q каломель (Hg 2 Cl 2) - как местный антисептик; q раствор сулемы (Hg. Cl 2) - для дезинфекции; антисептик q ртутная серная мазь (содержит около 30% металлической ртути), до 2002 г применялась наружно при кожных паразитарных заболеваниях (педикулез) и при сифилисе. n

n n Цинк является простетическим центром многих ферментов, связывается с гексамерами инсулина. Является металлом–антиоксидантом и проявляет синергический эффект (т. е. веществом, способствующим проявлению их действия) с природным антиоксидантом – витамином Е Человек поглощает 10— 15 мг цинка в день. Наиболее высокая концентрация цинка (15 ммоль)обнаружена в предстательной железе. Ионы цинка в ферментах часто могут быть заменены ионами Mn 2+ и Co 2+ или некоторыми другими ионами без существенного снижения каталитической активности. С цинком конкурируют Cu 2+ и очень токсичный Cd 2+.

n n n n Цинк входит в состав ферментов и комплексов, обеспечивающие важнейшие физиологические функции организма: образование, рост и метаболизм клеток, синтез белков, заживление ран; активизация имунных реакций; усвоение углеводов и жиров; поддержание и улучшение памяти; поддержание обонятельной и вкусовой деятельности; обеспечение стабильности сетчатки и прозрачности хрусталика глаза; нормальное развитие и функционирование половых органов.

2. Цинка оксид n n n Zn. O Zinci oxydum M 81, 38 Получение - прокаливание цинкового шпата: Zn. CO 3 Zn. O+CO 2 - прокаливание свежеосажденного основного карбоната цинка, который получают при взаимодействии горячего раствора кристаллической соды с водным раствором сульфата цинка: 5 Zn. SO 4 + 5 Na 2 СО 3 + ЗН 2 О 2 Zn. CO 3. 3 Zn(OH)2+ 5 Na 2 SO 4 + ЗСО 2 Осадок основного карбоната цинка отстаивают и после слива жидкости отмывают от сульфат-ионов. После просушивания осадок основного карбоната цинка прокаливают до прекращения выделения CO 2: 2 Zn. CO 3. 3 Zn(OH)2 ЗН 2 О + 2 CO 2 + 5 Zn. O

2. 1. Описание n n В чистом виде оксид цинка представляет собой белый или с желтоватым оттенком аморфный порошок, нерастворимый в воде и спирте. Поглощает углекислый газ из воздуха. Zn. O + СО 2 Zn. СO 3 Растворим в минеральных и уксусной кислотах: Zn. O+2 HCl Zn. Cl 2+H 2 O Растворим в щелочах, при этом сначала образуется гидроксид цинка, который растворяется в избытке реактива с образованием гидроксокомплекса цинка: Zn. Cl 2 + 2 Na. OH 2 Na. Cl + Zn(OH)2 Na. OH 2 Na. OH Zn. O Zn(OH)2 Na 2 [Zn(OH)4] белый тетрагидроксицинкат натрия (раствор) В избытке раствора аммиака оксид цинка образует комплексные аммиакаты цинка: Zn. O + 4 NH 3 + Н 2 О [Zn(NН 3)4](ОН)2 (комплексный аммиакат цинка)

2. 2. Определение подлинности n n Перед испытанием на подлинность оксида цинка его переводят в растворимое соединение, добавляя кислоту или щелочь, так как это амфотерный оксид. Обычно добавляют разведенную хлороводородную кислоту, а далее – проводят реакции на ион цинка по «Общим реакциям подлинности» . Характерной реакцией на Zn 2+ является реакция с Na 2 S. В отличие от солей других тяжелых металлов сульфид натрия в кислой среде осаждает из солей цинка сульфид цинка (Zn. S) белого цвета: Zn. O+2 HCl Zn. Cl 2+H 2 O Zn 2+ + S 2 - Zn. S белый Следует учитывать, что при переводе оксида цинка в ион цинка с помощью хлороводородной кислоты не должно быть ее переизбытка, в противном случае сульфид цинка не образуется, он легко растворяется в избытке хлороводородной кислоты - р. Н<2 (поэтому избыток кислоты нейтрализуют, реакция среды должна быть нейтральной). Сульфид цинка нерастворим в уксусной кислоте.

n n Реакция с раствором гексацианоферрата (II) калия: выпадает светло-желтый кристаллический осадок двойной соли, нерастворимый в кислотах, но растворимый в щелочах: 3 Zn. SO 4 + 2 K 4[Fe(CN)6] K 2 Zn 3[Fe(CN)6]2 + 3 K 2 SO 4 светло-желтый t, 0 C Zn. O Специфичной нефармакопейной реакцией на цинк во всех его соединениях является реакция образования зелени Ринмана состава от Zn. Co 2 O 4 до Zn. Co. O 2 , которую получают при прокаливании с нитратом кобальта осажденных гидроксо-карбонатов или спеканием оксидов: (Zn. OH)2 CO 3 + 4 Co. NO 3 = 2 Zn. Co 2 O 4 + 5 CO 2 + 2 NO+ 3 H 2 O Zn. O + Co. O = Zn. Co. O 2 Если содержание Co. O превышает 70%, то смесь получается не зеленого, а розового цвета.

2. 3. Оценка чистоты n n n Допустимые примеси: железо, алюминий, медь, свинец, кадмий, мышьяк, карбонаты. Для обнаружения примесей ионов металлов, а именно железа, меди и алюминия используют общий реактив – раствор аммиака: Fe(ОН)3 (бурый осадок) Zn. O + NH 3. Н 2 О Сu(NH 3)4 (ОН)2 (синий цвет) Al(OH)3 (белый осадок) При этом не должно образовываться окрашивания раствора. Катионы цинка не мешают определению, т. к. он с аммиаком образует бесцветный раствор аммиаката цинка - Zn(NH 3)4 2+. Для обнаружения примеси свинца используют реакцию получения нерастворимого в уксусной кислоте желтого хромата свинца: Рb(СН 3 СОО)2 + К 2 Сr. О 4 + CH 3 COOH Рb. Сr. O 4 + 2 CH 3 COOK желтый Традиционную реакцию с Na 2 S или (NH 4)2 S не применяют, так как данная реакция позволяет обнаружить не только свинец, но и другие тяжелые металлы. Карбонаты определяют по выделению углекислого газа прибавлении хлороводородной кислоты: Zn. СO 3 +НСl Zn. Сl 2 + СO 2 + Н 2 О

2. 4. Количественное определение n Количественное определение оксида цинка в препарате проводят комплексонометрическим методом. Предварительно препарат растворяют в хлороводородной кислоте. В качестве индикатора, используют кислотный хром черный специальный в аммиачном буферном растворе. Аммиачный буфер добавляют для связывания ионов водорода, которые образуются при титровании трилоном Б Zn О + HCl → Zn. Cl 2 Ind 2 - + Zn 2+ → Zn. Ind Красно-фиолетовый n n Zn. Ind + H 2 Y → Zn. Y 2 - +Ind 2 - + 2 H+ Титруют трилоном Б до синего окрашивания (от красно-фиолетового до синего). В пересчете на Zn. O должно быть 99 -100, 5% вещества.

n n Определение цинка проводится в слабокислой среде, в качестве буфера применяется гексаметилентетрамин (СН 2)6 N 4 , индикатор – ксиленоловый оранжевый (р. Н 1 -3). (Гексаметилентетрамин проявляет основные свойства и может реагировать с кислотами как однокислотное основание. ЭДТА разрушает комплекс индикатора со всеми металлами). Zn. O +НСl Zn. Сl 2 HInd 2 - + Zn 2+ Zn. Ind- + H+ Zn 2+ + H 2 Y ↔Zn. Y 2 - + 2 H+ Zn. Ind- + H 2 Y Zn. Y 2 - + HInd 2(СН 2)6 N 4 + НСl (СН 2)6 N 4. НСl (соль)

2. 5. Применение и хранение n n n Применяется оксид цинка наружно как вяжущее, адсорбирующее, подсушивающее, антисептическое средство в виде присыпок, мазей и паст. (Оксид цинка образует альбуминаты, денатурирует белки). Применяется при опрелостях, потнице, пролежнях, дерматитах, вызванных обветриванием кожи. Входит в состав готовых лекарственных средств, например детская присыпка, цинковая мазь. Содержится в специальных бинтах для перевязки ног при венозных ранах. Хранить препарат следует в плотно закрытой таре без доступа воздуха, чтобы не попадала углекислота. При неправильном хранении оксид цинка может поглощать углекислый газ и образуется карбонат цинка: Zn. O + СО 2 Zn. СO 3

3. Цинка сульфат Zinci sulfas Zn. SO 4. 7 Н 2 O Mr 287, 54 n n n Сульфат цинка применялся в медицине издавна под названием белого купороса. Такое название объясняется тем, что эта соль бесцветна в отличие от медного и железного купороса. Получение. Сульфат цинка получают растворением цинка или его оксида в разбавленной серной кислоте: Zn + H 2 SO 4 Zn. SO 4 + H 2 Zn. O + H 2 SO 4 Zn. SO 4 + H 2 O Обычно сырье для получения сульфата цинка бывает загрязнено такими примесями, как медь, свинец, кадмий, железо. Медь, свинец и кадмий не растворяются в разбавленой серной кислоте. А для освобождения от примеси железа, раствор обрабатывают пероксидом водорода: 2 Fe. SO 4 + Н 2 SО 4 + Н 2 О 2 Fe 2(SO 4)3 + 2 Н 2 O К раствору образующегося сульфата железа(III) добавляют оксид цинка в присутствии воды. Осадок гидроксида железа(III) отфильтровывают, а раствор, содержащий Zn. SO 4, упаривают до образования кристаллов соли.

n n n 3. 1. Описание. Сульфат цинка представляет собой бесцветные прозрачные кристаллы или мелкокристаллический порошок вяжущего металлического вкуса без запаха. Очень легко растворим в воде, практически не растворим в спирте. Медленно растворим в глицерине (1: 10). На воздухе выветривается. 3. 2. Подлинность Zn 2+ + S 2 - Zn. S белый 3 Zn. SO 4 + 2 K 4[Fe(CN)6] K 2 Zn 3[Fe(CN)6]2 + 3 K 2 SO 4 светло-желтый Ва 2++ SО 42 - Ва. SО 4

3. 3. Оценка чистоты n n Допустимые примеси: хлориды, алюминий, железо, медь (определяются с раствором аммиака); Определяется кислотность ( р. Н = 4, 4 - 5, 6 определение наличия примеси кислоты в процессе получения). 3. 4. Количественное определение Содержание Zn. SO 4 в препарате может быть определено тем же методом, что и для оксида цинка, (с примененикм индикатора ксиленолового оранжевого и ацетатного буферного раствора). Содержание вещества - 99 -104%.

3. 5. Применение n n n Цинка сульфат - антисептическое, вяжущее, иммуномодулирующее средство. Применяют при коньюктивите, ларингите в виде 0, 1 -0, 5% растворов. Внутрь применяют при дефиците цинка в организме, (гипогонадизме), облысении, церебральном параличе, заболеваниях печени, сахарном диабете, болезни Вильсона. Коновалова (антагонист меди). При приеме внутрь с лечебной целью – 2— 50 мг 2 -3 раза в день. В качестве рвотного средства 100 -300 мг однократно. Таблетки, капсулы, глазные капли (0, 25% раствор – ВР). «Цинкит» (Германия) – 1 драже или 1 шипучая таблетка содержит 44 мг сульфата цинка (10 мг Zn). В виде комбинированного препарата (вместе с борной кислотой) используется при коньюктивитах – 1 -2 капли в пораженный глаз). Хранить его следует с предосторожностью (список Б), в хорошо закупоренной таре. При передозировке возможно отравление солями цинка: тошнота, рвота.

Лекция 9 ЛС на основе d-элементов VIII Б группы ПСЭ Fe, Co, Ni; Ru, Rh, Pd; Os, Ir, Pt

n n Семейство железа: Fe – Co - Ni Легкие платиновые металлы: Ru – Rh - Pd, Тяжелые платиновые металлы: Os – Ir – Pt. В группе сходство между элементами одного периода больше, чем сходство между элементами первого, второго и третьего ряда переходных металлов. Железо и кобальт – жизненно необходимые элементы. Никель входит в состав фермента уреаза. Остальные металлы не являются жизненно необходимыми. Железо, кобальт, никель, родий и палладий при высоких дозах токсичны. Установлена их канцерогенность. Данные по токсичности рутения и иридия малочисленны. Вдыхание паров осмиевой кислоты вызывает раздражение легочной ткани и закупорку просвета бронхов. Простые соли платины слаботоксичны, но хлороплатинаты весьма токсичны. Некоторые соли платины оказывают протиоопухолевое действие, препятствуя репликации ДНК. Токсичность металла в пределах каждой триады возрастает с увеличением атомной массы.
Железо и его соединения Железо содержится в обычных почвах до 4%. В организме здорового человека содержится приблизительно 4 -5 граммов железа. Около 70% всего железа организма входит в состав крови - в эритроцитах ( гемоглобине). Остаток содержится в селезенке, печени и костном мозге.

Железо и его соединения n Железо входит также в состав окислительных ферментов: цитохромов, каталазы, пероксидазы. В связанной форме железо находится в белках, выполняющих в организме роль переносчика железа: q гемоглобине. Простетическая группа гемоглобина комплекс железа (II) с порфирином; q ферритине, является депонирующим белком Fe(III). Содержание железа в ферритине составляет 17 — 23%. (в микроскопии ферритин часто используют как своеобразный маркер);
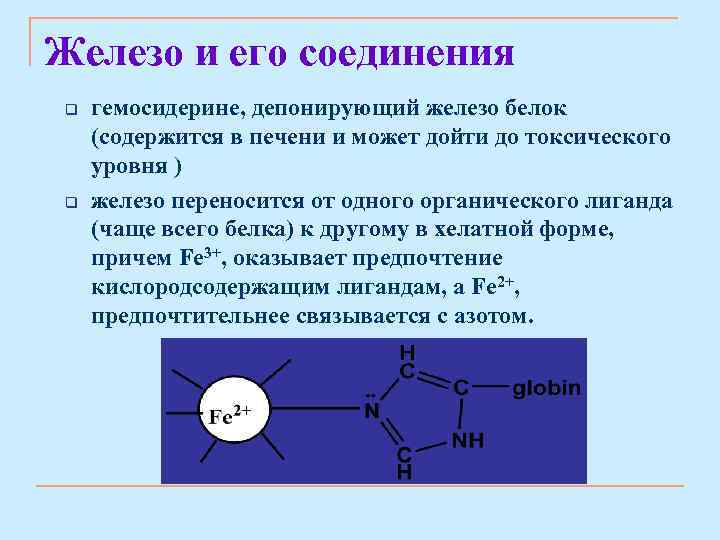
Железо и его соединения q q гемосидерине, депонирующий железо белок (содержится в печени и может дойти до токсического уровня ) железо переносится от одного органического лиганда (чаще всего белка) к другому в хелатной форме, причем Fe 3+, оказывает предпочтение кислородсодержащим лигандам, а Fe 2+, предпочтительнее связывается с азотом.
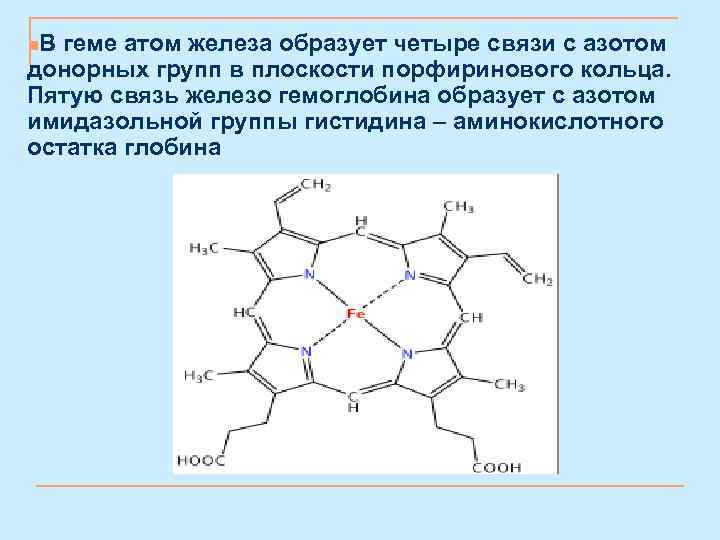
n. В геме атом железа образует четыре связи с азотом донорных групп в плоскости порфиринового кольца. Пятую связь железо гемоглобина образует с азотом имидазольной группы гистидина – аминокислотного остатка глобина

n В среднем суточный рацион человека содержит около 15 мг железа; из них всасывается около 1 мг. Обычно этого достаточно, чтобы компенсировать небольшие потери железа, в основном с желчью. Не выяснен механизм, обеспечивающий выведение из организма избыточных количеств железа; содержание железа регулируется только уровнем его поступления в организм. Этот уровень повышается у женщин во время беременности и у молодых женщин в критические дни (для возмещения потери железа с кровью).

n. Механизм регуляции всасывания железа до конца не выяснен. Считают, что, попав в организм, Fe 3+ связывается с белком трансферрином (молекулярная масса - 80 000 а. е. м. ), содержащим два центра связывания железа. Для переноса железа из трансферрина в гем, находящихся в предшественниках эритроцитов, образующихся в костном мозге, железо (III) восстанавливается до железа (II). Восстановителями являются аскорбиновая кислота или глутатион. (Попав в организм, железо в нем удерживается. В результате ежесуточного разрушения 9 млрд. эритроцитов освобождаются 20 -25 мг железа, которое почти полностью снова используется или резервируется в организме). n
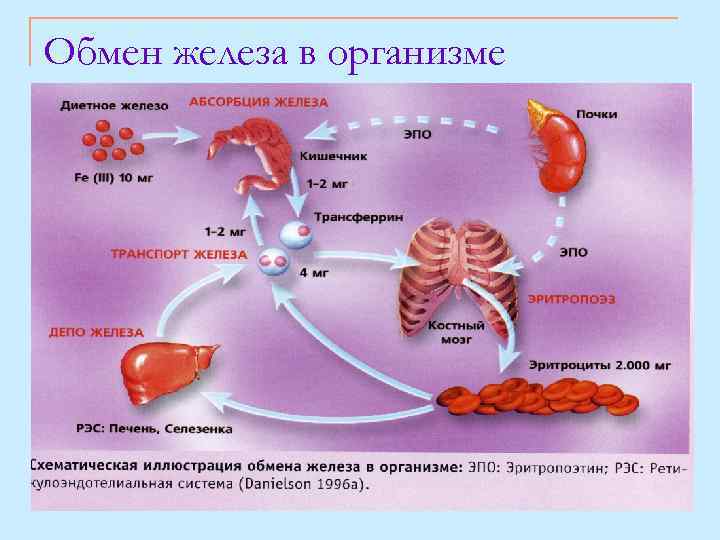
Обмен железа в организме

n n Главной функцией трансферрина является транспорт железа в организме, но он может служить и буфером, регулирующим поступление железа; возможно, всасывание железа через слизистую кишечника регулируется степенью насыщения железом трансферрина в крови. Железосвязывающие белки, находящиеся в жидких средах организма, объединяют в группу с общим названием сидерофилины. Препараты железа применяются главным образом при анемии, малокровии, а также как кровоостанавливающее средство. ЛС на основе железа являются железо восстановленное, сульфат железа(II), комплексные соединения железа и платины.
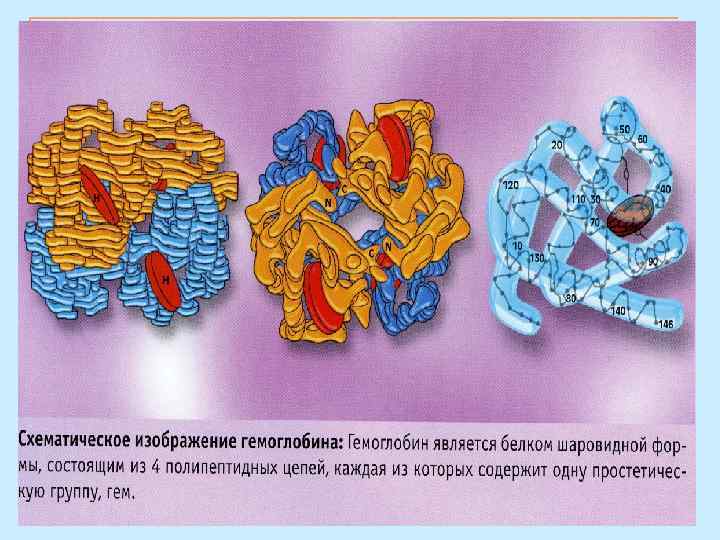

n Молекула гемоглобина: 4 субъединицы глобина окрашены в разные цвета

Железо выполняет в организме следующие функции: n n n участвует в процессах кроветворения и внутриклеточного обмена необходимо для образования гемоглобина и миоглобина обеспечивает транспортировку кислорода в организме нормализует работу щитовидной железы влияет на метаболизм витаминов группы В входит в состав некоторых ферментов (в том числе рибонуклеотид-редуктаз, который участвует в синтезе ДНК) необходимо для процессов роста организма регулирует иммунитет (обеспечивает активность интерферона и клеток-киллеров) оказывает детоксикационное действие (входит в состав печени и принимает участие в обезвреживании токсинов) является компонентом многих окислительных ферментов предупреждает развитие анемии улучшает состояние кожи, ногтей, волос

В случае недостатка железа наблюдаются такие симптомы: n Усталость Ломкость ногтей Депрессия

n n n n Нервные расстройства Выпадение и поседение волос Повышенная чувствительность к холоду Ухудшение мозговой активности Пищеварительные расстройства Головокружения Воспалительный процесс в полости рта Снижение функции щитовидной железы Ожирение

Свекла Яблоко Брокколи Ягоды Для того чтобы не страдать такими заболеваниями нужно употреблять продукты: 1)Растительного происхождения Изюм Шиповник Белые грибы Сухофрукты
Яйца Мясо Железо, которое в них содержится легко усваивается организмом. Поэтому мясные продукты должны обязательно присутствовать в рационе каждого человека не менее 2– 3 раз в неделю. 2)Продукты животного происхождения Творог

Железа(II) сульфат Ferri(II) sulfas n n Fe. SO 4. 7 Н 2 О Получение q Избыток восстановленного железа растворяют в 25 -30% серной кислоте при 80°С в атмосфере углекислого газа. Fe + Н 2 SO 4 Fe. SO 4 + Н 2 q Раствор упаривают без доступа воздуха до выпадения кристаллов, которые сушат при 30°С. Описание q Прозрачные призматические кристаллы светлого голубоватозеленого цвета или кристаллический бледно-зеленый порошок, хорошо растворимый в воде, очень легко - в горячей воде, практически нерастворим в спирте. На воздухе выветривается. Сульфат железа(II) растворим в воде (1: 2, 2) с образованием растворов слабокислой реакции: [Fe(H 2 O)4]2+ + HOH [Fe(H 2 O)3 OH]+ + H 3 O+ Растворимые соли железа (II) с раствором щелочи и аммиака образуют осадок гидроксид железа (III) бурого цвета. Fе 2+ + 2 ОН- Fе(ОН)2 Fе(ОН)3 Соли железа (II) легко окисляются кислородом воздуха до железа (III) и приобретают бурый цвет.

Реакции подлинности на Fe 2+ и Fe 3+ n Для установления подлинности соединений железа в ГФXI описаны два метода (А и Б) идентификации ионов (Fe 2+) и три (А, Б и В) ионов железа (Fe 3+). ГФXI А. n Fе 2+ + K 3[Fe(CN)6] 2 К+ + KFe[Fe(CN)6] Fe 3+ + K 4 [Fe(CN)6] → 3 K+ + KFe[Fe(CN)6]↓ Fe 4[Fe(CN)6]3·n. K 4[Fe(CN)6]·m. H 2 O, где n = 0, 3 -0, 8; m = 12 -24; упрощенно - KFe[Fe(CN)6] (берлинская лазурь, турнбулевая синь, парижская синяя). Fe 2 + + K 4[Fe(CN)6] Fe 2[Fe(CN)6] + 4 K+ окисл. (белый осадок) (KBr. O 3, K 2 Cr 2 O 7) Ионы Fe 3+ с феррицианидом калия (K 3[Fe(CN)6]) осадка не дают, но раствор приобретает темно-бурую окраску.

Реакции подлинности на Fe 2+ и Fe 3+ ГФXI Б n n основан на реакции образования роданидов железа, окрашивающих раствор в красный цвет. Fe 3+ + SCNˉ ↔ [Fe. SCN]2+ Fe 3+ + 2 SCNˉ ↔ [Fe(SCN)2]+ Fe 3+ + 3 SCNˉ ↔ Fe(SCN)3 и т. д. до Fe 3+ + 6 SCNˉ ↔ [Fe(SCN)6]3– Это одна из наиболее специфичных реакций на окисное железо. Вещества, мешающие определению Fe 3+ - фосфорная, щавелевая, винная, лимонная кислоты и их соли.

Реакции подлинности на Fe 2+ и Fe 3+ n Общим реактивом для открытия ионов железа в степени окисления +2 и +3 является сульфид аммония. В обоих случаях выпадают черные осадки сульфидов железа. Fe 2+ + S 2 - Fe. S Fe 3+ + S 2 - Fe. S + S Fe. S + 2 HCl → H 2 S + Fe. Cl 2 Рассмотренные методы определения железа позволяют открыть его лишь в препаратах, содержащих простые соли железа, растворимые в воде, например, железа закисного сульфат, железа закисного лактат, ферамид и др. Препараты, представляющие собой прочные комплексные соединения железа (ферроцерон, оксиферрискарбон натрия) или нерастворимые в воде (таблетки «Каферид» ), предварительно минерализуют с целью перевести железо в раствор.

Определение подлинности n n Сульфат-ион обнаруживают по реакции с раствором хлорида бария. Катион железа (II) обнаруживают по реакцию образования темно-синего осадка турнбулевой сини при действии раствора гексацианоферрата (III) калия: помощью различных реакций. Fе. SO 4 + K 3[Fe(CN)6] 2 К 2 SO 4 + KFe. Fe(CN)6 Осадок нерастворим в минеральных кислотах. Реакция образования сульфида железа при действии сульфида натрия или аммония. Образуется черный осадок, растворимый в хлороводородной кислоте: Fe 2+ + S 2 - Fe. S + 2 HCI Fe. CI 2 + Н 2 S

Оценка чистоты Недопустимая примесь - ионы меди Cu+, Cu 2+. n Навеску препарата окисляют пергидролем, а затем добавляют раствор аммиака. Образуется бурый осадок гидроксида железа(III ). n Раствор фильтруют, на фильтре остается осадок гидроксида железа (III), а полученный фильтрат должен быть бесцветным. Fe 2+ +2 NH 3 + 2 H 2 O Fe(OH)2 + 2 NH 4+ Fe(ОН) 2(суспензия) + О 2(воздух) 4 Fe. О(OH) + 2 H 2 O n В присутствии примеси солей меди раствор окрашивается в темно-синий цвет комплексного аммиаката меди: Cu 2+ + 4 NH 3 [Cu(NH 3)4]2+ Допустимые примеси: хлориды, тяжелые металлы, железо (III), цинк. р. Н = 3, 0 - 4, 0 n
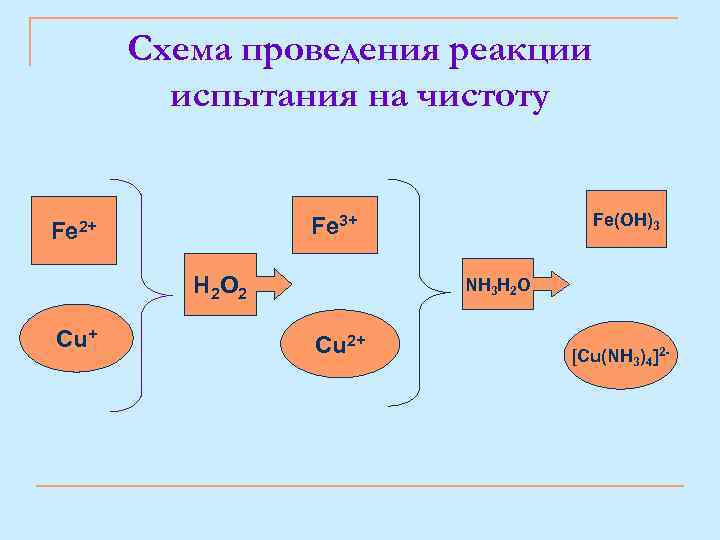
Схема проведения реакции испытания на чистоту H 2 O 2 Cu+ Fe(OH)3 Fe 3+ Fe 2+ NH 3 H 2 O Cu 2+ [Cu(NH 3)4]2 -

Количественное определение n n n Цериметрический метод: Ce 4+ + Fe 2+ → Ce 3+ + Fe 3+ Ионы Ce 4+ - окрашены в желтый или желто-оранжевый цвет, а ионы Ce 3+ бесцветны. Титрование ведут до исчезновения желтой окраски. Можно использовать индикатор 1, 10 -фенантролин, который с Fе 2+ образует комплекс красного цвета (ферроин). Титрование ведут от красного окрашивания до голубого или голубовато-зеленого (восстановленная форма индикатора – красная, окисленная – голубая).
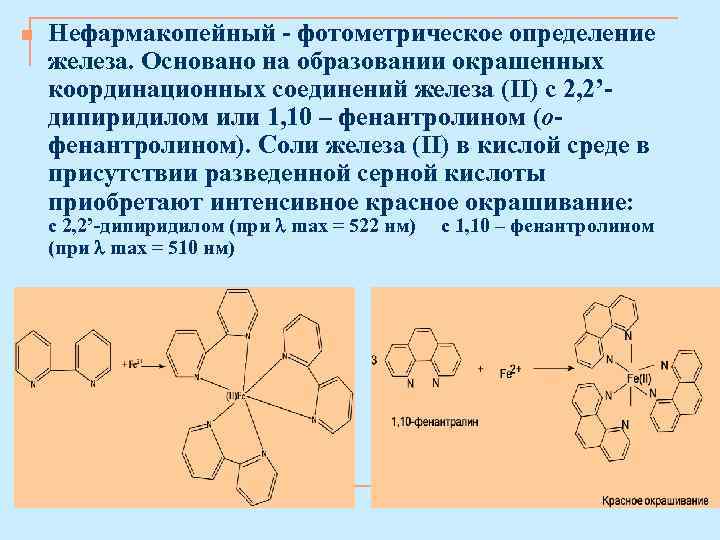
n Нефармакопейный - фотометрическое определение железа. Основано на образовании окрашенных координационных соединений железа (II) с 2, 2’дипиридилом или 1, 10 – фенантролином (офенантролином). Соли железа (II) в кислой среде в присутствии разведенной серной кислоты приобретают интенсивное красное окрашивание: с 2, 2’-дипиридилом (при max = 522 нм) (при max = 510 нм) с 1, 10 – фенантролином

n n Применение В комплексной терапии гипохромных (железодефицитных) анемий. Хранение В хорошо закрытых банках в сухом месте, чтобы не допустить потери кристаллизационной воды в железе (II) сульфате. Железо (II) может также окисляться во влажном воздухе с образованием основной соли Fe 2(OH)4 SО 4. При 64°С железа(II) сульфат плавится в своей кристаллизационной воде.

Препараты железа n n Феррумлек (Ferrum Lek) содержит 0, 1 г железа (III) в виде комплекса с мальтозой (дисахарид – 2 молекулы глюкозы) в 2 мл ампулированного раствора (для внутримышечных инъекций) или 0, 1 г железа сахарата в 5 мл ампулированного раствора (для внутривенного введения). Применяют для лечения гипохромных анемий. Драже ферроплекс (Ferroplex) 0, 05 г железа (II) сульфата и 0, 03 г кислоты аскорбиновой; Таблетки феррокаль (Ferrocalum) содержат 0, 2 г железа (II) сульфата, 0, 1 г кальция фруктозодифосфата и 0, 02 г церебролицетина; Конферон (Conferon) - капсулы, содержащие по 0, 25 г железа(III) сульфата и 0, 035 г диоктилсульфосукцината натрия.

Железа глицерофосфат (Ferri glycerophsphas) n n n Соль железа(III) глицерофосфорной кислоты гидрат Желтый или зеленовато-желтый аморфный порошок с характерным запахом. Практически не растворим в воде, растворим при нагревании в разведенной соляной кислоте. Содержит около 18 % железа(III). Назначают внутрь при гипохромной анемии взрослым по 1 г 3— 4 раза в день, детям по 0, 3 -0, 5 г 2— 3 раза в день. Форма выпуска: порошок. Хранение: в сухом, защищенном от света месте.

Железа лактат Ferri lactas n Описание. Зеленовато-белый кристаллический порошок или сростки мелких игольчатых кристаллов с характерным запахом. Трудно и медленно растворим в холодной воде (1: 50), растворим в кипящей воде (1: 12), практически нерастворим в спирте, легко растворим в разведенных минеральных кислотах. Водные растворы имеют слабокислую реакцию, зеленовато-желтую окраску; при соприкосновении с воздухом раствор не буреет.

n n n Определение подлинности Fe 2+, СН 3 СНОНСОО-. Фармакологическое действие: Препарат Fe 2+, устраняет клинические (слабость, повышенная утомляемость, головокружение, тахикардия, дистрофические изменения кожи) и лабораторные симптомы анемии. Для растворения и диссоциации Fe лактата необходимо наличие в желудке достаточного количества свободной HCl. Железа лактат легче всасывается из желудка, не вызывает раздражения слизистых оболочек. Форма выпуска: таблетки “Гемостимулин”, “Фитоферролактол”, “Каферрид”, “Феррамид”, сироп алое с железом, “гемофер”, “Ферроцерон”. Способ применения В капсулах по 1 г 3 -4 раза в день. Условия храниения В защищенном от света месте.
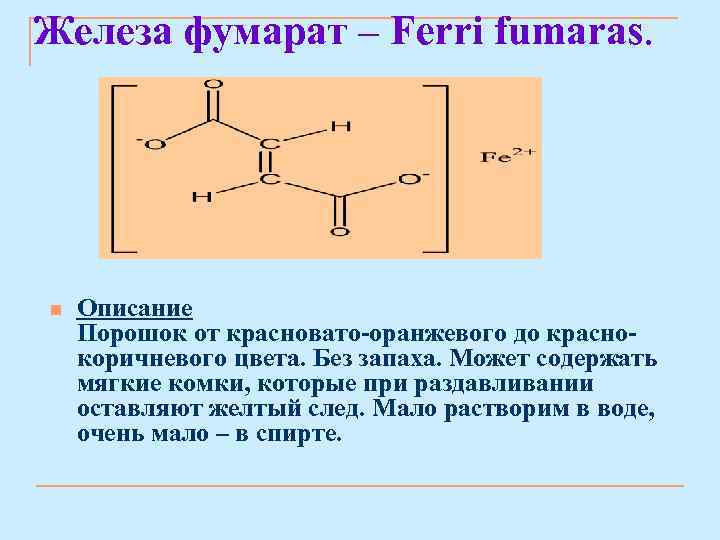
Железа фумарат – Ferri fumaras. n Описание Порошок от красновато-оранжевого до краснокоричневого цвета. Без запаха. Может содержать мягкие комки, которые при раздавливании оставляют желтый след. Мало растворим в воде, очень мало – в спирте.
Копия Лекция IIБ.ppt