1 КИСЛОТА АСКОРБИНОВАЯ Acidum ascorbinicum С6Н8О6 М.м. 176,13

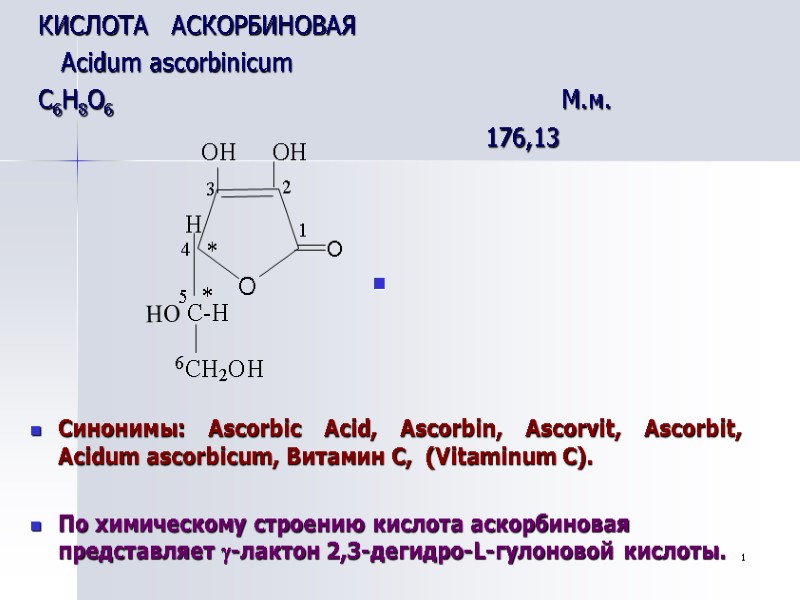
1 КИСЛОТА АСКОРБИНОВАЯ Acidum ascorbinicum С6Н8О6 М.м. 176,13 Cинонимы: Ascorbic Acid, Ascorbin, Ascorvit, Ascorbit, Acidum ascorbicum, Витамин С, (Vitaminum C). По химическому строению кислота аскорбиновая представляет -лактон 2,3-дегидро-L-гулоновой кислоты. O O H C H 2 O H O O H O H H C - H 1 2 3 4 5 6 * *
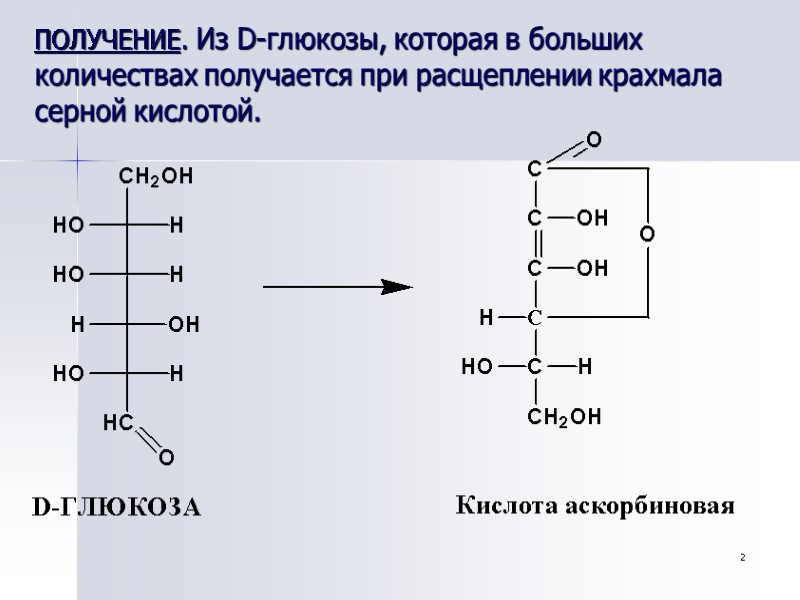
2 ПОЛУЧЕНИЕ. Из D-глюкозы, которая в больших количествах получается при расщеплении крахмала серной кислотой.

3 ОПИСАНИЕ Кислота аскорбиновая – белый кристаллический порошок без запаха, кислого вкуса. РАСТВОРИМОСТЬ. Аскорбиновая кислота легко растворима в воде (1:3,5), хуже в спирте и практически нерастворима в эфире, бензоле и хлороформе.
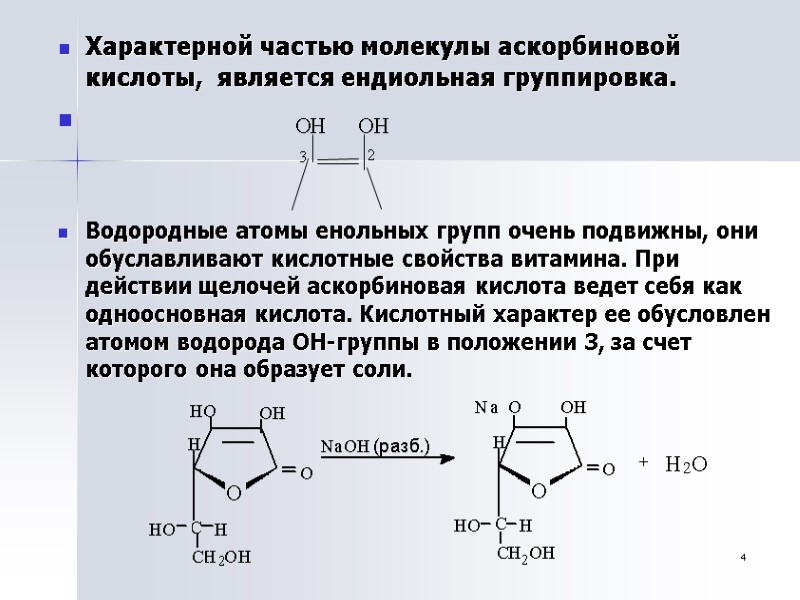
4 Характерной частью молекулы аскорбиновой кислоты, является ендиольная группировка. Водородные атомы енольных групп очень подвижны, они обуславливают кислотные свойства витамина. При действии щелочей аскорбиновая кислота ведет себя как одноосновная кислота. Кислотный характер ее обусловлен атомом водорода ОН-группы в положении 3, за счет которого она образует соли.
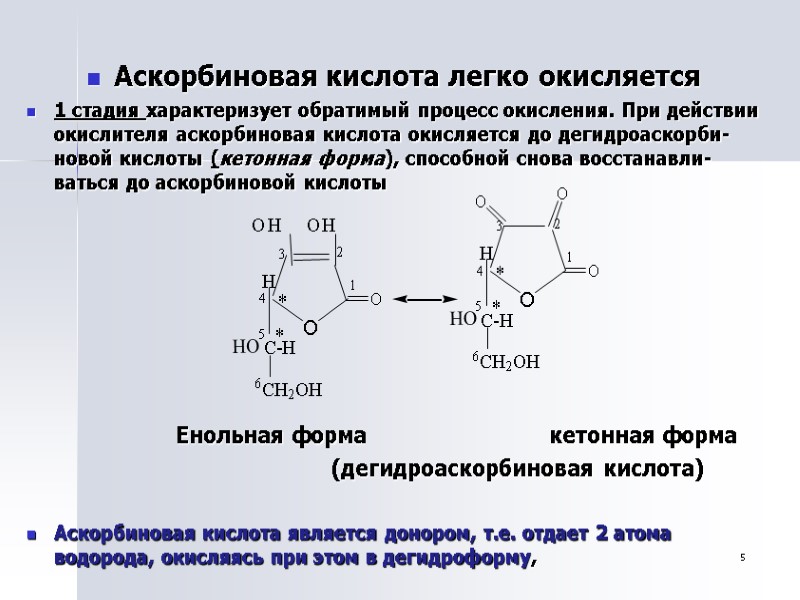
5 Аскорбиновая кислота легко окисляется 1 стадия характеризует обратимый процесс окисления. При действии окислителя аскорбиновая кислота окисляется до дегидроаскорби-новой кислоты (кетонная форма), способной снова восстанавли-ваться до аскорбиновой кислоты Енольная форма кетонная форма (дегидроаскорбиновая кислота) Аскорбиновая кислота является донором, т.е. отдает 2 атома водорода, окисляясь при этом в дегидроформу,

6 2 стадия – В водной среде процесс окисления может идти дальше – до разложения дегидроаскорбиновой кислоты. Это необратимый процесс окисления с потерей физиологической активности и протекает до 2,3-дикетогулоновой к-ты Необходимо предотвращать протекание 2-й стадии. Для этого при изготовлении растворов аскорбиновой кислоты для иньекций добавляют различные стабилизаторы, например гидросульфит натрия и др., а также обеспечивают условия хранения: отсутствие света, соприкосновения с металлами, особенно солями железа.

7 ПОДЛИННОСТЬ. (ВР и ГФХII): 1. По удельному вращению - удельное вращение 10% р-ра аскорбиновой кислоты равно от +20,50 до +21,50. 2. рН =2,1 – 2,6 (5% р-ра) 3. Сравнение ИК-спектра субстанции с ИК-спектром образца. 4. Ультрафиолетовый спектр 0,001% р-ра имеет мах при 243 нм.
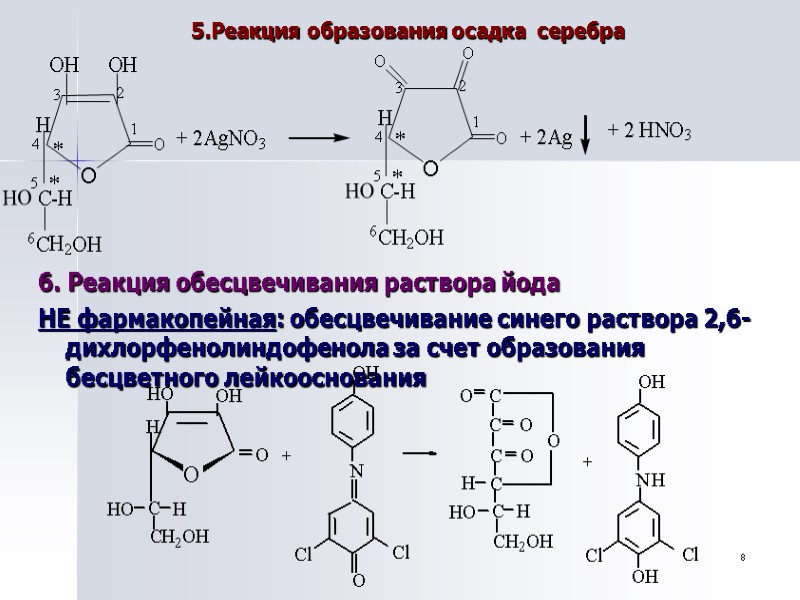
8 5.Реакция образования осадка серебра 6. Реакция обесцвечивания раствора йода НЕ фармакопейная: обесцвечивание синего раствора 2,6-дихлорфенолиндофенола за счет образования бесцветного лейкооснования O O H C H 2 O H O O H O H H C - H 1 2 3 4 5 6 * * O O H C H 2 O H O H C - H 1 2 3 4 5 6 * * O O + 2 A g N O 3 + 2 A g + 2 H N O 3
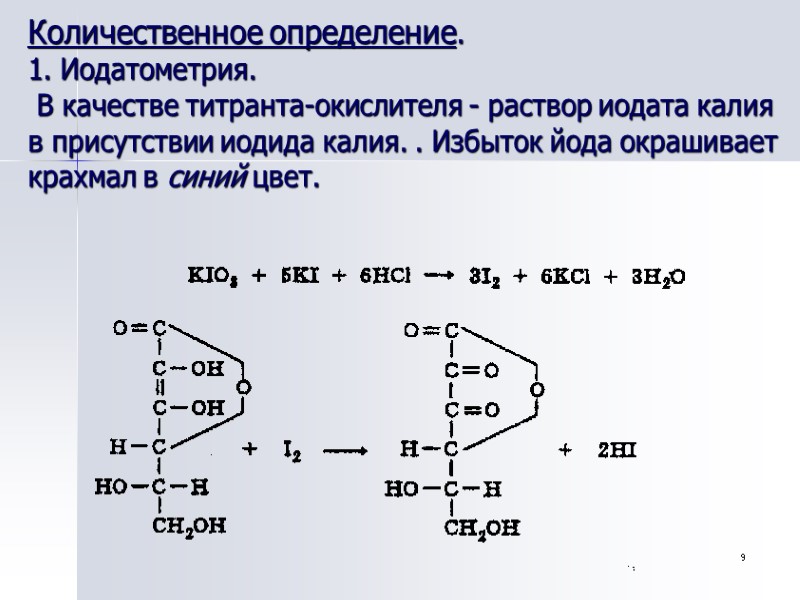
9 Количественное определение. 1. Иодатометрия. В качестве титранта-окислителя - раствор иодата калия в присутствии иодида калия. . Избыток йода окрашивает крахмал в синий цвет.

10 Чистота. Содержание меди определяют по величине абсорбции при 324,8 нм Содержание железа определяют по величине абсорбции при 248,3 нм Щавелевая кислота – не более 0,2%, при сравнении с эталонным раствором (после добавления CaCl2) Сульфатная зола и тяжелые металлы Микробиологическая чистота

11 Применение. Во всех случаях, когда организм нуждается в дополнительном введении этого витамина: для профилактики и лечения цинги, при геморрагических диатезах, носовых, легочных, печеночных, маточных и других кровотечениях, в том числе вызванных лучевой болезнью, а также передозировкой антикоагулянтов, при инфекционных заболеваниях и интоксикациях. при усиленном физическом труде, умственном напряжении. при атеросклерозе: положительно влияет на липидный обмен.

12 Хранение. В хорошо закрытой таре, предохраняя от действия света и кислорода воздуха. Устойчива в кристаллическом виде (в отсутствии влаги), в растворах быстро окисляется. При этом раствор окрашивается в желтый цвет и теряет свою активность. Особенно легко окисление происходит на воздухе, в присутствии следов металлов, в щелочной и кислой среде. Для повышения стабильности к растворам кислоты прибавляют восстановители, например, натрия метагидросульфит и натрия сульфит.

13 Раствор аскорбиновой кислоты 5% для инъекций (Solutio Аcidi ascorbinici 5% pro injectionibus) Состав: аскорбиновой кислоты –50 г натрия гидрокарбоната – 23,85 г (рН=6,0-7,0 – чтобы не раздражать ткани) натрия метабисульфита – 1 г (или натрия сульфита безводного-2г) антиоксидант для сохранения пр-та воды для инъекций, насыщенной углекислым газом – до 1 л. NaHCO3 + H2O = NaOH + CO2 + H2O щелочн. рН

14 Описание. Прозрачная бесцветная или желтоватого цвета жидкость При количественном определении следует учитывать, что сульфит натрия (Na2SO3 или метабисульфита натрия - Na2S2O5), - как восстановитель может реагировать с йодом. При гидролизе в р-ре образуется гидросульфит натрия NaHSO3. Na2SO3 + Н2О NaHSO3 + NaOH Na2S2O5 + Н2О 2NaHSO3 Чтобы предотвратить взаимодействие метабисульфита натрия с йодом, предварительно к раствору аскорбиновой кислоты добавляют раствор формальдегида, который связывает гидросульфит натрия:

15 АМИНОКИСЛОТЫ АЛИФАТИЧЕСКОГО РЯДА И ИХ ПРОИЗВОДНЫЕ Кислота глутаминая, кислота гамма-аминомасляная, цистеин, ацетилцистеин, метионин, пеницилламин, кальций-динатриевая соль этилендиаминтет-рауксусной кислоты, пирацетам, каптоприл, эналаприл, кислота аминокапроновая, мелфалан

16 Аминокислоты производные углеводородов, в молекуле которых содержатся одновременно карбоксильная и аминогруппа. В зависимости от расположения аминогруппы по отношению к карбоксилу различают , , - и другие аминокислоты.

17 По номенклатуре ИЮПАК буквы не употребляются. Аминокислоты называют по названию соответствующей карбоновой кислоты с добавлением приставки амино-. Положение аминогруппы в углеродной цепи указывают цифрой. Аминокислоты подразделяются на природные и синтетические. Аминокислоты являются источником построения жизненно необходимых веществ – белков, пептидов, ферментов, гормонов, участвуют в азотном обмене. В настоящее время известно более 150 аминокислот. В состав белков входит 26 аминокислот. «Заменимые» аминокислоты синтезируются в организме человека в количестве, достаточном для удовлетворения потребности организма. «Незаменимые» аминокислоты либо не синтезируются в организме человека, либо синтезируются в недостаточном количестве и поэтому должны пополняться с пищей.
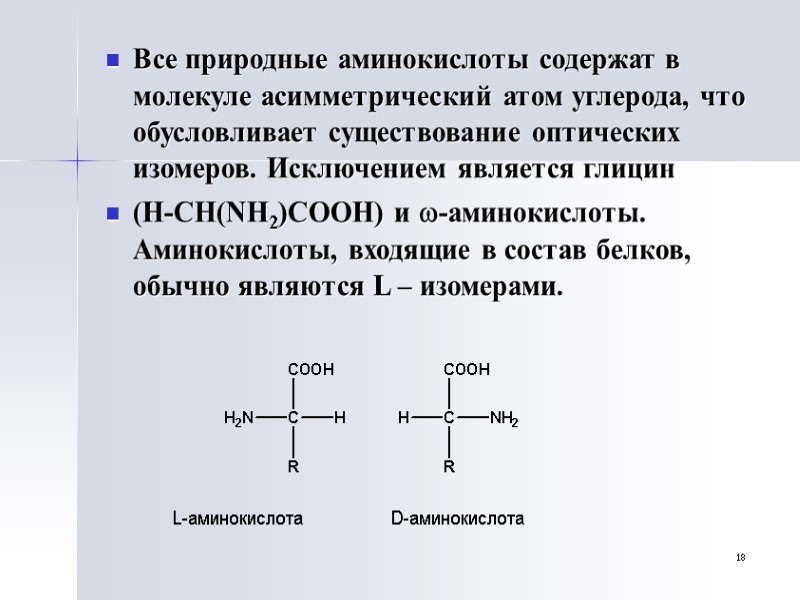
18 Все природные аминокислоты содержат в молекуле асимметрический атом углерода, что обусловливает существование оптических изомеров. Исключением является глицин (Н-СН(NН2)СООН) и -аминокислоты. Аминокислоты, входящие в состав белков, обычно являются L – изомерами. L-аминокислота D-аминокислота
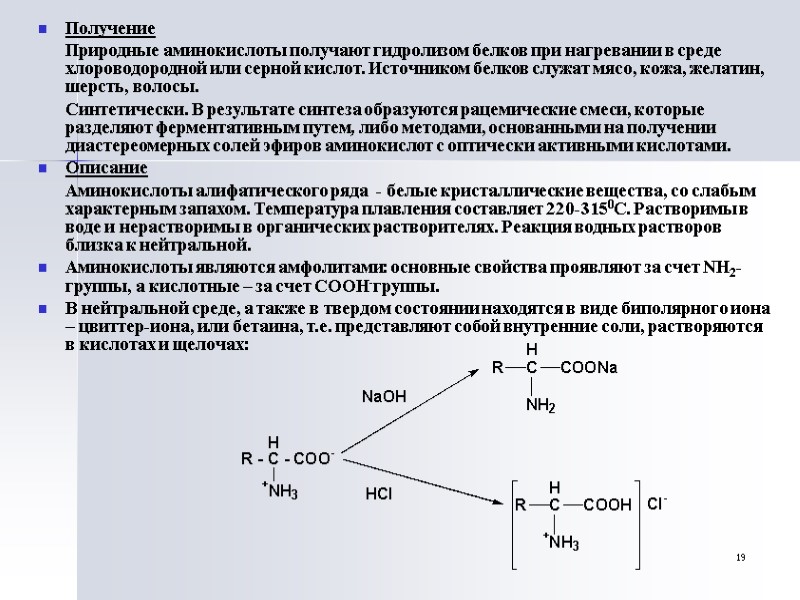
19 Получение Природные аминокислоты получают гидролизом белков при нагревании в среде хлороводородной или серной кислот. Источником белков служат мясо, кожа, желатин, шерсть, волосы. Синтетически. В результате синтеза образуются рацемические смеси, которые разделяют ферментативным путем, либо методами, основанными на получении диастереомерных солей эфиров аминокислот с оптически активными кислотами. Описание Аминокислоты алифатического ряда - белые кристаллические вещества, со слабым характерным запахом. Температура плавления составляет 220-3150С. Растворимы в воде и нерастворимы в органических растворителях. Реакция водных растворов близка к нейтральной. Аминокислоты являются амфолитами: основные свойства проявляют за счет NН2-группы, а кислотные – за счет СООН-группы. В нейтральной среде, а также в твердом состоянии находятся в виде биполярного иона – цвиттер-иона, или бетаина, т.е. представляют собой внутренние соли, растворяются в кислотах и щелочах:
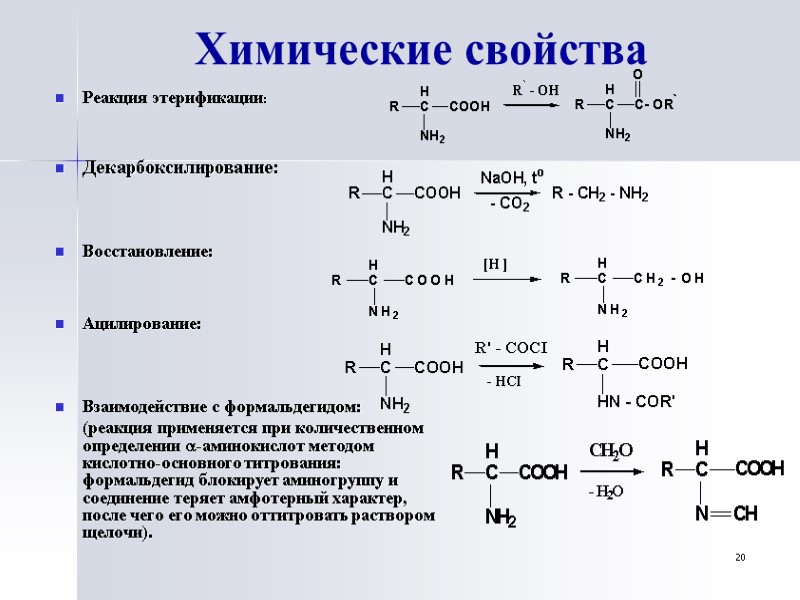
20 Химические свойства Реакция этерификации: Декарбоксилирование: Восстановление: Ацилирование: Взаимодействие с формальдегидом: (реакция применяется при количественном определении -аминокислот методом кислотно-основного титрования: формальдегид блокирует аминогруппу и соединение теряет амфотерный характер, после чего его можно оттитровать раствором щелочи).
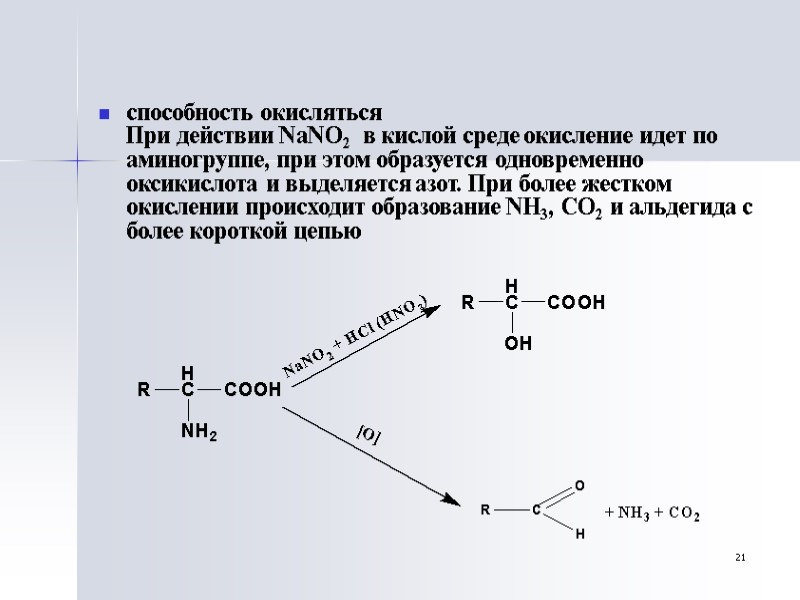
21 способность окисляться При действии NaNO2 в кислой среде окисление идет по аминогруппе, при этом образуется одновременно оксикислота и выделяется азот. При более жестком окислении происходит образование NH3, CO2 и альдегида с более короткой цепью
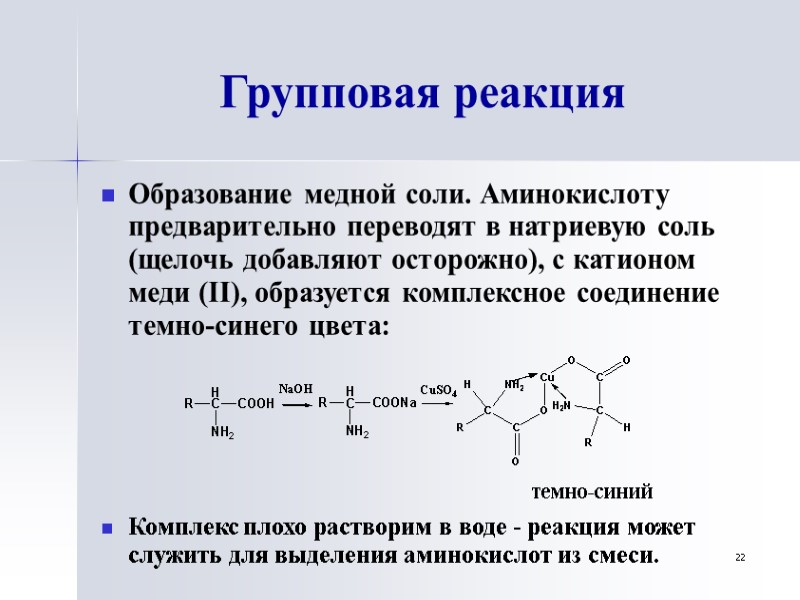
22 Групповая реакция Образование медной соли. Аминокислоту предварительно переводят в натриевую соль (щелочь добавляют осторожно), с катионом меди (II), образуется комплексное соединение темно-синего цвета: темно-синий Комплекс плохо растворим в воде - реакция может служить для выделения аминокислот из смеси.
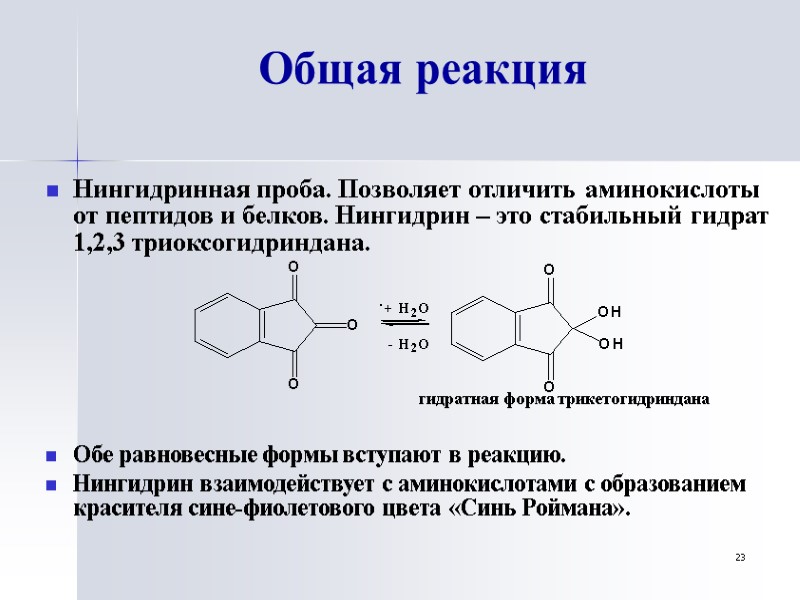
23 Общая реакция Нингидринная проба. Позволяет отличить аминокислоты от пептидов и белков. Нингидрин – это стабильный гидрат 1,2,3 триоксогидриндана. гидратная форма трикетогидриндана Обе равновесные формы вступают в реакцию. Нингидрин взаимодействует с аминокислотами с образованием красителя сине-фиолетового цвета «Синь Роймана».
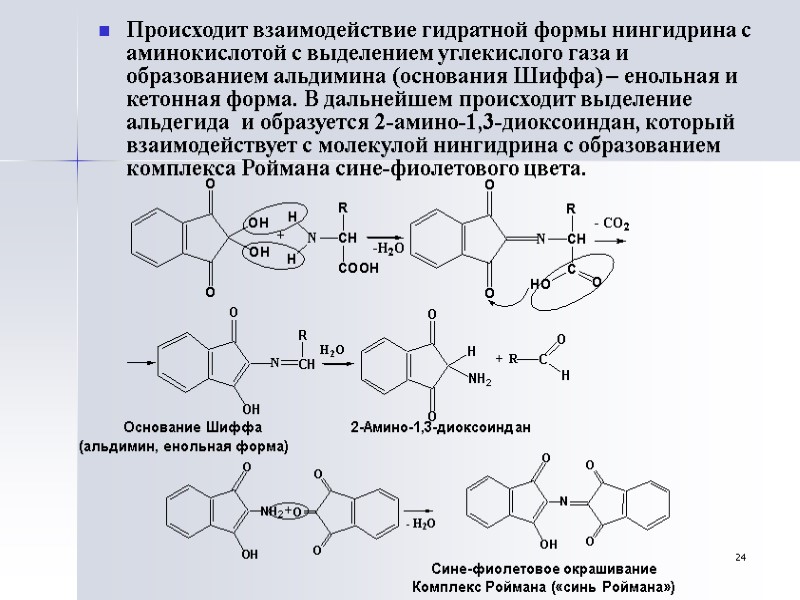
24 Происходит взаимодействие гидратной формы нингидрина с аминокислотой с выделением углекислого газа и образованием альдимина (основания Шиффа) – енольная и кетонная форма. В дальнейшем происходит выделение альдегида и образуется 2-амино-1,3-диоксоиндан, который взаимодействует с молекулой нингидрина с образованием комплекса Роймана сине-фиолетового цвета. Основание Шиффа 2-Амино-1,3-диоксоиндан (альдимин, енольная форма) Сине-фиолетовое окрашивание Комплекс Роймана («синь Роймана»)

25 Аминокислоты, содержащие в молекуле атом серы, испытывают на присутствие тио- или тиометильной группы (с нитропруссидом натрия, хлоридом железа (III) или нитритом натрия). Органически связанную серу окисляют до сульфат-иона или разрушают серосодержащую аминокислоту до образования сероводорода, который обнаруживают по запаху. Количественное определение Йодометрическим методом.

26 КИСЛОТА ГЛУТАМИНОВАЯ ACIDUM GLUTAMINICUM С5Н8NО4 Мr 147,13 2-аминоглутаровая кислота, -аминоглутаровая Глутаминовая кислота входит в состав белков: миозин, казеин, -лактоглобулин. В большом количестве содержится в белках мозга, злаках. Ранее глютаминовую кислоту получали из злаков путем кислотного гидролиза. В настоящее время она синтезируется. Описание Белый кристаллический порошок с едва ощутимым запахом. Мало растворим в холодной воде, растворим в горячей. Практически не растворим в спирте и эфире. Растворяется в кислотах и щелочах. Температура плавления – не ниже 1900С. Удельное вращение - от +300 до +340 (5% раствор в разведенной хлороводородной кислоте) ИК-спектрофотометрия
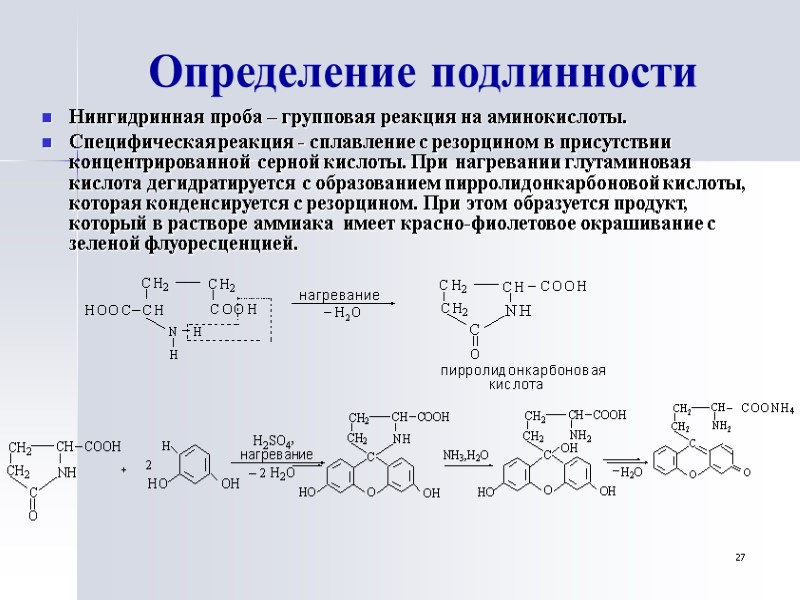
27 Определение подлинности Hингидринная проба – групповая реакция на аминокислоты. Специфическая реакция - сплавление с резорцином в присутствии концентрированной серной кислоты. При нагревании глутаминовая кислота дегидратируется с образованием пирролидонкарбоновой кислоты, которая конденсируется с резорцином. При этом образуется продукт, который в растворе аммиака имеет красно-фиолетовое окрашивание с зеленой флуоресценцией.
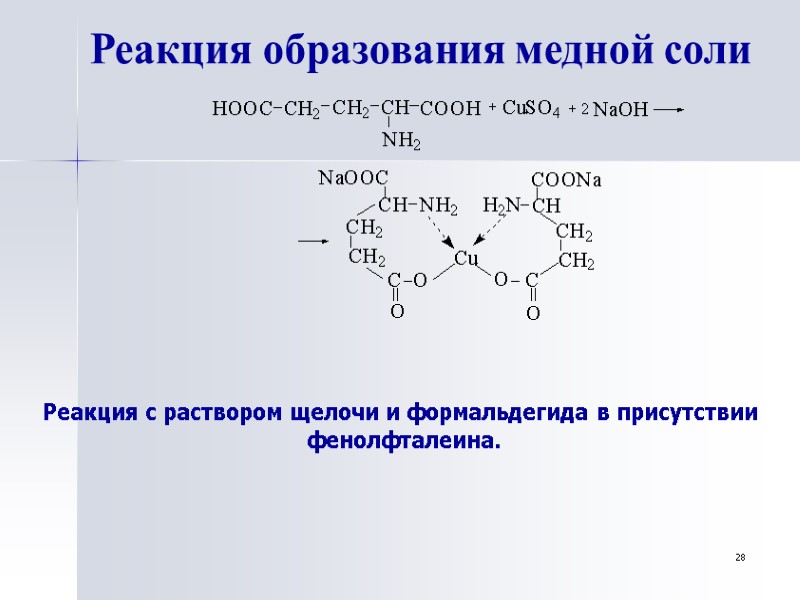
28 Реакция образования медной соли Реакция с раствором щелочи и формальдегида в присутствии фенолфталеина.

29 Оценка чистоты Недопустимые примеси: Посторонние аминокислоты. 1,5 г препарата растворяют в 30 мл горячей свежепрокипяченной воды и по охлаждении фильтруют; к 5 мл того же фильтрата прибавляют 5 мл реактива Фелинга и кипятят на сетке 2 минуты; не должно появляться зеленое или бурое окрашивание. Родственные примеси, дающие реакцию с нингидрином (методом ТСХ, ЕР) органические примеси (с концентрированной серной кислотой). Определяют кислотность: рН фильтрата должен быть 3,1 – 3,7. Допустимые примеси: хлориды, сульфаты, ионы аммония, железо, тяжелые металлы и мышьяк. Потеря в массе при высушивании, сульфатная зола.
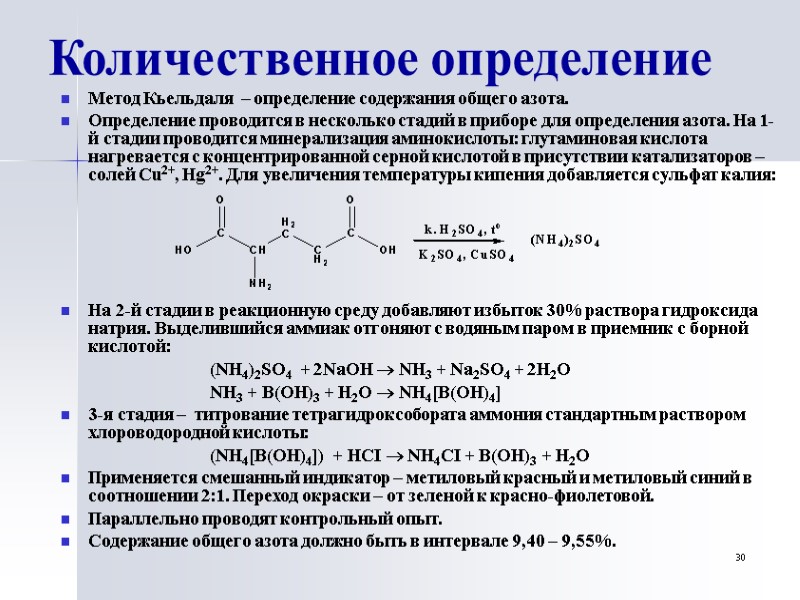
30 Количественное определение Метод Кьельдаля – определение содержания общего азота. Определение проводится в несколько стадий в приборе для определения азота. На 1-й стадии проводится минерализация аминокислоты: глутаминовая кислота нагревается с концентрированной серной кислотой в присутствии катализаторов – солей Сu2+, Hg2+. Для увеличения температуры кипения добавляется сульфат калия: На 2-й стадии в реакционную среду добавляют избыток 30% раствора гидроксида натрия. Выделившийся аммиак отгоняют с водяным паром в приемник с борной кислотой: (NH4)2SO4 + 2NaOH NH3 + Na2SO4 + 2H2O NH3 + B(OH)3 + H2O NH4[B(OH)4] 3-я стадия – титрование тетрагидроксобората аммония стандартным раствором хлороводородной кислоты: (NH4[B(OH)4]) + HCI NH4CI + B(OH)3 + H2O Применяется смешанный индикатор – метиловый красный и метиловый синий в соотношении 2:1. Переход окраски – от зеленой к красно-фиолетовой. Параллельно проводят контрольный опыт. Содержание общего азота должно быть в интервале 9,40 – 9,55%.

31 Метод нейтрализации Глутаминовую кислоту титруют раствором гидроксида натрия. Титрование идет по одной карбоксильной группе: Индикатор - бромтимоловый синий. Переход окраски от желтой до голубой. Метод формольного титрования по Серенсу (нефармакопейный). Титрование проходит по двум карбоксильным группам. Метод основан на том, что формальдегид блокирует аминогруппу, соединение теряет амфотерность. Образуется N-метиленовое производное, которое обладает сильнокислым характером и может быть оттитровано раствором щелочи по фенолфталеину.

32 Применение При различных психических расстройствах. Выпускается в таблетках, покрытых оболочкой, по 0,25 г, в ампулах в виде 1% раствора. Хранение В хорошо закрытой таре в защищенном от света месте.

33 МЕТИОНИН Methioninum (H3C – S – CH2 – CH2CH(NH2)-COOH) C8H12NO2S (2- амино-4 метилтиобутановая кислота) Мr 149,21 Впервые был открыт в белках в 1928 г. Содержится в белках крови, протоплазмы, в альбумине яйца, миозине, казеине. Получают метионин гидролизом этих белков с последующим высаливанием из гидролизата с помощью хлорида натрия. Затем его отделяют от других аминокислот хроматографическим методом. В настоящее время метионин получают и синтетически из ацетилмалонового эфира, который конденсируется с -метилтиоэтанолом:

34 Метионин является незаменимой аминокислотой, то есть не синтезируется в организме человека. Содержится в следующих продуктах питания:

35 Описание Белый кристаллический порошок или белые кристаллы, растворим в воде, трудно растворим в спирте, практически нерастворим в эфире.

36 Определение подлинности Нингидринная проба. Реакция с нитропруссидом натрия. Для определения в метионине метилсульфидной группы препарат сплавляют с 30% раствором щелочи, пробирку закрывают фильтровальной бумагой, смоченной 5% раствором нитропруссида натрия. К охлажденному сплаву добавляют разведенную серную кислоту, появляется запах H2S и меркаптана: Na2S + H3CSNa + 2H2SO4 H2S +CH3SH + + Na2SO4 + NaHSO4 После добавления серной кислоты на бумаге появляется красно-фиолетовое окрашивание: нитропруссид натрия в аммиачной среде с сероводородом образует комплексный анион красно-фиолетового цвета: S2- + [Fe(CN)5NO]2- [Fe(CN)5NOS]4- По ВР: - определение уд. вращения (+22,5 - +240); - по ИК-спектрам; - по хроматограммам, используя нингидринную реакцию; - по реакции с нитропруссидом натрия.

37 Оценка чистоты Не допустимые примеси: цианиды, мышьяк. Определение цианидов: к препарату добавляют воду, раствор железа сульфата (II), железа хлорида (III), раствор гидроксида натрия и нагревают. После подкисления хлороводородной кислотой смесь не должна окрашиваться в синий цвет. 6NaCN + FeSO4 Na4[Fe(CN)6] + Na2SO4 FeCl3 + Na4[Fe(CN)6] NaFe[Fe(CN)6] + 3NaCl Допустимые примеси: хлориды, сульфаты, тяжелые металлы,ионы аммония, родственные примеси (методом ТСХ). Потеря в весе при высушивании не должна превышать 0,5%. рН = 5,5-6,5

38 Количественное определение Метод Кьельдаля Йодометрический метод. Окисление серы йодом в среде фосфатного буфера (K2НPO4 + KH2PO4) Препарат растворяют в воде, добавляют фосфатный буфер и йодид калия до полного растворения. Затем точно добавляют раствор йода и оставляют на 30 минут. Метионин окисляется до соответствующего сульфоксида. I2 + 2Na2S2O3 2NaI + Na2S4O6 Избыток йода оттитровывают раствором тиосульфата натрия, прибавляя в конце титрования раствор крахмала. Параллельно проводят контрольный опыт. По ВР: метод неводного титрования (растворитель – муравьиная кислота с добавлением ледяной уксусной кислоты; титрант – 0,1М хлорной кислоты. Окончание – потенциометрически.

39 Применение Для лечения и предупреждения заболеваний и токсических поражений печени, а также при хроническом алкоголизме, сахарном диабете, для лечения дистрофии, возникающей в результате белковой недостаточности. Выпускается в порошке и таблетках по 0,25 г. Хранение В стеклянных банках оранжевого стекла в защищенном от света месте.

40 ЦИСТЕИН Cysteinum (цистеина гидрохлорид) 2-амино-3-меркаптопропановая кислота Описание Белый кристаллический порошок со слабым специфическим запахом. Хорошо растворим в воде, разведенных минеральных кислотах, плохо растворим в спирте, практически нерастворим в эфире. Цистеин является: заменимой аминокислотой; может синтезироваться в организме с использованием метионина. Недостаток этой аминокислоты может привести к нарушению обменных процессов в организме. ∙HCl∙ H2O

41 Определение подлинности Реакция с нингидрином. Реакция образования сульфида свинца. При нагревании со щелочью цистеин выделяет сульфид натрия, имеющий резкий запах и вызывающий почернение бумаги, смоченной ацетатом свинца: Реакция с FeCl3. Появляется быстро исчезающее сине-фиолетовое окрашивание. По ВР: - определение удельного вращения (8%) (+5,5 - +7,00); - по ИК-спектрам; - по хроматограммам, используя нингидринную реакцию; - по реакции с нитропруссидом натрия (окрашивание фиолетовое, красно-коричневое, оранжевое) Определение хлорид-ионов. . …

42 Оценка чистоты: Допустимые примеси: сульфаты, железо, тяжелые металлы и аммиак. Недопустимые примеси: другие аминокислоты (ТСХ). Количественное определение: Обратный йодометрический метод. Цистеин титруют 0,1М раствором йода в кислой среде в прис. KI. При этом происходит окисление сульфгидрильных групп. Избыток йода оттитровывают стандартным раствором тиосульфата натрия. I2 + 2Na2S2O3 2NaI + Na2S4O6

43 Применение Регулирует процессы обмена веществ хрусталика глаза. Применяется для задержки развития катаракты. Форма выпуска: порошок в плотно укупоренных банках по 10 г. Готовые растворы и хранят не более 4 ч. Хранение В сухом прохладном, защищенном от света месте. Растворы готовят непосредственно перед применением, так как водные растворы не стойкие, окисляются кислородом воздуха с выделением осадка. Растворы готовят в асептических условиях, их нельзя стерилизовать путем нагревания, так как цистеин разлагается.
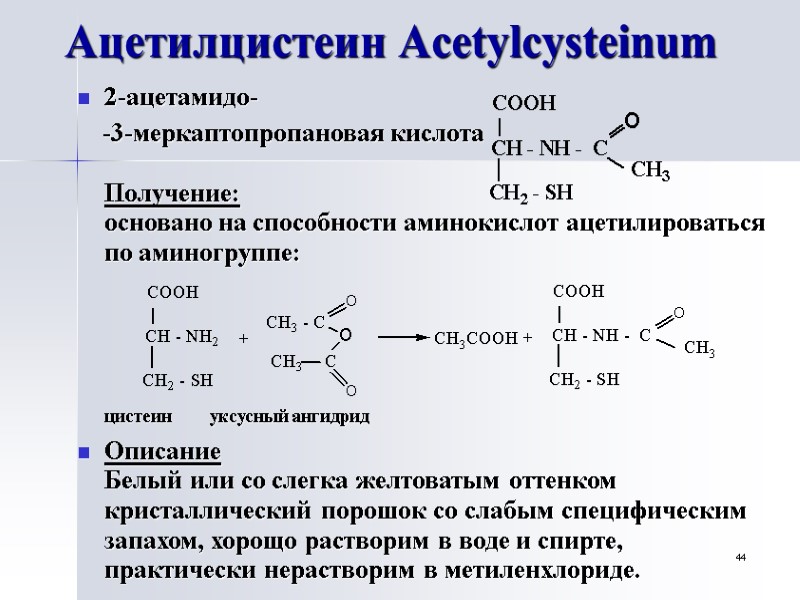
44 Ацетилцистеин Acetylcysteinum 2-ацетамидо- -3-меркаптопропановая кислота Получение: основано на способности аминокислот ацетилироваться по аминогруппе: цистеин уксусный ангидрид Описание Белый или со слегка желтоватым оттенком кристаллический порошок со слабым специфическим запахом, хорощо растворим в воде и спирте, практически нерастворим в метиленхлориде.

45 Определение подлинности Ацетилцистеин, в отличие от других аминокислот, не взаимодействует с нингидрином По физическим константам: - tпл. – 104-1100С. - Удельное вращение (5%): +21 - +260 (в растворе гидроксида натрия). - ИК-спектрометрия. Реакция сплавления с тиоцианатом калия протекает с образованием сероводорода, который обнаруживают с помощью фильтровальной бумаги, смоченной раствором ацетата свинца. H2S + Pb(CH3COO)2 PbS + CH3COOH черный
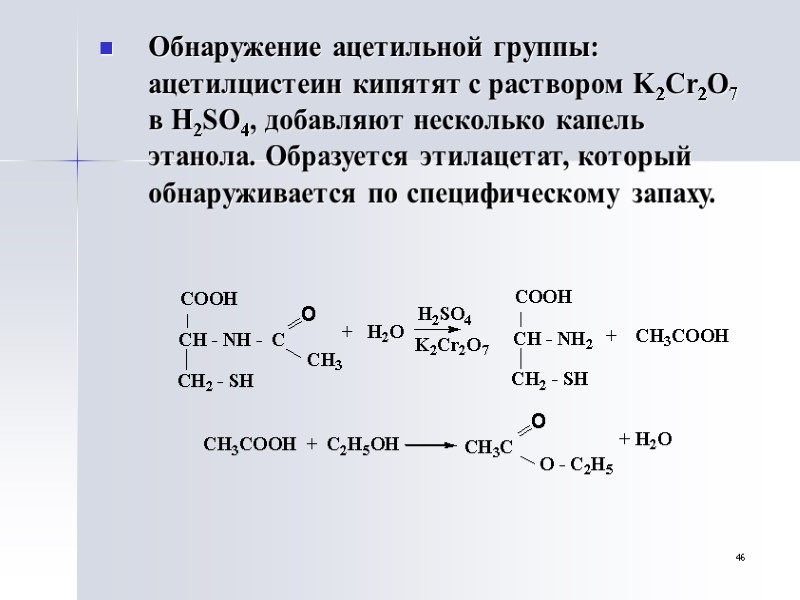
46 Обнаружение ацетильной группы: ацетилцистеин кипятят с раствором K2Cr2O7 в H2SO4, добавляют несколько капель этанола. Образуется этилацетат, который обнаруживается по специфическому запаху.

47 Оценка чистоты Допустимые примеси: тяжелые металлы, цинк, родственные примеси определяются методом ВЭЖХ. Потеря при высушивании должна составлять не более 1%. Количественное определение Йодометрический метод. Проводится аналогично цистеину. Применение Ацетилцистеин оказывает муколитическое действие, отхаркивающее, антибиотическое. Применяют при бронхитах, пневмонии, бронхиальной астме, отитах, ринитах. Используют в виде 20% раствора для ингаляций . Детоксицирующее средство. Применяется также при отравлении парацетамолом. Как антиоксидант, он защищает печень от воздействия некоторых токсических веществ. Хранение Список Б. Хранят в хорошо закрытой таре, предохраняющей от действия света, в сухом прохладном месте.

48 Пеницилламин Penicillaminum 2-амино-3-меркапто-3-метил-бутановая кислота Пенищилламин представляет собой часть молекулы пенициллина. Обладает в растворах оптической активностью. Получение Из бензилпенициллина путем его разрушения до пеницилламина. Описание Белый порошок со специфическим запахом. Легко растворим в воде, мало растворим в 95% спирте, практически не растворим в эфире и хлороформе. Подлинность Определение удельного вращения – -60,5о – -64,5о. рН=4,5 – 5,5 Реакция с нингидрином (по аминогруппе - сине-фиолетовое окрашивание). Реакция с фосфорно-вольфрамовой кислотой (H3PO4 .12WO3) на меркаптогруппу (SН). Образуется соединение голубого цвета.

49 Оценка чистоты Суммарное содержание примесей пенициллиновой природы определяется методом тонкослойной хроматографии и не должно превышать 1%. Дисульфид пеницилламина – определяют методом ТСХ, содержание нормируется - не более 1%. Недопустимая примесь - бензилпенициллин. Потеря при высушивании при t=600С должна составлять не более 0,5%.

50 Количественное определение По ВР – метод неводного титрования. Препарат растворяют в безводной уксусной кислоте. Титрант – хлорная кислота. Точку эквивалентности определяют потенциоме-трически.

51 Применение Пеницилламин отличается высокой комплексообразущей активностью в отношении ионов железа, ртути, свинца, меди и кальция. Поэтому его применяют при острых и хронических отравлениях тяжелыми металлами, при болезни Вильсона. Пеницилламин способствует связыванию и выведению меди из организма. Препарат назначают внутрь в капсулах и таблетках по 0,15 и 0,25 г. Хранение В сухом, защищенном от света месте, при комнатной температуре.

52 Аминалон Aminalonum -аминомасляная кислота (4-аминобутановая кислота) Н2N–СН2-СН2-СН2–СООН Получение Путем гидролиза белков. В настоящее время препарат получают синтетически. Описание Белый кристаллический порошок со слабым специфичесим запахом. Легко растворим в воде, очень мало растворим в спирте. рН = 6,5-7,5.
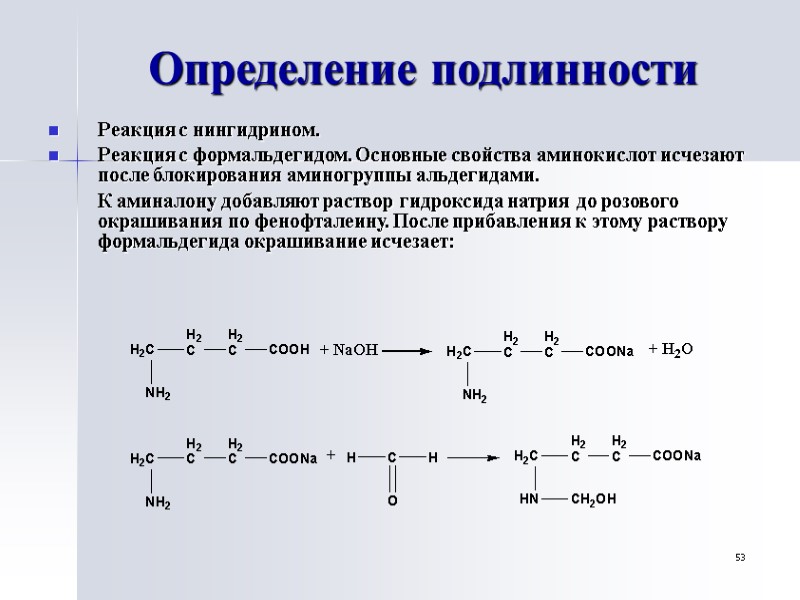
53 Определение подлинности Реакция с нингидрином. Реакция с формальдегидом. Основные свойства аминокислот исчезают после блокирования аминогруппы альдегидами. К аминалону добавляют раствор гидроксида натрия до розового окрашивания по фенофталеину. После прибавления к этому раствору формальдегида окрашивание исчезает:

54 Количественное определение Метод кислотно-основного титрования в неводных средах: Растворитель - ледяная уксусная кислота (аминокислоты титруют как основания). В среде безводного растворителя аминалон становится сопряженной кислотой. Титрант – 0,1М раствор хлорной кислоты. Индикатор – кристаллический фиолетовый. Изменение окраски – от зеленой к синей.

55 Метод нейтрализации в водной среде. Н2N–СН2-СН2-СН2–СООН + NaOH Н2N–СН2-СН2-СН2–СООNa + H2O Во избежании мешающего влияния аминогруппы (образование цвиттер-иона) добавляют раствор формальдегида; при этом образуется N-метилено-вое производное. Индикатор – бромтимоловый синий. При рН 6,0 – 7,6 – переход окраски от желтой к синей. Применение Ноотропное средство при сосудистых заболеваниях головного мозга. Выпускается в таблетках по 0,25 г, покрытых оболочкой. Хранение В сухом защищенном от света месте.

56 Пирацетам Pyracetamum Ноотропил 2-(2-оксо-1-пирролидинил)ацетамид Применяют также раствор пирацетама Solutio Pyracetami 20% pro injectionibus Состав: пирацетама - 200 г натрия ацетата – 1 г уксусной кислоты разб. до рН=5,8 воды для инъекций – до 1 л По структуре пирацетам является лактамом и амидом. Описание Белый кристаллический порошок. Легко растворим в воде, спирте, не растворим в эфире. Раствор пирацетама – бесцветная, прозрачная жидкость. Тпл.=151-1550С; рН раствора = 5,0-6,0.
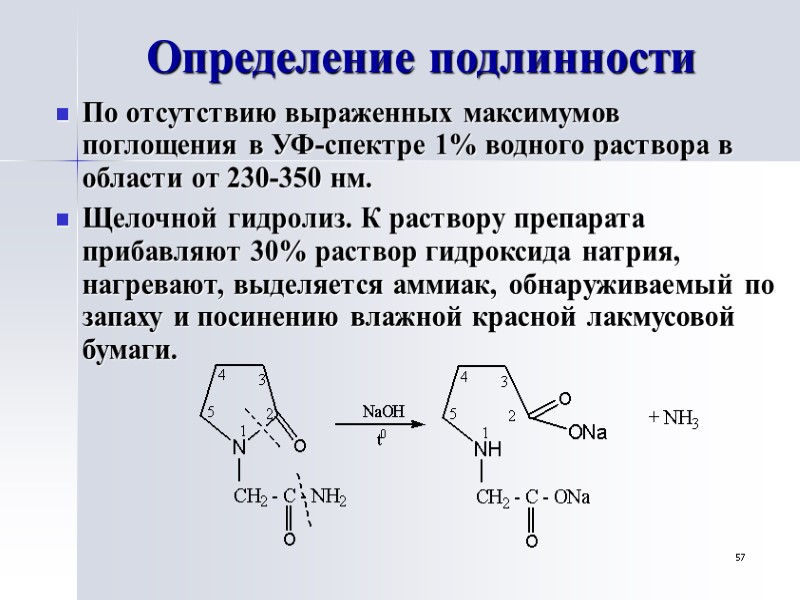
57 Определение подлинности По отсутствию выраженных максимумов поглощения в УФ-спектре 1% водного раствора в области от 230-350 нм. Щелочной гидролиз. К раствору препарата прибавляют 30% раствор гидроксида натрия, нагревают, выделяется аммиак, обнаруживаемый по запаху и посинению влажной красной лакмусовой бумаги.

58 Оценка чистоты Посторонние примеси определяются методом ТСХ (не более 0,5%). Количественное определение Метод Кьельдаля. Неводное титрование. ВЭЖХ. Применение При заболеваниях ЦНС с сосудистыми расстройствами. Улучшает кровоснабжение головного мозга, оказывает положительное влияние на память. Выпускаются в таблетках, покрытых оболочкой по 0,2 г, в капсулах по 0,4 г, 20% раствор для инъекций в ампулах по 5 мл. Хранение В сухом защищенном от света месте.

59 Тетацин кальция раствор для инъекций 10% Solucio Tetacini – Calcii pro injectionibus 10% (кальций динатриевая соль этилендиамина тетрауксусной кислоты) Состав: динатриевая соль ЭДТА – 100 г СаСО3 – 34 г HCI – 8 мл Н2О для инъекций – до 1 л Получение. В воде для инъекций растворяют 100 г высушенной динатриевой соли ЭДТА, 34 г СаСО3, 8 мл разведенной хлороводородной кислоты. Общий объем доводят водой для инъекций до 1 л. Раствор разливают в ампулы и стерилизуют. Обязательной контролируют рН (5,0-7,0). Описание. Бесцветная прозрачная жидкость.

60 Определение подлинности Подлинность препарата определяется реакциями на ионы кальция и натрия. На свободный ион кальция: Препарат подщелачивают раствором аммиака по лакмусовой бумажке. Добавляют раствор оксалата аммония. Образуется белый слабый осадок: Са2+ + (NH4)2C2O4 СаС2О4 На связанный кальций: Чтобы доказать наличие кальция, связанного с ЭДТА, его необходимо вытеснить из комплекса металлом, образующим более прочный комплекс. С этой целью используется Pb(NО3)2. [ЭДТА-Са] Nа2 + Pb(NО3)2 [ЭДТА-Pb]Nа2 + Са(NО3)2 Затем необходимо проверить отсутствие ионов свинца в растворе, которые будут мешать открытию ионов кальция – не должно быть желтого осадка иодида свинца: Рb2+ + 2I- РbI2 Далее открывают ион кальция реакцией с оксалатом аммония: (NH4)2C2O4 + Са(NО3)2 СаС2О4 + 2NН4NО3 белый На Nа+ - окрашивание пламени в желтый цвет. рН = 5,0-7,0

61 Оценка чистоты 1. Определяют содержание свободного кальция - не более 0,05%. Для его определения препарат титруют ЭДТА до не -изменяющейся фиолетовой окраски. Индикатор – мурексид. 2. Испытание на пирогенность. По ВР – дополнительно: хлориды, тяжелые металлы, железо. Содержание воды – от 5 до 13%. Количественное определение Проводят по содержанию кальция путем титрования стандартным раствором нитрата свинца в присутствии гексаметилентетрамина (СН2)6N4 : [ЭДТА-Са] Nа2 + Pb(NО3)2 [ЭДТА- Pb]Nа2 + Са(NО3)2 Индикатор – ксиленоловый оранжевый. Применение Детоксицирующее средство при отравлении тяжелыми металлами Хранение В защищенном от света месте.

62 Кислота аминокапроновая Acidum aminocapronicum НООС-СН2-СН2-СН2-СН2-СН2-NН2 С6Н13NО2 6-аминогексановая кислота Описание Белый кристаллический порошок без запаха, растворим в воде, спирте, кислотах, нерастворим в метаноле и хлороформе. Тпл. – 200-204оС. Определение подлинности - Реакция с нингидрином. - Реакция сплавления с тиоцианатом калия. - Реакция с 5% раствором хлорамина в присутствии 1% раствора фенола (специфическая реакция). Появляется синее окрашивание, которое не образуют другие аминокислоты. По ВР – ИК-спектрофотометрия; - по хроматограммам, используя нингидринную реакцию; - с диметилформамидом и аскорбиновой кислотой – оранжевое окрашивание, которое при рН 9,3-10,5 приобретает голубую окраску.

63 Определение чистоты Допустимые примеси – тяжелые металлы, сульфаты. Количественное определение 1. Метод неводного титрования – титрант - раствор НСlО4 в среде ледяной уксусной кислоты. Индикатор – кристаллический фиолетовый. Переход окраски – от зеленой к синей. 2. Определение в смешанных растворителях – титрант 0,1М раствор NaOH в водно-ацетоновой среде (5:25). Индикатор – тимолфталеин. Применение Кровоостанавливающее средство. При остром кровотечении вводят в/в 4-5 г, растворенных в 250 мл 0,9% раствора хлорида натрия в течение 1 часа.
![64 Мелфалан Melphalanum Производное фенилаланина C13H18Cl2N2O2 Mr 305,2 4-[Бис(2-хлорэтил)-амино]-L-фенилаланин 64 Мелфалан Melphalanum Производное фенилаланина C13H18Cl2N2O2 Mr 305,2 4-[Бис(2-хлорэтил)-амино]-L-фенилаланин](https://present5.com/presentacii-2/20171213\39786-lektsia_aminokisloty_dav-1.ppt\39786-lektsia_aminokisloty_dav-1_64.jpg)
64 Мелфалан Melphalanum Производное фенилаланина C13H18Cl2N2O2 Mr 305,2 4-[Бис(2-хлорэтил)-амино]-L-фенилаланин Фармакологический эффект мелфалана обусловлен наличием в молекуле бис-(-хлорэтил)-амина. Синтезируют из L-фенилаланина. Описание Белый или c желтоватым оттенком порошок со слабым запахом. Практически не растворим в воде, хлороформе и эфире. Медленно растворим в метаноле. Растворим в минеральных разведенных кислотах.

65 Определение подлинности ИК-спектроскопия УФ-спектрофотометрия. Имеется максимум поглощения при 260 нм (растворитель - метанол). Проба Бельштейна - на органически связанный хлор. Крупинку мелфалана нагревают на медной проволоке в пламени горелки. Пламя приобретает зеленую окраску. В молекуле мелфалана атом хлора непрочно связан с атомом углерода. Для его обнаружения достаточно нагреть препарат в водно-спиртовой среде с раствором нитрата серебра.

66 Оценка чистоты Допустимые примеси – хлориды. Сухой остаток – не более чем 0,7%. Сульфатная зола – не более чем 0,3%. Количественное определение Аргентометрический метод. Мелфалан количественно определяют по хлорид-иону, который образуется после деструкции молекулы в результате воздействия на навеску 0,5моль/л раствора гидроксида натрия. Затем уксусной кислотой нейтрализуют по фенолфталеину и титруют 0,1М раствором нитрата серебра. Окончание – потенциометрическое. Применение Противоопухолевое, цитостатическое действие. Форма выпуска – таблетки, раствор для инъекций. Хранение В хорошо закрытых контейнерах, защищая от света и поддерживая температуру 25оС.
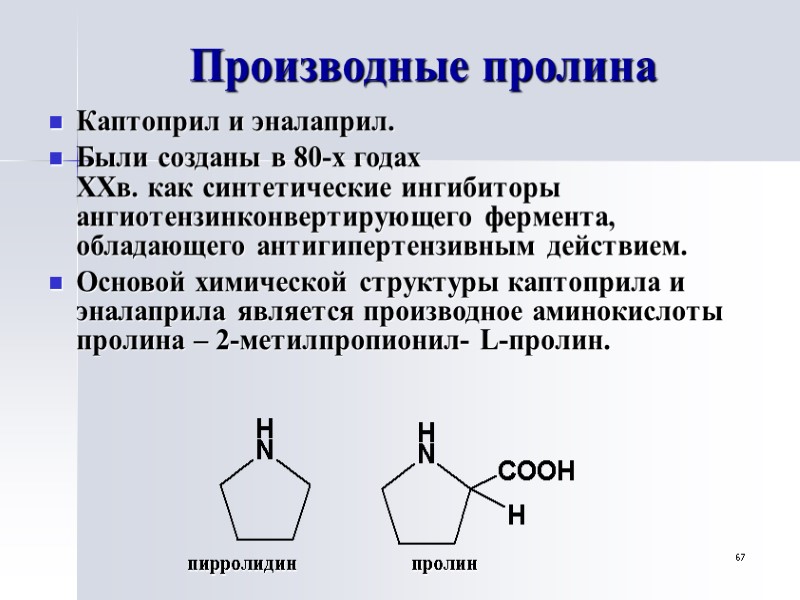
67 Производные пролина Каптоприл и эналаприл. Были созданы в 80-х годах XXв. как синтетические ингибиторы ангиотензинконвертирующего фермента, обладающего антигипертензивным действием. Основой химической структуры каптоприла и эналаприла является производное аминокислоты пролина – 2-метилпропионил- L-пролин. пирролидин пролин
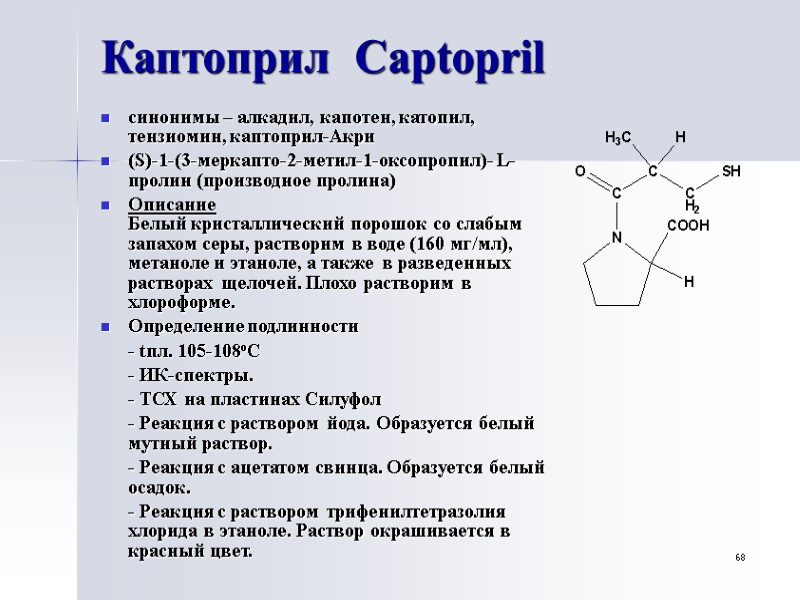
68 Каптоприл Captopril синонимы – алкадил, капотен, катопил, тензиомин, каптоприл-Акри (S)-1-(3-меркапто-2-метил-1-оксопропил)- L-пролин (производное пролина) Описание Белый кристаллический порошок со слабым запахом серы, растворим в воде (160 мг/мл), метаноле и этаноле, а также в разведенных растворах щелочей. Плохо растворим в хлороформе. Определение подлинности - tпл. 105-108оС - ИК-спектры. - ТСХ на пластинах Силуфол - Реакция с раствором йода. Образуется белый мутный раствор. - Реакция с ацетатом свинца. Образуется белый осадок. - Реакция с раствором трифенилтетразолия хлорида в этаноле. Раствор окрашивается в красный цвет.

69 Определение чистоты - рН раствора 2,0-2,6. - Удельное вращение - -156о - -161о. - Допустимые примеси: тяжелые металлы, каптоприла дисульфид (методом ВЭЖХ). Количественное определение Йодометрический метод. Титрант – раствор йода 0,05моль/л. Окончание – потенциометрическое. Хранение В плотно закрытых контейнерах. Применение При гипертонической болезни, гипертоническом кризе.

70 ЭНАЛАПРИЛ Enalapril Синонимы: энам, энап С24Н32N2О9 Мr 492,5 ( (S)-1[N-[1-(этоксикарбонил)-3-фенилпропил] – L-аланил ]-L-пролин малеат) Является «пролекарством» - в организме гидролизуется до каптоприла, который ингибирует ангиотензинконвер-тирующий фермент. Описание Белый кристаллический порошок, плохо растворим в воде, растворим в метиловом и этиловом спиртах, в разбавленных растворах щелочей.

71 Определение подлинности - Тпл.= 143 – 145оС. - ИК-спектры. - Реакция с резорцином. Растворить 30 мг препарата в 3 мл воды. Прибавить бромной воды и нагреть на водяной бане до полного обесцвечивания раствора и охладить. К 0,2 мл этого раствора прибавить 3 мл 0,3% раствора резорцина в серной кислоте и нагревать на водяной бане в течение 15 минут. Появляется красно-коричневое окрашивание. - Гидроксамовая реакция. Реакцию проводят с раствором гидроксиламина гидрохлорида в метаноле в присутствии гидроксида калия в этаноле. Гидроксаматы железа – красно-коричневого цвета. Оценка чистоты - рН раствора – 2,4 – 2,9. - Удельное вращение - -48о - -51о. - Допустимые примеси: тяжелые металлы. Количественное определение Метод нейтрализации. Титрант - 0,1моль/л раствор гидроксида натрия, конец титрования определяют потенциометрически. Применение При гипертонической болезни, сердечной недостаточности. Форма выпуска - таблетки Хранение В хорошо закрытых банках, в защищенном от света месте.
39786-lektsia_aminokisloty_dav-1.ppt
- Количество слайдов: 71

