1 «Электродные потенциалы. Гальванические элементы. ЭДС.






































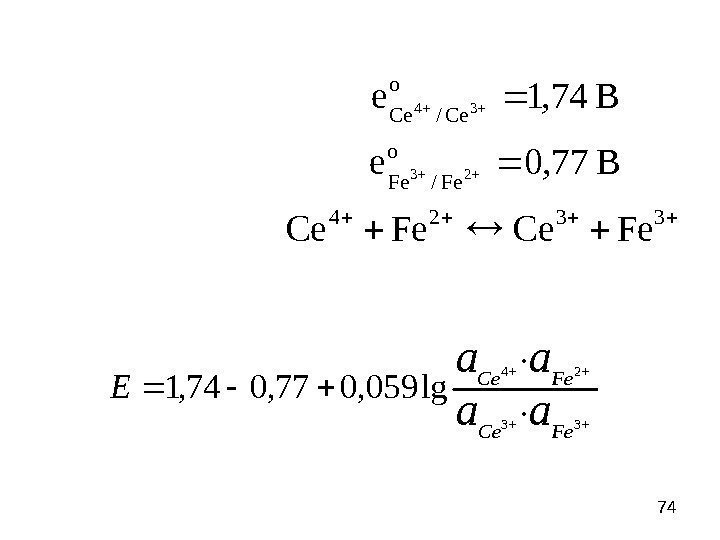











lect07.ppt
- Размер: 9.4 Мб
- Автор: Светлана Чуйнышена
- Количество слайдов: 88
Описание презентации 1 «Электродные потенциалы. Гальванические элементы. ЭДС. по слайдам
 1 «Электродные потенциалы. Гальванические элементы. ЭДС. » Кафедра общей и медицинской химии
1 «Электродные потенциалы. Гальванические элементы. ЭДС. » Кафедра общей и медицинской химии
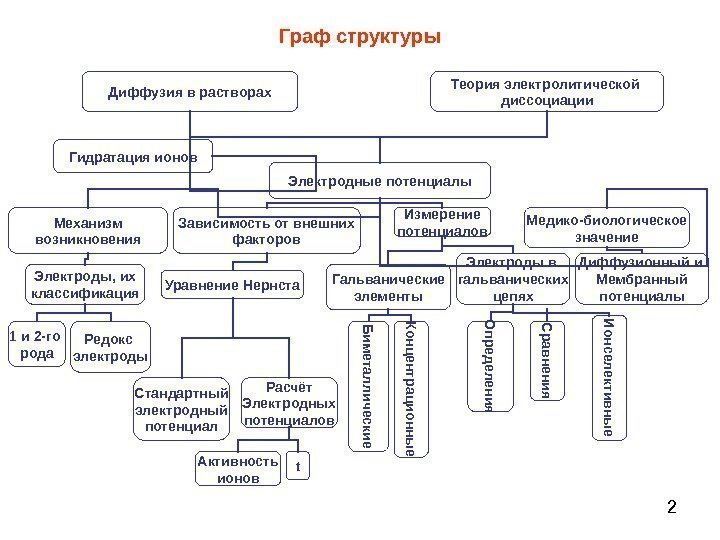
 2 Граф структуры Диффузия в растворах Теория электролитической диссоциации Электродные потенциалы Зависимость от внешних факторов. Механизм возникновения Измерение потенциалов Медико-биологическое значение Уравнение Нернста Гальванические элементы Диффузионный и Мембранный потенциалы Стандартный электродный потенциал. Редокс электроды. Электроды, их классификация Расчёт Электродных потенциалов Электроды в гальванических цепях. Концентрационны е Б им еталлические С равнения О пределения. Гидратация ионов 1 и 2 -го рода t. Активность ионов И онселективны е
2 Граф структуры Диффузия в растворах Теория электролитической диссоциации Электродные потенциалы Зависимость от внешних факторов. Механизм возникновения Измерение потенциалов Медико-биологическое значение Уравнение Нернста Гальванические элементы Диффузионный и Мембранный потенциалы Стандартный электродный потенциал. Редокс электроды. Электроды, их классификация Расчёт Электродных потенциалов Электроды в гальванических цепях. Концентрационны е Б им еталлические С равнения О пределения. Гидратация ионов 1 и 2 -го рода t. Активность ионов И онселективны е
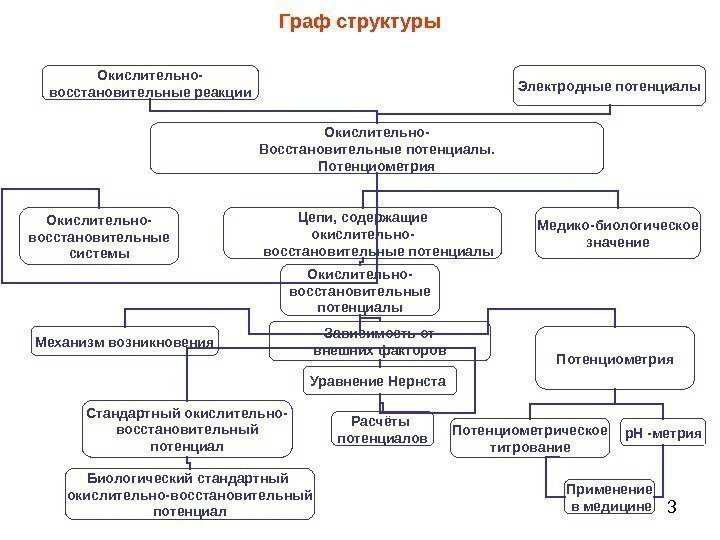
 3 Граф структуры Окислительно- восстановительные реакции Электродные потенциалы Окислительно- Восстановительные потенциалы. Потенциометрия Цепи, содержащие окислительно- восстановительные потенциалы. Окислительно- восстановительные системы Медико-биологическое значение Окислительно- восстановительные потенциалы Потенциометрия. Зависимость от внешних факторов. Механизм возникновения Уравнение Нернста Расчёты потенциалов. Стандартный окислительно- восстановительный потенциал Биологический стандартный окислительно-восстановительный потенциал Потенциометрическое титрование p. H -метрия Применение в медицине
3 Граф структуры Окислительно- восстановительные реакции Электродные потенциалы Окислительно- Восстановительные потенциалы. Потенциометрия Цепи, содержащие окислительно- восстановительные потенциалы. Окислительно- восстановительные системы Медико-биологическое значение Окислительно- восстановительные потенциалы Потенциометрия. Зависимость от внешних факторов. Механизм возникновения Уравнение Нернста Расчёты потенциалов. Стандартный окислительно- восстановительный потенциал Биологический стандартный окислительно-восстановительный потенциал Потенциометрическое титрование p. H -метрия Применение в медицине
 4(22. 09. 1791 — 25. 08. 1867) Д иректор лаборатории (1825 г. ) и профессор Королевского института (1827 г. ). Самостоятельно проводил исследования по химии к важнейшим из которых относятся получение бензола и сжижение хлора. Майкл Фарадей Английский физик и химик, член Лондонского королевского общества Электролиз Установил (1833 г. ) количественные законы электролиза.
4(22. 09. 1791 — 25. 08. 1867) Д иректор лаборатории (1825 г. ) и профессор Королевского института (1827 г. ). Самостоятельно проводил исследования по химии к важнейшим из которых относятся получение бензола и сжижение хлора. Майкл Фарадей Английский физик и химик, член Лондонского королевского общества Электролиз Установил (1833 г. ) количественные законы электролиза.
 5 Электролиз – окислительно-восстановительный процесс, происходящий на электродах при прохождении постоянного электрического тока через раствор или расплав электролита
5 Электролиз – окислительно-восстановительный процесс, происходящий на электродах при прохождении постоянного электрического тока через раствор или расплав электролита
 6 Анод(+) – положительно заряженный электрод, на аноде окисляются (теряют электроны) анионы (АА)!!!!!!! – к А ноду идут А нионы Катод(-) – отрицательно заряженный электрод, на катоде восстанавливаются (присоединяют электроны) катионы металлов и ионы Н + (ККК) !!!!!! – К К атоду идут К атионы
6 Анод(+) – положительно заряженный электрод, на аноде окисляются (теряют электроны) анионы (АА)!!!!!!! – к А ноду идут А нионы Катод(-) – отрицательно заряженный электрод, на катоде восстанавливаются (присоединяют электроны) катионы металлов и ионы Н + (ККК) !!!!!! – К К атоду идут К атионы
 7 При электролизе растворов или расплавов различных химических соединений одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные их химическим эквивалентам F = 96485 Кл/моль. Itm Fn M · F = q e · N A – количество электричества, переносимое 1 моль электронов (однозарядных ионов). n- число электронов
7 При электролизе растворов или расплавов различных химических соединений одинаковые количества электричества выделяют на электродах массы веществ, пропорциональные их химическим эквивалентам F = 96485 Кл/моль. Itm Fn M · F = q e · N A – количество электричества, переносимое 1 моль электронов (однозарядных ионов). n- число электронов
 8 Задача Рассчитать массу хрома полученного электролизом раствора сульфата хрома(III) в течение 100 мин при силе тока 75 А?
8 Задача Рассчитать массу хрома полученного электролизом раствора сульфата хрома(III) в течение 100 мин при силе тока 75 А?
 9 Решение Электролиз раствора сульфата хрома(III) можно представить cледующей схемой: Cr 2 (SO 4 ) 3 + 4 H 2 O → 2 Cr + H 2 ↑ + 2 O 2 ↑ + 3 H 2 SO 4 В процессе электролиза катион хрома принимает три электрона, превращаясь в атом: Cr 3+ +3 e → Cr 0 Itm Fn M · гm 84. 801006075 · 964853 52 Itm Fn M ·
9 Решение Электролиз раствора сульфата хрома(III) можно представить cледующей схемой: Cr 2 (SO 4 ) 3 + 4 H 2 O → 2 Cr + H 2 ↑ + 2 O 2 ↑ + 3 H 2 SO 4 В процессе электролиза катион хрома принимает три электрона, превращаясь в атом: Cr 3+ +3 e → Cr 0 Itm Fn M · гm 84. 801006075 · 964853 52 Itm Fn M ·
 10 Значение электролиза 1. Получение чистых металлов электролизом
10 Значение электролиза 1. Получение чистых металлов электролизом
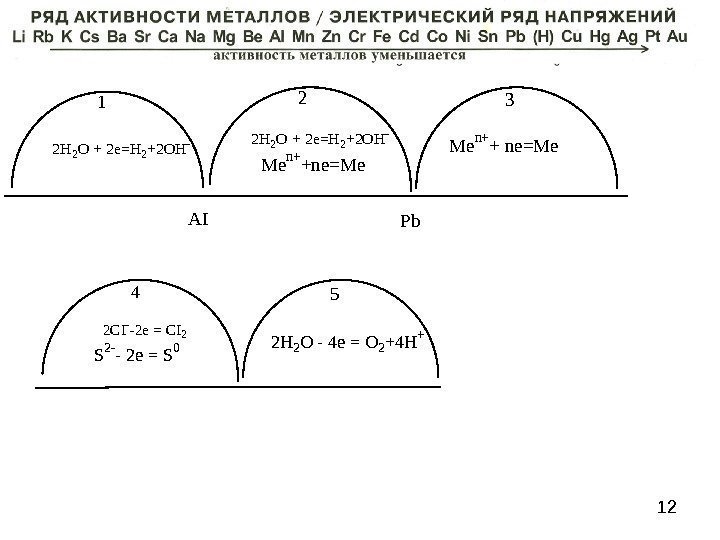
 11 2 C I — — 2 e = C I 2 S 2 — — 2 e = S 0 2 H 2 O — 4 e = O 2 + 4 H +4 5 2 H 2 O + 2 e=H 2+2 OH — Me n+ +ne=Me Me n+ + ne=Me Pb. AI 132 Инертный анод Восстановление на катоде (–) Окисление на аноде (+) Инертный катод Схема электролиза
11 2 C I — — 2 e = C I 2 S 2 — — 2 e = S 0 2 H 2 O — 4 e = O 2 + 4 H +4 5 2 H 2 O + 2 e=H 2+2 OH — Me n+ +ne=Me Me n+ + ne=Me Pb. AI 132 Инертный анод Восстановление на катоде (–) Окисление на аноде (+) Инертный катод Схема электролиза
 12 2 C I — — 2 e = C I 2 S 2 — — 2 e = S 0 2 H 2 O — 4 e = O 2 + 4 H +4 52 H 2 O + 2 e = H 2 + 2 O H — Men++ne=Me Men++ ne=Me Pb. AI
12 2 C I — — 2 e = C I 2 S 2 — — 2 e = S 0 2 H 2 O — 4 e = O 2 + 4 H +4 52 H 2 O + 2 e = H 2 + 2 O H — Men++ne=Me Men++ ne=Me Pb. AI
 13 Электролитическое копирование гравированных пластин для печатания бумажных денег 2. Гальваническое осаждение металлов
13 Электролитическое копирование гравированных пластин для печатания бумажных денег 2. Гальваническое осаждение металлов
 143. Создание химических источников тока. а) бытовые батарейки
143. Создание химических источников тока. а) бытовые батарейки
 15 Коррозия – совокупность самопроизвольных окислительно -восстановительных процессов под воздействием окружающей среды, приводящих к разрушению металла. Me n+ — n e → Me
15 Коррозия – совокупность самопроизвольных окислительно -восстановительных процессов под воздействием окружающей среды, приводящих к разрушению металла. Me n+ — n e → Me
 16 а) химическая – взаимодействие металлов с газами или жидкостями — неэлектролитами 2 Fe+3 SO 2 +3 O 2 Fe 2 (SO 4 ) 3 T
16 а) химическая – взаимодействие металлов с газами или жидкостями — неэлектролитами 2 Fe+3 SO 2 +3 O 2 Fe 2 (SO 4 ) 3 T
 17 б) электрохимическая (распространена в гораздо большей степени! ее и обсудим!)
17 б) электрохимическая (распространена в гораздо большей степени! ее и обсудим!)
 18 Металлы и их сплавы неоднородны, поэтому при контакте с водой на поверхности образуется множество гальванических пар. Большинство металлов окисляется кислородом воздуха, образуя на поверхности оксидные пленки. Если кристаллическая решетка оксида близка к кристаллической решетке металла, то эта пленка прочная, плотная, хорошо связана с поверхностью и защищает металл от дальнейшего разрушения. «Повезло» Zn, AI, Cr, Ni, Sn, Pb ! «Не повезло» железу, оксидная пленка которого рыхлая, пористая, легко отделяется от поверхности и не способна защитить его от коррозии !
18 Металлы и их сплавы неоднородны, поэтому при контакте с водой на поверхности образуется множество гальванических пар. Большинство металлов окисляется кислородом воздуха, образуя на поверхности оксидные пленки. Если кристаллическая решетка оксида близка к кристаллической решетке металла, то эта пленка прочная, плотная, хорошо связана с поверхностью и защищает металл от дальнейшего разрушения. «Повезло» Zn, AI, Cr, Ni, Sn, Pb ! «Не повезло» железу, оксидная пленка которого рыхлая, пористая, легко отделяется от поверхности и не способна защитить его от коррозии !
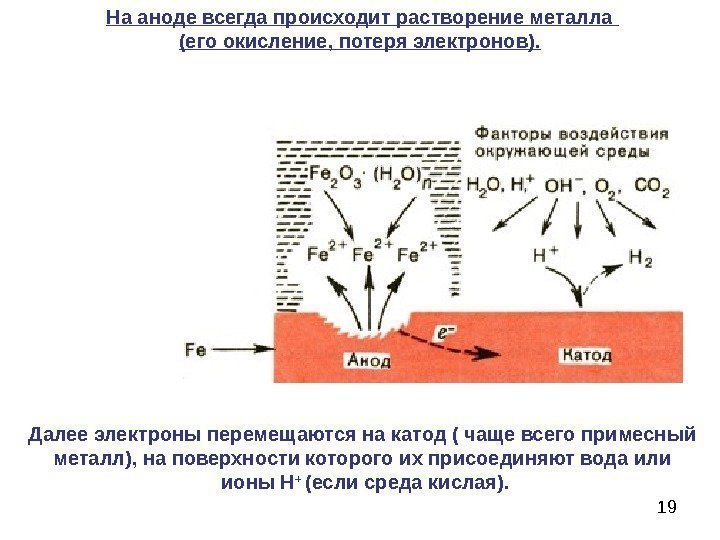
 19 Далее электроны перемещаются на катод ( чаще всего примесный металл), на поверхности которого их присоединяют вода или ионы Н + (если среда кислая). На аноде всегда происходит растворение металла (его окисление, потеря электронов).
19 Далее электроны перемещаются на катод ( чаще всего примесный металл), на поверхности которого их присоединяют вода или ионы Н + (если среда кислая). На аноде всегда происходит растворение металла (его окисление, потеря электронов).
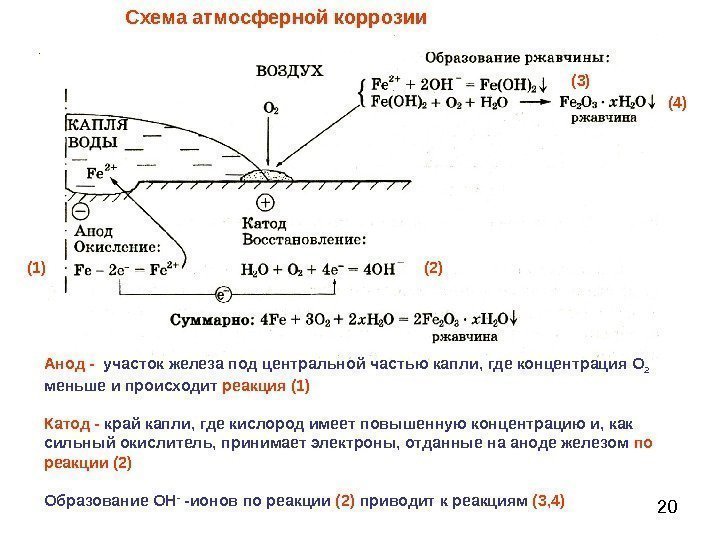
 20 Схема атмосферной коррозии Анод — участок железа под центральной частью капли, где концентрация О 2 меньше и происходит реакция (1) Катод — край капли, где кислород имеет повышенную концентрацию и, как сильный окислитель, принимает электроны, отданные на аноде железом по реакции (2) Образование ОН — -ионов по реакции (2) приводит к реакциям (3, 4)(1) (2) (3) (4)
20 Схема атмосферной коррозии Анод — участок железа под центральной частью капли, где концентрация О 2 меньше и происходит реакция (1) Катод — край капли, где кислород имеет повышенную концентрацию и, как сильный окислитель, принимает электроны, отданные на аноде железом по реакции (2) Образование ОН — -ионов по реакции (2) приводит к реакциям (3, 4)(1) (2) (3) (4)
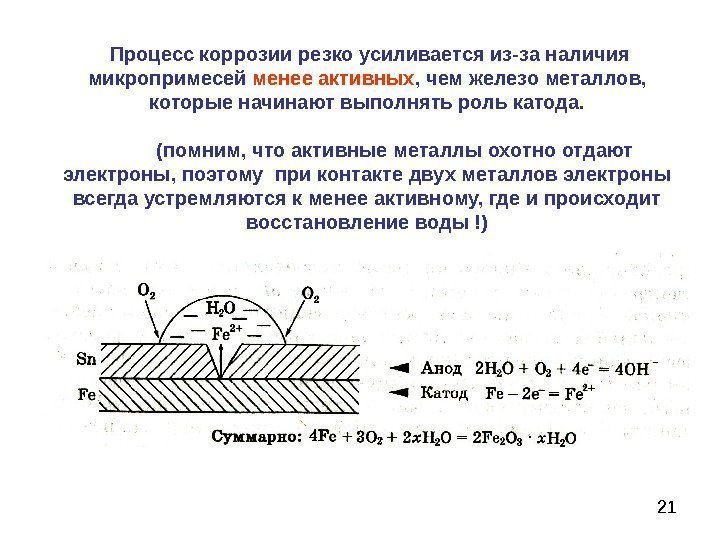
 21 Процесс коррозии резко усиливается из-за наличия микропримесей менее активных , чем железо металлов, которые начинают выполнять роль катода. (помним, что активные металлы охотно отдают электроны, поэтому при контакте двух металлов электроны всегда устремляются к менее активному, где и происходит восстановление воды !)
21 Процесс коррозии резко усиливается из-за наличия микропримесей менее активных , чем железо металлов, которые начинают выполнять роль катода. (помним, что активные металлы охотно отдают электроны, поэтому при контакте двух металлов электроны всегда устремляются к менее активному, где и происходит восстановление воды !)
 22 Защита от коррозии
22 Защита от коррозии
 231. Защитное покрытие (лаки, краски, пленки, смазки) – блокируется выход металла в виде ионов и доступ окислителей 2. Использование легированных сплавов — снижают скорость коррозии в конкретной коррозионно-активной среде.
231. Защитное покрытие (лаки, краски, пленки, смазки) – блокируется выход металла в виде ионов и доступ окислителей 2. Использование легированных сплавов — снижают скорость коррозии в конкретной коррозионно-активной среде.
 243. Введение ингибиторов коррозии –чаще всего при транспортировке агрессивных жидкостей по железной дороге или трубопроводам 4. Снижение агрессивности среды – деаэрация воды (удаление О 2 ) на промышленных предприятиях.
243. Введение ингибиторов коррозии –чаще всего при транспортировке агрессивных жидкостей по железной дороге или трубопроводам 4. Снижение агрессивности среды – деаэрация воды (удаление О 2 ) на промышленных предприятиях.
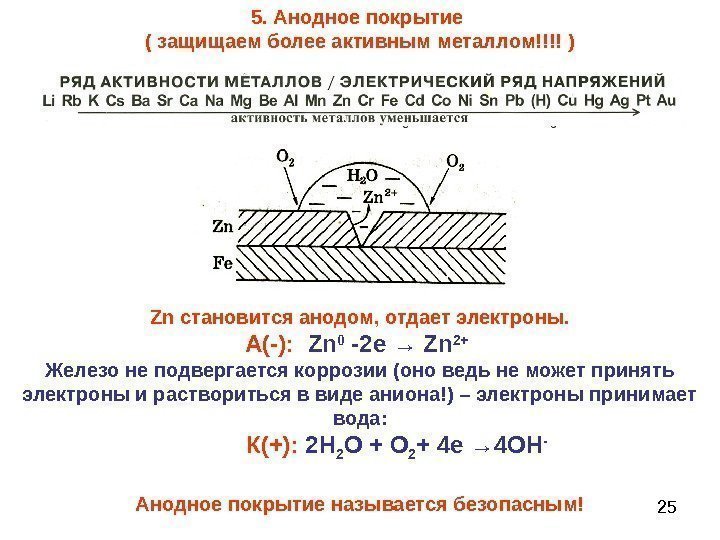
 255. Анодное покрытие ( защищаем более активным металлом!!!! ) Zn становится анодом, отдает электроны. А(-): Zn 0 -2 е → Zn 2+ Железо не подвергается коррозии (оно ведь не может принять электроны и раствориться в виде аниона!) – электроны принимает вода: К(+): 2 Н 2 О + О 2 + 4 е → 4 ОН — Анодное покрытие называется безопасным!
255. Анодное покрытие ( защищаем более активным металлом!!!! ) Zn становится анодом, отдает электроны. А(-): Zn 0 -2 е → Zn 2+ Железо не подвергается коррозии (оно ведь не может принять электроны и раствориться в виде аниона!) – электроны принимает вода: К(+): 2 Н 2 О + О 2 + 4 е → 4 ОН — Анодное покрытие называется безопасным!
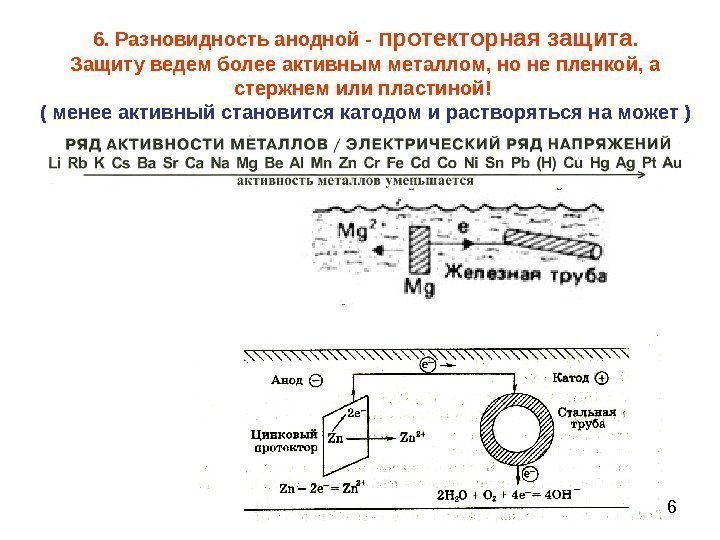
 266. Разновидность анодной — протекторная защита. Защиту ведем более активным металлом, но не пленкой, а стержнем или пластиной! ( менее активный становится катодом и растворяться на может )
266. Разновидность анодной — протекторная защита. Защиту ведем более активным металлом, но не пленкой, а стержнем или пластиной! ( менее активный становится катодом и растворяться на может )
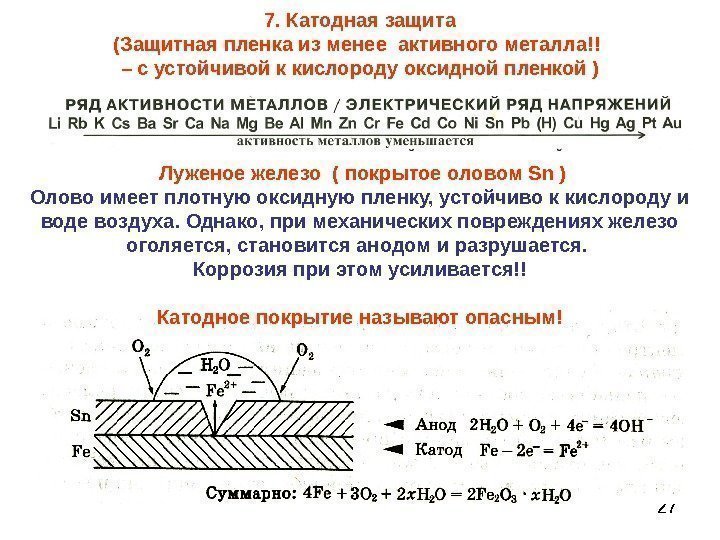
 277. Катодная защита (Защитная пленка из менее активного металла!! – с устойчивой к кислороду оксидной пленкой ) Луженое железо ( покрытое оловом Sn ) Олово имеет плотную оксидную пленку, устойчиво к кислороду и воде воздуха. Однако, при механических повреждениях железо оголяется, становится анодом и разрушается. Коррозия при этом усиливается!! Катодное покрытие называют опасным!
277. Катодная защита (Защитная пленка из менее активного металла!! – с устойчивой к кислороду оксидной пленкой ) Луженое железо ( покрытое оловом Sn ) Олово имеет плотную оксидную пленку, устойчиво к кислороду и воде воздуха. Однако, при механических повреждениях железо оголяется, становится анодом и разрушается. Коррозия при этом усиливается!! Катодное покрытие называют опасным!
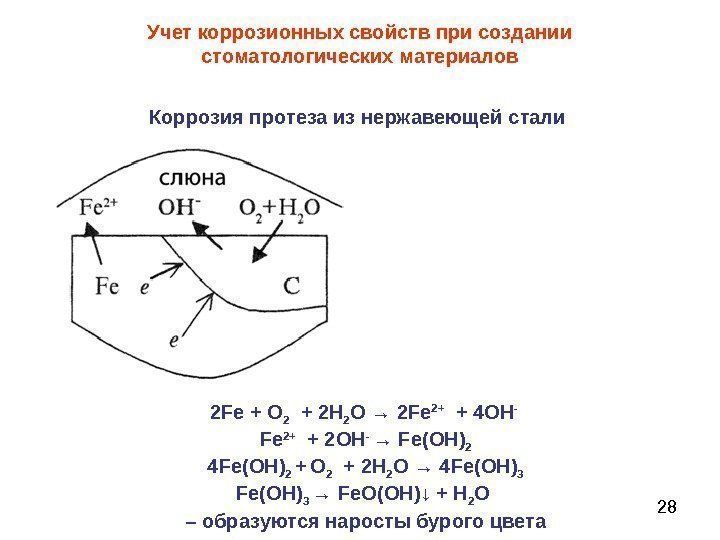
 28 Учет коррозионных свойств при создании стоматологических материалов Коррозия протеза из нержавеющей стали 2 Fe + О 2 + 2 Н 2 О → 2 Fe 2+ + 4 О H — Fe 2+ + 2 О H — → Fe (ОН) 2 4 Fe (ОН) 2 + О 2 + 2 Н 2 О → 4 Fe (ОН) 3 → Fe О(ОН) ↓ + Н 2 O – образуются наросты бурого цвета
28 Учет коррозионных свойств при создании стоматологических материалов Коррозия протеза из нержавеющей стали 2 Fe + О 2 + 2 Н 2 О → 2 Fe 2+ + 4 О H — Fe 2+ + 2 О H — → Fe (ОН) 2 4 Fe (ОН) 2 + О 2 + 2 Н 2 О → 4 Fe (ОН) 3 → Fe О(ОН) ↓ + Н 2 O – образуются наросты бурого цвета
 29 Параллельно протекает реакция Fe + 2 Н 2 O — 2 е→ Fe (ОН) 2 + 2 Н + — у больных с протезами из нержавеющей стали появляется кислый привкус и чувство жжения в полости рта
29 Параллельно протекает реакция Fe + 2 Н 2 O — 2 е→ Fe (ОН) 2 + 2 Н + — у больных с протезами из нержавеющей стали появляется кислый привкус и чувство жжения в полости рта
 30 Коррозия при контакте золотого и железного протезов 2 Fe + О 2 + 4 Н + → 2 Fe 2+ + 2 Н 2 0 φ 0 ( О 2 , 4 Н + /2 Н 2 0 ) = + 0. 875 В φ 0 ( F е 2+ / Fe) = — 0. 44 В Е= + 0. 875 — ( — 0. 44 ) = + 1. 315 В В отличие от обычного гальванического элемента, коррозионный элемент оказывается короткозамкнутым (электроны движутся внутри металла)
30 Коррозия при контакте золотого и железного протезов 2 Fe + О 2 + 4 Н + → 2 Fe 2+ + 2 Н 2 0 φ 0 ( О 2 , 4 Н + /2 Н 2 0 ) = + 0. 875 В φ 0 ( F е 2+ / Fe) = — 0. 44 В Е= + 0. 875 — ( — 0. 44 ) = + 1. 315 В В отличие от обычного гальванического элемента, коррозионный элемент оказывается короткозамкнутым (электроны движутся внутри металла)
 31 В 1888 — 1889 гг. Нернст изучал поведение электролитов при пропускании электрического тока и открыл фундаментальный закон, известный как уравнение Нернста. Закон устанавливает зависимость между электродвижущей силой (разностью потенциалов) и концентрацией ионов и позволяет предсказать максимальный потенциал, который может быть получен в результате электрохимического взаимодействия. Нобелевская премия по химии (1920) «в признание его работ по термодинамике» . Вальтер Нернст (25. 06. 1864 – 18. 11. 1941)[Red] [Ox] ln n. F RT ее о [Red] [Ox] lg n 0, 059 ее о Уравнение Нернста.
31 В 1888 — 1889 гг. Нернст изучал поведение электролитов при пропускании электрического тока и открыл фундаментальный закон, известный как уравнение Нернста. Закон устанавливает зависимость между электродвижущей силой (разностью потенциалов) и концентрацией ионов и позволяет предсказать максимальный потенциал, который может быть получен в результате электрохимического взаимодействия. Нобелевская премия по химии (1920) «в признание его работ по термодинамике» . Вальтер Нернст (25. 06. 1864 – 18. 11. 1941)[Red] [Ox] ln n. F RT ее о [Red] [Ox] lg n 0, 059 ее о Уравнение Нернста.
 32 Возникновение электродных потенциалов. Электроды I рода – металл, погруженный в раствор собственной соли. а) Цинковый электрод ( I рода) Zn 0 — 2ē = Zn 2+ (раств. ) Zn 2+ + 2ē = Zn 0 (осажд. ) Zn 0 — 2ē ↔ Zn 2+2 n. Z Zn 22 Zn/lg 2 0, 059 76. 0 a Zn. Znе Поскольку а Zn =1 , 76. 0 е/ 02 ВZn. Zn — граница раздела ж-ж — граница раздела тв-ж || |
32 Возникновение электродных потенциалов. Электроды I рода – металл, погруженный в раствор собственной соли. а) Цинковый электрод ( I рода) Zn 0 — 2ē = Zn 2+ (раств. ) Zn 2+ + 2ē = Zn 0 (осажд. ) Zn 0 — 2ē ↔ Zn 2+2 n. Z Zn 22 Zn/lg 2 0, 059 76. 0 a Zn. Znе Поскольку а Zn =1 , 76. 0 е/ 02 ВZn. Zn — граница раздела ж-ж — граница раздела тв-ж || |
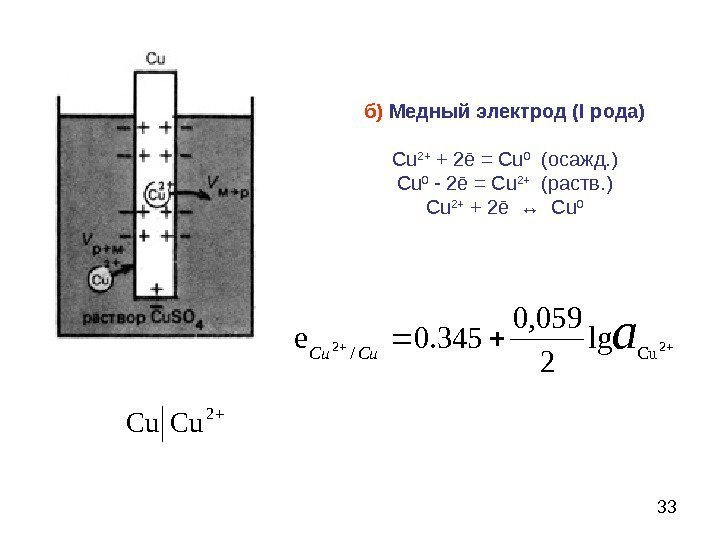
 3322 Cu/ lg 2 0, 059 345. 0 еa Cu. Cuб) Медный электрод ( I рода) Cu 2+ + 2ē = Cu 0 (осажд. ) Cu 0 — 2ē = Cu 2+ (раств. ) Cu 2+ + 2ē ↔ Cu 0 2 u. C Cu
3322 Cu/ lg 2 0, 059 345. 0 еa Cu. Cuб) Медный электрод ( I рода) Cu 2+ + 2ē = Cu 0 (осажд. ) Cu 0 — 2ē = Cu 2+ (раств. ) Cu 2+ + 2ē ↔ Cu 0 2 u. C Cu
 34 Платиновый электрод, покрытый платиновой чернью Водородный электрод в) Водородный электрод ( 1 рода, но… используется и как электрод сравнения, и как электрод определения ) 2 H + + 2ē = H 2 (окис. ) H 2 — 2ē = 2 H + (восст. ) 2 H + + 2ē ↔ H 2 2 H/ lg 20, 059 2 ao HH еер. Не. HH 059. 0 a 0, 059 lg 0 Н 2/ Потенциал стандартного водородного электрода для всех температур условно принят за ноль 0 0 2 Hе H H )Pt(2 Стандартный водородный электрод — электрод, в котором давление водорода — 101 к. Па, а активность ионов водорода -1 г-ион/л. ( а н+ = 1, р. Н = 0)
34 Платиновый электрод, покрытый платиновой чернью Водородный электрод в) Водородный электрод ( 1 рода, но… используется и как электрод сравнения, и как электрод определения ) 2 H + + 2ē = H 2 (окис. ) H 2 — 2ē = 2 H + (восст. ) 2 H + + 2ē ↔ H 2 2 H/ lg 20, 059 2 ao HH еер. Не. HH 059. 0 a 0, 059 lg 0 Н 2/ Потенциал стандартного водородного электрода для всех температур условно принят за ноль 0 0 2 Hе H H )Pt(2 Стандартный водородный электрод — электрод, в котором давление водорода — 101 к. Па, а активность ионов водорода -1 г-ион/л. ( а н+ = 1, р. Н = 0)
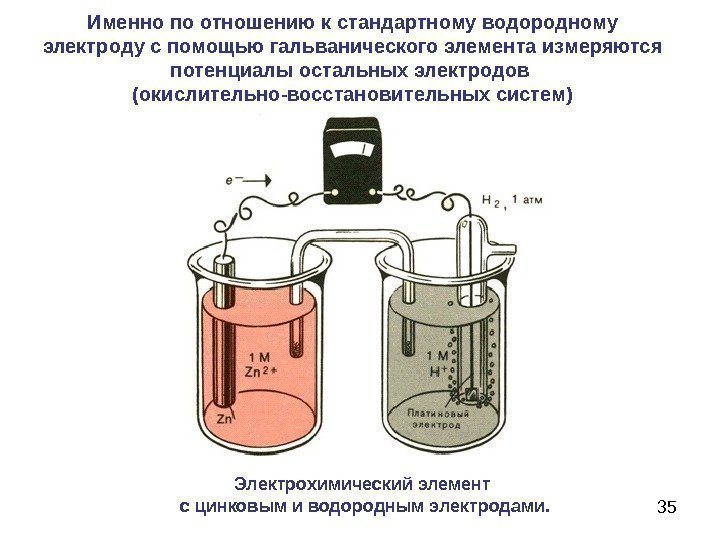
 35 Электрохимический элемент с цинковым и водородным электродами. Именно по отношению к стандартному водородному электроду с помощью гальванического элемента измеряются потенциалы остальных электродов (окислительно-восстановительных систем)
35 Электрохимический элемент с цинковым и водородным электродами. Именно по отношению к стандартному водородному электроду с помощью гальванического элемента измеряются потенциалы остальных электродов (окислительно-восстановительных систем)
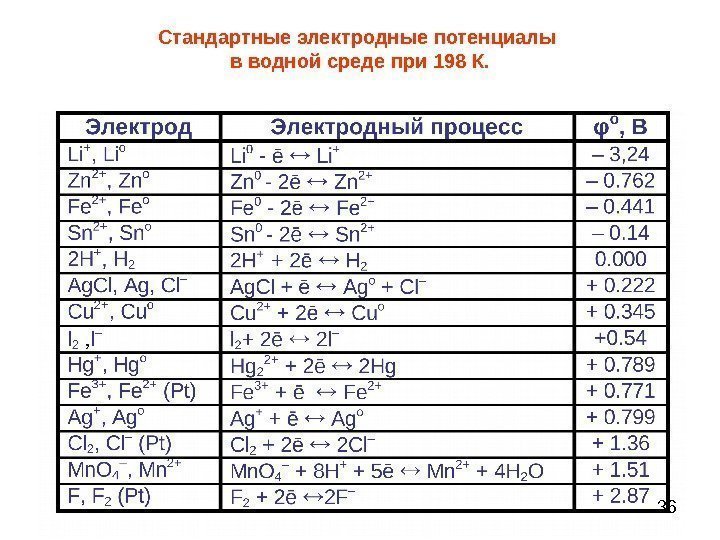
 36 Стандартные электродные потенциалы в водной среде при 198 К.
36 Стандартные электродные потенциалы в водной среде при 198 К.
 37 Пользуясь значениями е о , можно прогнозировать возможность протекания и направление окислительно-восстановительной реакции. F 2 + 2 e → 2 F — е 0 = 2. 87 В I 2 +2 e → 2 I — е 0 = 0. 54 В F 2 + 2 I — = I 2 + 2 F — F 2 + 2 KI = I 2 + 2 KF Из пары с большим е 0 берем окислитель. Из пары с меньшим е 0 – берем восстановитель. Оставшиеся вещества есть продукты реакции. Направление окислительно – восстановительных реакций
37 Пользуясь значениями е о , можно прогнозировать возможность протекания и направление окислительно-восстановительной реакции. F 2 + 2 e → 2 F — е 0 = 2. 87 В I 2 +2 e → 2 I — е 0 = 0. 54 В F 2 + 2 I — = I 2 + 2 F — F 2 + 2 KI = I 2 + 2 KF Из пары с большим е 0 берем окислитель. Из пары с меньшим е 0 – берем восстановитель. Оставшиеся вещества есть продукты реакции. Направление окислительно – восстановительных реакций
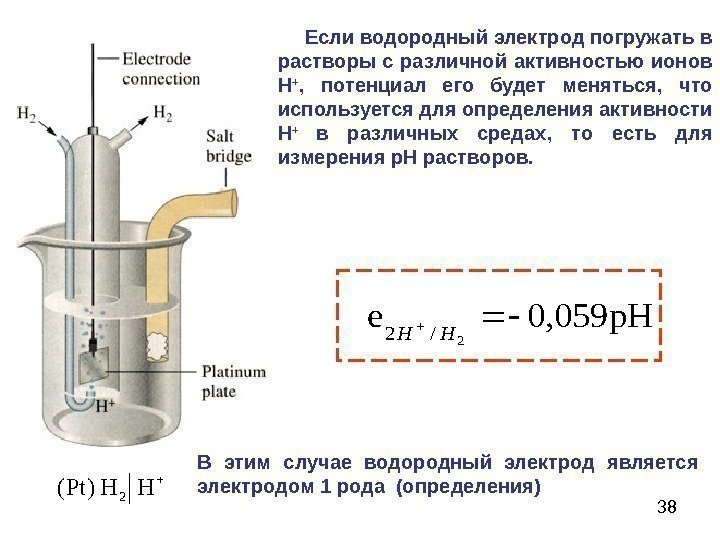
 38 Если водородный электрод погружать в растворы с различной активностью ионов Н + , потенциал его будет меняться, что используется для определения активности Н + в различных средах, то есть для измерения р. Н растворов. H H )Pt( 2 0, 059 p. Hе 2/2 HH В этим случае водородный электрод является электродом 1 рода (определения)
38 Если водородный электрод погружать в растворы с различной активностью ионов Н + , потенциал его будет меняться, что используется для определения активности Н + в различных средах, то есть для измерения р. Н растворов. H H )Pt( 2 0, 059 p. Hе 2/2 HH В этим случае водородный электрод является электродом 1 рода (определения)
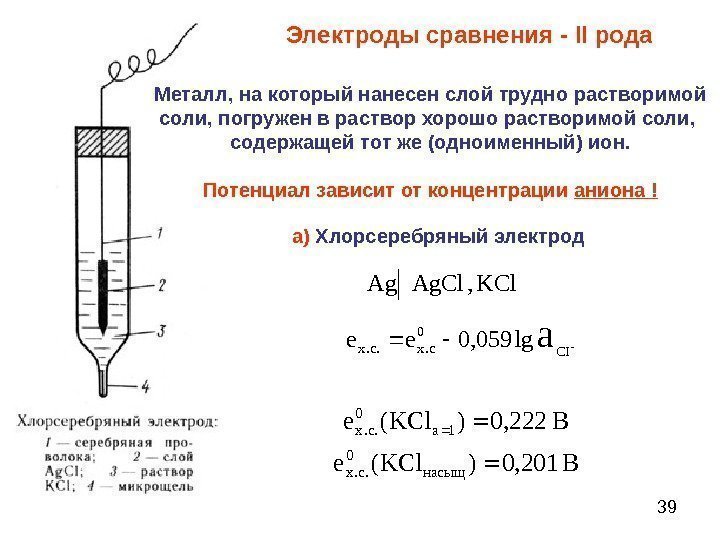
 39 Электроды сравнения — II рода а) Хлорсеребряный электрод KCl, Ag. Cl. Ag ВKClенасыщсх aсх 201, 0)( 222, 0)( 0. . 1 0. . Металл, на который нанесен слой трудно растворимой соли, погружен в раствор хорошо растворимой соли, содержащей тот же (одноименный) ион. Потенциал зависит от концентрации аниона ! CIсхсхaееlg 059, 0 0. . .
39 Электроды сравнения — II рода а) Хлорсеребряный электрод KCl, Ag. Cl. Ag ВKClенасыщсх aсх 201, 0)( 222, 0)( 0. . 1 0. . Металл, на который нанесен слой трудно растворимой соли, погружен в раствор хорошо растворимой соли, содержащей тот же (одноименный) ион. Потенциал зависит от концентрации аниона ! CIсхсхaееlg 059, 0 0. . .
 40 Ag. Ag. Ag aее lg 059, 00 // Cl K KCl Cl Ag Ag. Cl 10 10 Ag. Cl 10· 8, 1 1 10· 8, 1 ][Cl ПР ]Ag[ Ве е ПРе сх Cl сх Ag. Clсхa 222, 010· 8, 1 lg 059, 0799, 0 0. . 100. . Вывод уравнения потенциала хлорсеребряного электрода: 1 – серебряная проволока 2 – слой А g. CI 3 – раствор К CICI 4 – микрощель с асбестовой прокладкой
40 Ag. Ag. Ag aее lg 059, 00 // Cl K KCl Cl Ag Ag. Cl 10 10 Ag. Cl 10· 8, 1 1 10· 8, 1 ][Cl ПР ]Ag[ Ве е ПРе сх Cl сх Ag. Clсхa 222, 010· 8, 1 lg 059, 0799, 0 0. . 100. . Вывод уравнения потенциала хлорсеребряного электрода: 1 – серебряная проволока 2 – слой А g. CI 3 – раствор К CICI 4 – микрощель с асбестовой прокладкой
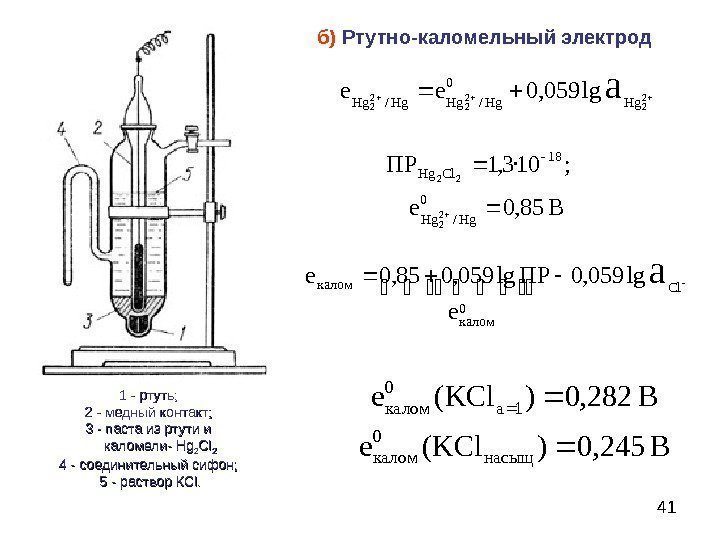
 41 б) Ртутно-каломельный электрод 1 — ртуть; 2 — медный контакт; 3 — паста из ртути и каломели — Hg. Hg 22 CICI 22 4 — соединительный сифон; 5 — раствор КС l. l. 222222 lg 059, 0 0 // Hg. Hg. Hgaее В 85, 0 ; 10· 3, 1 ПР 0 / 18 Cl. Hg 2 2 22 Hg. Hgе Cl 0 калом a lg 059, 0 е ПРlg 059, 085, 0 е ВKClе насыщкалом aкалом 245, 0)( 282, 0)(
41 б) Ртутно-каломельный электрод 1 — ртуть; 2 — медный контакт; 3 — паста из ртути и каломели — Hg. Hg 22 CICI 22 4 — соединительный сифон; 5 — раствор КС l. l. 222222 lg 059, 0 0 // Hg. Hg. Hgaее В 85, 0 ; 10· 3, 1 ПР 0 / 18 Cl. Hg 2 2 22 Hg. Hgе Cl 0 калом a lg 059, 0 е ПРlg 059, 085, 0 е ВKClе насыщкалом aкалом 245, 0)( 282, 0)(
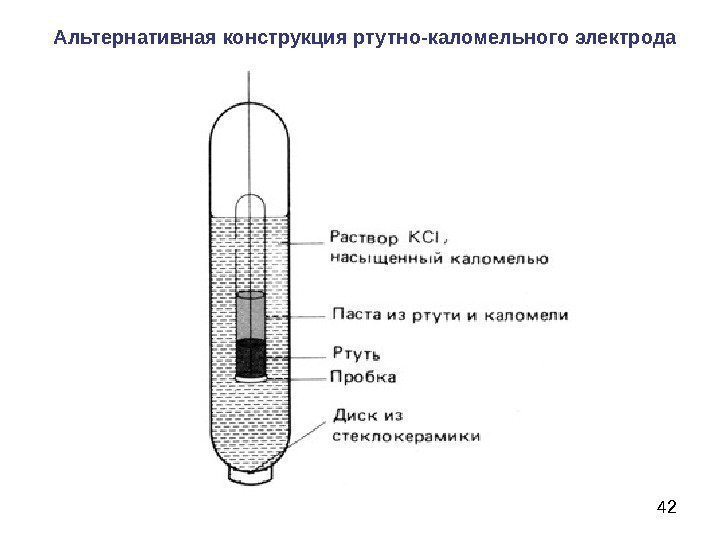
 42 Альтернативная конструкция ртутно-каломельного электрода
42 Альтернативная конструкция ртутно-каломельного электрода
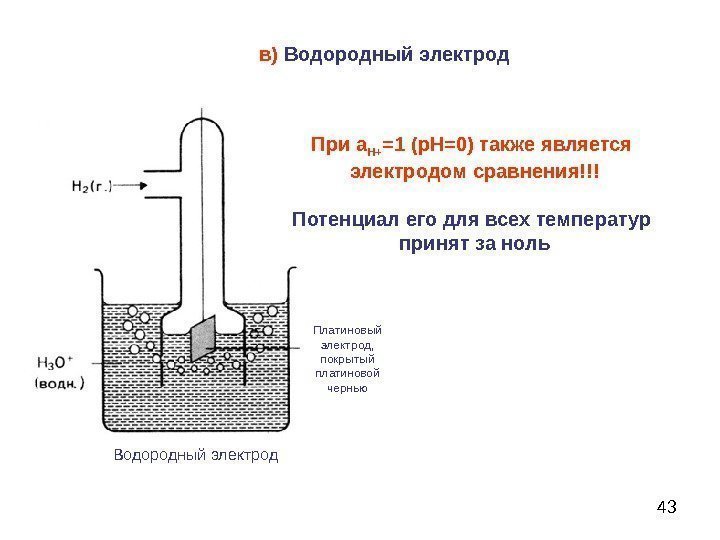
 43 Платиновый электрод, покрытый платиновой чернью Водородный электрод в) Водородный электрод При а Н+ =1 (р. Н=0) также является электродом сравнения!!! Потенциал его для всех температур принят за ноль
43 Платиновый электрод, покрытый платиновой чернью Водородный электрод в) Водородный электрод При а Н+ =1 (р. Н=0) также является электродом сравнения!!! Потенциал его для всех температур принят за ноль
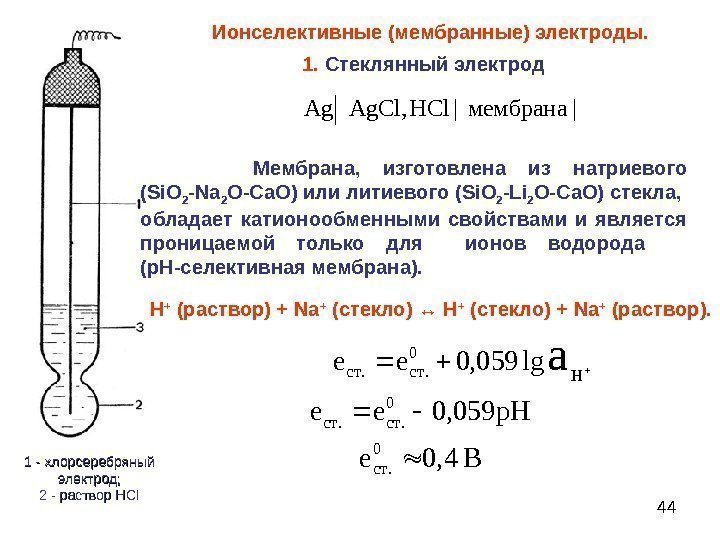
 44 Ионселективные (мембранные) электроды. 1 — хлорсеребряный электрод; 2 — раствор HCIHCI| мембрана |НClg. Cl, Ag. A 1. Стеклянный электрод Н + (раствор) + Na + (стекло) ↔ Н + (стекло) + Na + (раств op ). Мембрана, изготовлена из натриевого ( Si. O 2 — Na 2 O — Ca. O ) или литиевого ( Si. O 2 — Li 2 O — Ca. O ) стекла, обладает катионообменными свойствами и является проницаемой только для ионов водорода (р. Н-селективная мембрана). Ве р. Нее ее ст стст Hстст a 4, 0 059, 0 lg 059, 0 0. 0. .
44 Ионселективные (мембранные) электроды. 1 — хлорсеребряный электрод; 2 — раствор HCIHCI| мембрана |НClg. Cl, Ag. A 1. Стеклянный электрод Н + (раствор) + Na + (стекло) ↔ Н + (стекло) + Na + (раств op ). Мембрана, изготовлена из натриевого ( Si. O 2 — Na 2 O — Ca. O ) или литиевого ( Si. O 2 — Li 2 O — Ca. O ) стекла, обладает катионообменными свойствами и является проницаемой только для ионов водорода (р. Н-селективная мембрана). Ве р. Нее ее ст стст Hстст a 4, 0 059, 0 lg 059, 0 0. 0. .
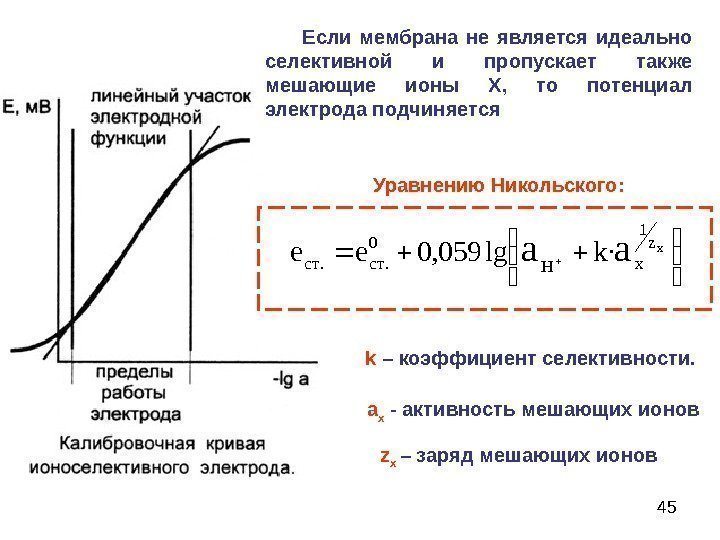
 45 Если мембрана не является идеально селективной и пропускает также мешающие ионы Х, то потенциал электрода подчиняется k – коэффициент селективности. xz x. Hстстaakее 1 0. . ·lg 059, 0 а x — активность мешающих ионов z x – заряд мешающих ионов. Уравнению Никольского:
45 Если мембрана не является идеально селективной и пропускает также мешающие ионы Х, то потенциал электрода подчиняется k – коэффициент селективности. xz x. Hстстaakее 1 0. . ·lg 059, 0 а x — активность мешающих ионов z x – заряд мешающих ионов. Уравнению Никольского:
 46 Советский физико-химик и радиохимик, академик. Окончил Ленинградский университет в 1925 году. НИКОЛЬСКИЙ Борис Петрович (14. 10. 1900 – 4. 01. 1990)
46 Советский физико-химик и радиохимик, академик. Окончил Ленинградский университет в 1925 году. НИКОЛЬСКИЙ Борис Петрович (14. 10. 1900 – 4. 01. 1990)
 47 С 1925 года работал в ЛГУ, одновременно с 1946 – в Радиевом институте. Предложил (1932– 1937) ионообменную теорию стеклянного электрода. Разработал (1932) потенциометрический метод титрования. Провел (1965– 1967) физико-химические исследования окислительно-восстановительной системы ферроцен – катион феррициния (компонент твердого ракетного топлива) Выполнил цикл работ в области прикладной и теоретической радиохимии.
47 С 1925 года работал в ЛГУ, одновременно с 1946 – в Радиевом институте. Предложил (1932– 1937) ионообменную теорию стеклянного электрода. Разработал (1932) потенциометрический метод титрования. Провел (1965– 1967) физико-химические исследования окислительно-восстановительной системы ферроцен – катион феррициния (компонент твердого ракетного топлива) Выполнил цикл работ в области прикладной и теоретической радиохимии.
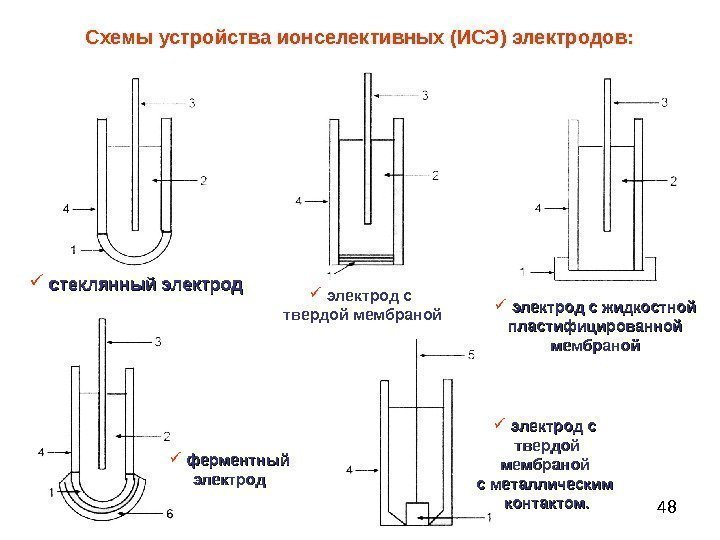
 48 Схемы устройства ионселективных (ИСЭ) электродов: электрод с твердой мембраной с металлическим контактом. стеклянный электрод с твердой мембраной электрод с жидкостной пластифицированной мембраной ферментный электрод
48 Схемы устройства ионселективных (ИСЭ) электродов: электрод с твердой мембраной с металлическим контактом. стеклянный электрод с твердой мембраной электрод с жидкостной пластифицированной мембраной ферментный электрод
 49 Обладают селективностью к катионам Cu 2+ , Mg 2+ , Mn 2+ , NH 4 + , анионам NO 3 – , СО 3 2– , SO 4 2 -. Наиболее важными для решения экологических проблем являются электроды, селективные к поверхностно-активным веществам (определение загрязнений моющими средствами) и к ацетилхолину (определение загрязнений фосфорорганическими ядохимикатами). Механическая непрочность пористых мембран, неизбежное попадание органической фазы в анализируемый раствор затрудняют применение ИСЭ с жидкими мембранами в биомедицинских исследованиях. электрод с жидкостной пластифицированной мембраной 2. Жидкостные ионселективные (ИСЭ) электроды
49 Обладают селективностью к катионам Cu 2+ , Mg 2+ , Mn 2+ , NH 4 + , анионам NO 3 – , СО 3 2– , SO 4 2 -. Наиболее важными для решения экологических проблем являются электроды, селективные к поверхностно-активным веществам (определение загрязнений моющими средствами) и к ацетилхолину (определение загрязнений фосфорорганическими ядохимикатами). Механическая непрочность пористых мембран, неизбежное попадание органической фазы в анализируемый раствор затрудняют применение ИСЭ с жидкими мембранами в биомедицинских исследованиях. электрод с жидкостной пластифицированной мембраной 2. Жидкостные ионселективные (ИСЭ) электроды
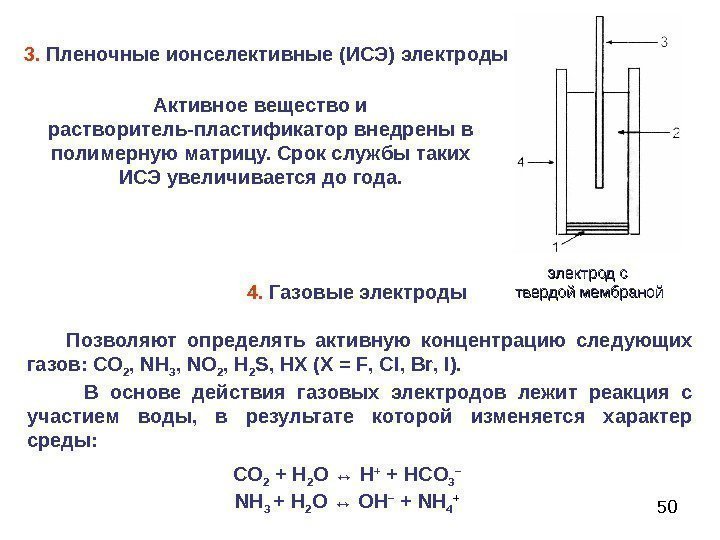
 503. Пленочные ионселективные (ИСЭ) электроды 4. Газовые электроды Позволяют определять активную концентрацию следующих газов: СО 2 , NH 3 , NO 2 , H 2 S , HX ( X = F , Cl , Br , I ). В основе действия газовых электродов лежит реакция с участием воды, в результате которой изменяется характер среды: СО 2 + Н 2 О ↔ Н + + HCO 3 – NH 3 + H 2 O ↔ OH – + NH 4 +Активное вещество и растворитель-пластификатор внедрены в полимерную матрицу. Срок службы таких ИСЭ увеличивается до года. электрод с твердой мембраной
503. Пленочные ионселективные (ИСЭ) электроды 4. Газовые электроды Позволяют определять активную концентрацию следующих газов: СО 2 , NH 3 , NO 2 , H 2 S , HX ( X = F , Cl , Br , I ). В основе действия газовых электродов лежит реакция с участием воды, в результате которой изменяется характер среды: СО 2 + Н 2 О ↔ Н + + HCO 3 – NH 3 + H 2 O ↔ OH – + NH 4 +Активное вещество и растворитель-пластификатор внедрены в полимерную матрицу. Срок службы таких ИСЭ увеличивается до года. электрод с твердой мембраной
 51 Созданы на основе иммобилизованных ферментов включенных в мембрану. Потенциал их зависит от концентрации продуктов распада. Используются для определения концентрации не только продуктов ферментативной реакции, но и любого участвующего в этой реакции вещества. Помимо высокой чувствительности позволяют определять вещества не по функциональным группам а по их биологическому действию. 5. Ферментные электроды ферментный электрод Определяемое вещество Фермент, включенный в мембрану Вещество, определяемое датчиком Глюкоза Глюкозооксидаза Н 2 О 2 Мочевина Уреаза N Н 4 + Глутаминаза N Н 4 + Аспарагиназа N Н 4 + L- аминокислоты L -аминооксидаза N Н 4 + D- аминокислоты D -аминооксидаза N Н 4 + Амигдалин β -глюкозидаза С N-
51 Созданы на основе иммобилизованных ферментов включенных в мембрану. Потенциал их зависит от концентрации продуктов распада. Используются для определения концентрации не только продуктов ферментативной реакции, но и любого участвующего в этой реакции вещества. Помимо высокой чувствительности позволяют определять вещества не по функциональным группам а по их биологическому действию. 5. Ферментные электроды ферментный электрод Определяемое вещество Фермент, включенный в мембрану Вещество, определяемое датчиком Глюкоза Глюкозооксидаза Н 2 О 2 Мочевина Уреаза N Н 4 + Глутаминаза N Н 4 + Аспарагиназа N Н 4 + L- аминокислоты L -аминооксидаза N Н 4 + D- аминокислоты D -аминооксидаза N Н 4 + Амигдалин β -глюкозидаза С N-
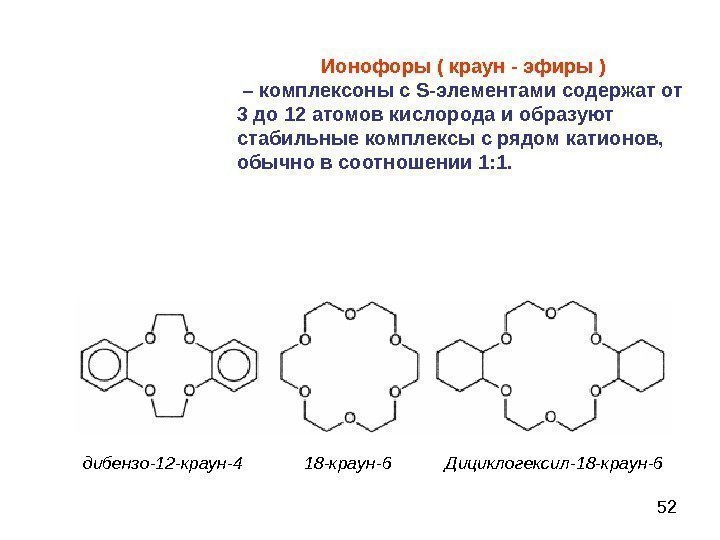
 52 Ионофоры ( краун — эфиры ) – комплексоны с S- элементами содержат от 3 до 12 атомов кислорода и образуют стабильные комплексы с рядом катионов, обычно в соотношении 1: 1. дибензо — 12 — краун — 4 18 — краун — 6 Дициклогексил — 18 — краун —
52 Ионофоры ( краун — эфиры ) – комплексоны с S- элементами содержат от 3 до 12 атомов кислорода и образуют стабильные комплексы с рядом катионов, обычно в соотношении 1: 1. дибензо — 12 — краун — 4 18 — краун — 6 Дициклогексил — 18 — краун —
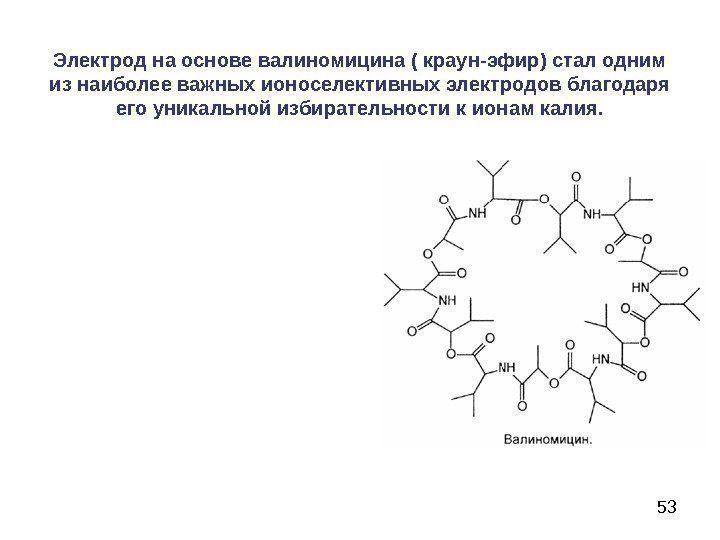
 53 Электрод на основе валиномицина ( краун-эфир) стал одним из наиболее важных ионоселективных электродов благодаря его уникальной избирательности к ионам калия.
53 Электрод на основе валиномицина ( краун-эфир) стал одним из наиболее важных ионоселективных электродов благодаря его уникальной избирательности к ионам калия.
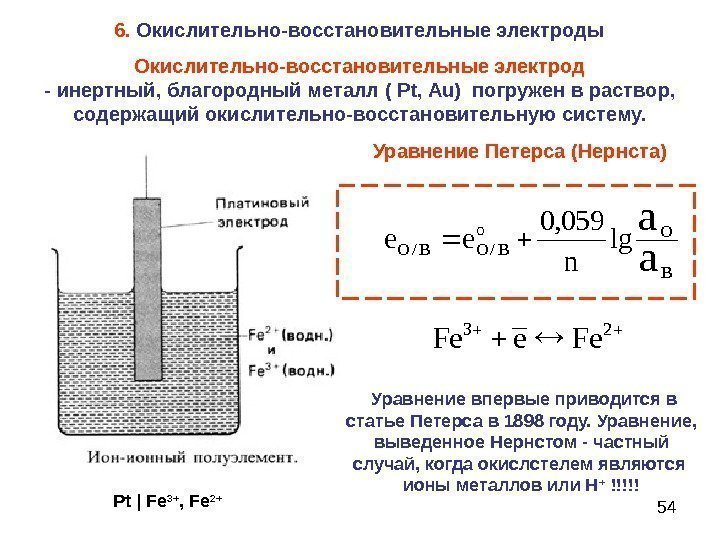
 54 Окислительно-восстановительные электрод — инертный, благородный металл ( Pt, Au ) погружен в раствор, содержащий окислительно-восстановительную систему. 23 Fee. Fe. B Oо ВОВО aa n ееlg 059, 0 //Уравнение Петерса (Нернста) Pt | Fe 3+ , Fe 2+6. Окислительно-восстановительные электроды Уравнение впервые приводится в статье Петерса в 1898 году. Уравнение, выведенное Нернстом — частный случай, когда окислстелем являются ионы металлов или Н + !!!!!
54 Окислительно-восстановительные электрод — инертный, благородный металл ( Pt, Au ) погружен в раствор, содержащий окислительно-восстановительную систему. 23 Fee. Fe. B Oо ВОВО aa n ееlg 059, 0 //Уравнение Петерса (Нернста) Pt | Fe 3+ , Fe 2+6. Окислительно-восстановительные электроды Уравнение впервые приводится в статье Петерса в 1898 году. Уравнение, выведенное Нернстом — частный случай, когда окислстелем являются ионы металлов или Н + !!!!!
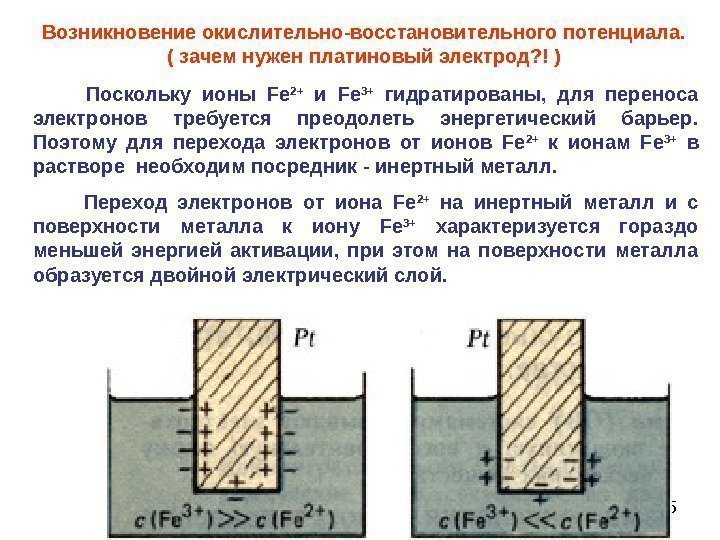
 55 Возникновение окислительно-восстановительного потенциала. ( зачем нужен платиновый электрод? ! ) Поскольку ионы Fe 2+ и Fe 3+ гидратированы, для переноса электронов требуется преодолеть энергетический барьер. Поэтому для перехода электронов от ионов Fe 2+ к ионам Fe 3+ в растворе необходим посредник — инертный металл. Переход электронов от иона Fe 2+ на инертный металл и с поверхности металла к иону Fe 3+ характеризуется гораздо меньшей энергией активации, при этом на поверхности металла образуется двойной электрический слой.
55 Возникновение окислительно-восстановительного потенциала. ( зачем нужен платиновый электрод? ! ) Поскольку ионы Fe 2+ и Fe 3+ гидратированы, для переноса электронов требуется преодолеть энергетический барьер. Поэтому для перехода электронов от ионов Fe 2+ к ионам Fe 3+ в растворе необходим посредник — инертный металл. Переход электронов от иона Fe 2+ на инертный металл и с поверхности металла к иону Fe 3+ характеризуется гораздо меньшей энергией активации, при этом на поверхности металла образуется двойной электрический слой.
 56 Если в окислительно-восстановительное уравнение входят ионы водорода, то потенциал данной системы зависит также от р. Н раствора: OH 4 Mne 5 H 8 Mn. O 2 2 4 24 2 4 8 / · lg 5059, 0 51, 1 Mn HMn. O a aa е В сильнокислых средах окислительная способность таких систем резко возрастает ! В 0, 85 e )10( 7 р. Н при В 1, 51 e 1)( 0 р. Н при 7 H H a a
56 Если в окислительно-восстановительное уравнение входят ионы водорода, то потенциал данной системы зависит также от р. Н раствора: OH 4 Mne 5 H 8 Mn. O 2 2 4 24 2 4 8 / · lg 5059, 0 51, 1 Mn HMn. O a aa е В сильнокислых средах окислительная способность таких систем резко возрастает ! В 0, 85 e )10( 7 р. Н при В 1, 51 e 1)( 0 р. Н при 7 H H a a
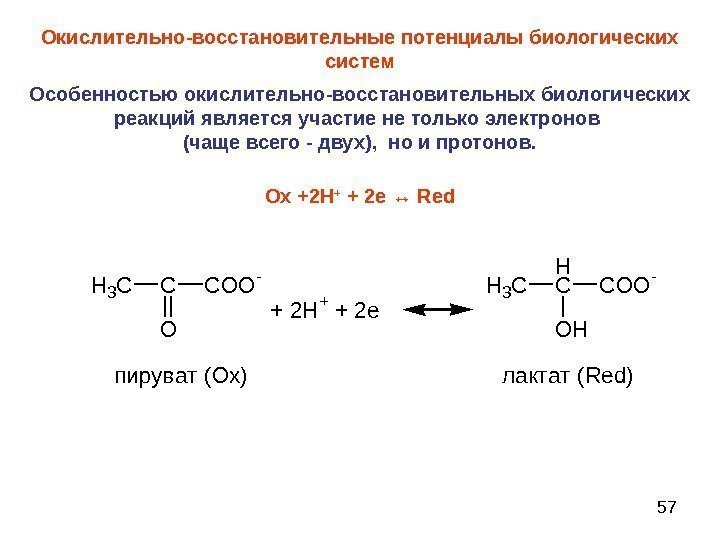
 57 Окислительно-восстановительные потенциалы биологических систем Особенностью окислительно-восстановительных биологических реакций является участие не только электронов (чаще всего — двух), но и протонов. O х +2 H + + 2 e ↔ Red H 3 C C O O — + 2 H + + 2 e H 3 C H C O O — п и р у в а т ( O x ) л а к т а т ( R e d )
57 Окислительно-восстановительные потенциалы биологических систем Особенностью окислительно-восстановительных биологических реакций является участие не только электронов (чаще всего — двух), но и протонов. O х +2 H + + 2 e ↔ Red H 3 C C O O — + 2 H + + 2 e H 3 C H C O O — п и р у в а т ( O x ) л а к т а т ( R e d )
 58 Так как большинство физиологических жидкостей имеют значение р. Н, близкое к 7, для биологических систем вводится нормальный восстановительный потенциал при р. Н=7 Уравнение Нернста ( Петерса ) принимает вид: B Oо В/О. норм aa lg 2059, 0 р. Н 059. 0 ее B Oо. станд. норм a a lg 2 059, 0 ее В 413. 0 е 7059. 0 ее 0 В/О о В/О 0. станд где
58 Так как большинство физиологических жидкостей имеют значение р. Н, близкое к 7, для биологических систем вводится нормальный восстановительный потенциал при р. Н=7 Уравнение Нернста ( Петерса ) принимает вид: B Oо В/О. норм aa lg 2059, 0 р. Н 059. 0 ее B Oо. станд. норм a a lg 2 059, 0 ее В 413. 0 е 7059. 0 ее 0 В/О о В/О 0. станд где
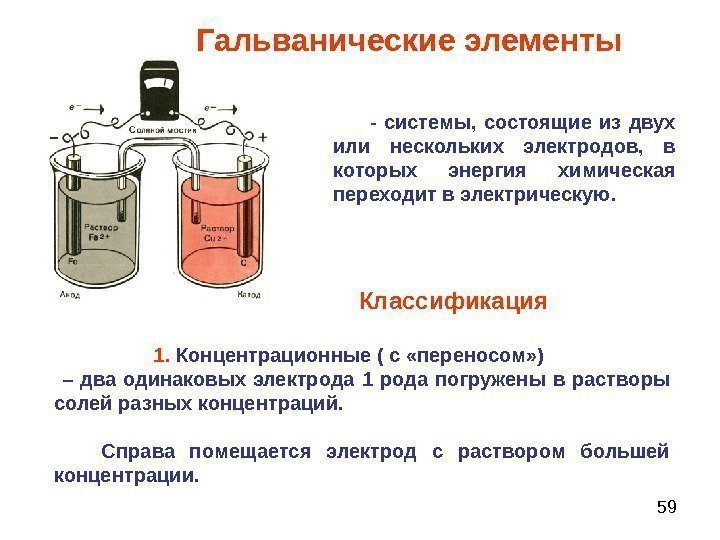
 59 — системы, состоящие из двух или нескольких электродов, в которых энергия химическая переходит в электрическую. 1. Концентрационные ( c «переносом» ) – два одинаковых электрода 1 рода погружены в растворы солей разных концентраций. Справа помещается электрод с раствором большей концентрации. Гальванические элементы Классификация
59 — системы, состоящие из двух или нескольких электродов, в которых энергия химическая переходит в электрическую. 1. Концентрационные ( c «переносом» ) – два одинаковых электрода 1 рода погружены в растворы солей разных концентраций. Справа помещается электрод с раствором большей концентрации. Гальванические элементы Классификация
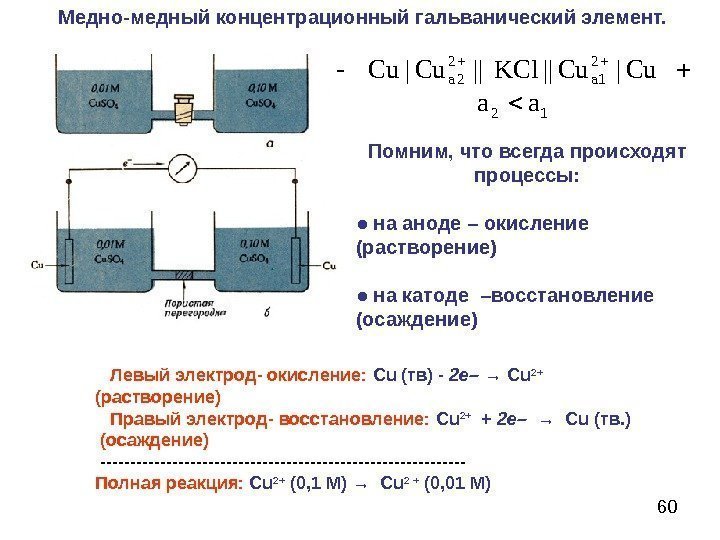
 60 Медно-медный концентрационный гальванический элемент. 12 2 a 1 2 2 a aa Cu|Cu||KCl ||Cu|Cu Левый электрод- окисление: С u (тв) — 2 е– → С u 2+ (растворение) Правый электрод- восстановление: С u 2+ + 2 е– → С u (тв. ) (осаждение) ——————————- Полная реакция: С u 2+ (0, 1 М) → С u 2 + (0, 01 М)Помним, что всегда происходят процессы: ● на аноде – окисление (растворение) ● на катоде – восстановление (осаждение)
60 Медно-медный концентрационный гальванический элемент. 12 2 a 1 2 2 a aa Cu|Cu||KCl ||Cu|Cu Левый электрод- окисление: С u (тв) — 2 е– → С u 2+ (растворение) Правый электрод- восстановление: С u 2+ + 2 е– → С u (тв. ) (осаждение) ——————————- Полная реакция: С u 2+ (0, 1 М) → С u 2 + (0, 01 М)Помним, что всегда происходят процессы: ● на аноде – окисление (растворение) ● на катоде – восстановление (осаждение)
 61 Расчет ЭДС для концентрационных гальванических элементов 12 2 a 12 2 a aa Cu|Cu||KCl ||Cu|Cu 2 2 Cu 2 Сu 1 a a lg 2059, 001. 0 lg 2 059, 0 E 22 Cu. Cu/Cu 1 1 lg 20, 059 345. 0 еa Е = е 1 — е 2 22 Cu. Cu/Cu 2 2 lg 20, 059 345. 0 е a 2 Cu 1 lg 2 0, 059 345. 0 Еa 2 Cu 2 lg 20, 059 345. 0 a 21 а а lg 2059, 0 E Ток в цепи прекращается, когда концентрации (активности) становятся одинаковыми
61 Расчет ЭДС для концентрационных гальванических элементов 12 2 a 12 2 a aa Cu|Cu||KCl ||Cu|Cu 2 2 Cu 2 Сu 1 a a lg 2059, 001. 0 lg 2 059, 0 E 22 Cu. Cu/Cu 1 1 lg 20, 059 345. 0 еa Е = е 1 — е 2 22 Cu. Cu/Cu 2 2 lg 20, 059 345. 0 е a 2 Cu 1 lg 2 0, 059 345. 0 Еa 2 Cu 2 lg 20, 059 345. 0 a 21 а а lg 2059, 0 E Ток в цепи прекращается, когда концентрации (активности) становятся одинаковыми
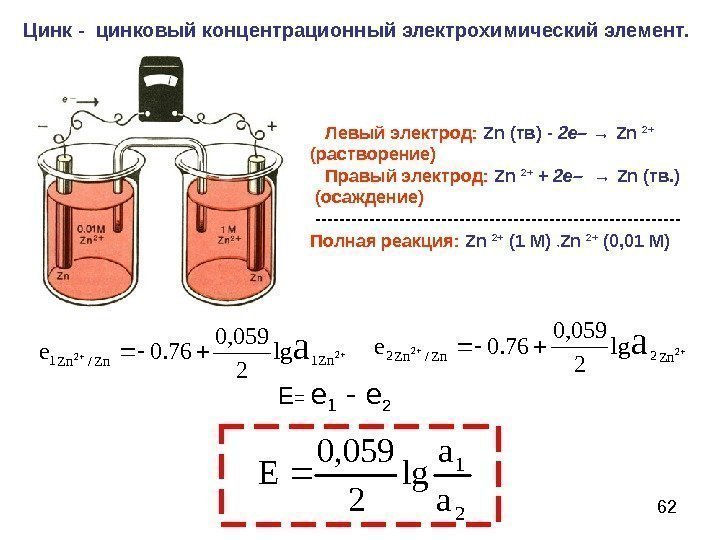
 62 Цинк — цинковый концентрационный электрохимический элемент. 22 Zn 1 Zn/Zn 1 alg 2 0, 059 76. 0 е 22 Zn/Zn 2 alg 2 0, 059 76. 0 е Е = е 1 — е 2 Левый электрод: Zn (тв) — 2 е– → Zn 2+ (растворение) Правый электрод: Zn 2+ + 2 е– → Zn (тв. ) (осаждение) ——————————- Полная реакция: Zn 2+ (1 М) → Zn 2+ (0, 01 М) 21 а а lg 2059,
62 Цинк — цинковый концентрационный электрохимический элемент. 22 Zn 1 Zn/Zn 1 alg 2 0, 059 76. 0 е 22 Zn/Zn 2 alg 2 0, 059 76. 0 е Е = е 1 — е 2 Левый электрод: Zn (тв) — 2 е– → Zn 2+ (растворение) Правый электрод: Zn 2+ + 2 е– → Zn (тв. ) (осаждение) ——————————- Полная реакция: Zn 2+ (1 М) → Zn 2+ (0, 01 М) 21 а а lg 2059,
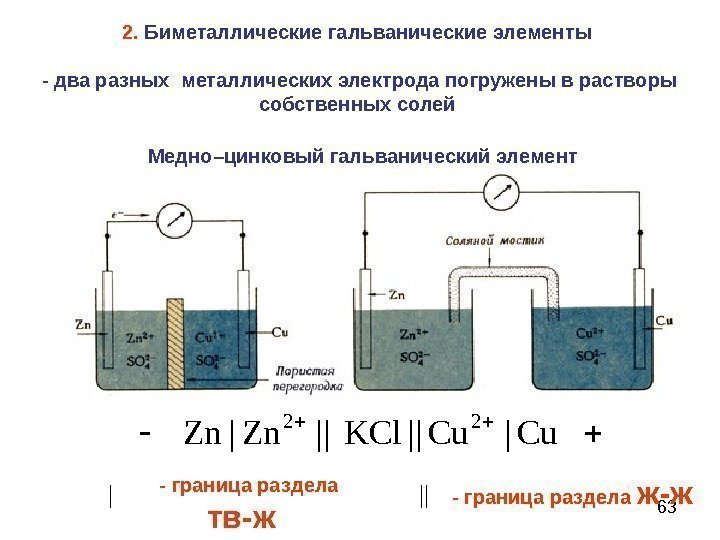
 63 Медно–цинковый гальванический элемент Cu|Cu||KCl ||Zn| Zn 22 | || — граница раздела тв-ж — граница раздела ж-ж 2. Биметаллические гальванические элементы — два разных металлических электрода погружены в растворы собственных солей
63 Медно–цинковый гальванический элемент Cu|Cu||KCl ||Zn| Zn 22 | || — граница раздела тв-ж — граница раздела ж-ж 2. Биметаллические гальванические элементы — два разных металлических электрода погружены в растворы собственных солей
 641 22 Zn. Cuaa. При В 1, 1)76, 0(34, 0 E 2 2 Zn Cu a a lg 2 059, 0 1, 1 E 22 22 lg 2 059, 0 е/ 0 Zn. Zn. Cu. Cuaa. E Zn. Cu. Cu ее. E // 22 Расчет ЭДС в биметаллических гальванических элементах При разных активностях: 2/ 0 1 2 059, 0 lg 2 059, 0 eе 222 Zn g. Ea Cu. Zn. Cua
641 22 Zn. Cuaa. При В 1, 1)76, 0(34, 0 E 2 2 Zn Cu a a lg 2 059, 0 1, 1 E 22 22 lg 2 059, 0 е/ 0 Zn. Zn. Cu. Cuaa. E Zn. Cu. Cu ее. E // 22 Расчет ЭДС в биметаллических гальванических элементах При разных активностях: 2/ 0 1 2 059, 0 lg 2 059, 0 eе 222 Zn g. Ea Cu. Zn. Cua
 65 3. Гальванические элементы без переноса Правила составления: Справа помещаем электрод с большим е 0 ; Для электрода определения пишем уравнение Нернста, для электрода сравнения – цифру; ЭДС – разность потенциалов правого и левого электродов ВKClенасыщсх aсх 201, 0)( 222, 0)( 0. . 1 0. . 0 0. водородне
65 3. Гальванические элементы без переноса Правила составления: Справа помещаем электрод с большим е 0 ; Для электрода определения пишем уравнение Нернста, для электрода сравнения – цифру; ЭДС – разность потенциалов правого и левого электродов ВKClенасыщсх aсх 201, 0)( 222, 0)( 0. . 1 0. . 0 0. водородне
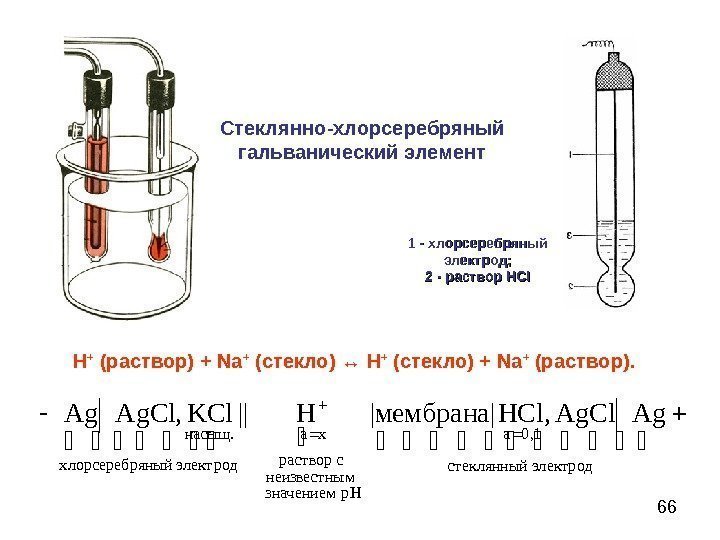
 66 электродстеклянный 1, 0 a р. Нзначением м неизвестны раствор с xa родяный электхлорсеребр насыщ. Ag. Cl, HClмембрана| |H|| KCl, Ag. Cl. Ag Стеклянно-хлорсеребряный гальванический элемент Н + (раствор) + Na + (стекло) ↔ Н + (стекло) + Na + (раств op ). 1 — хлорсеребряный электрод; 2 — раствор HCIHCI
66 электродстеклянный 1, 0 a р. Нзначением м неизвестны раствор с xa родяный электхлорсеребр насыщ. Ag. Cl, HClмембрана| |H|| KCl, Ag. Cl. Ag Стеклянно-хлорсеребряный гальванический элемент Н + (раствор) + Na + (стекло) ↔ Н + (стекло) + Na + (раств op ). 1 — хлорсеребряный электрод; 2 — раствор HCIHCI
 67 Расчет ЭДС для стеклянно-хлорсеребряного гальванического элемента 059, 0199, 0 059, 0 201, 0400, 0 201, 0059, 00. E p. H р. НE р. Не. E ее. E ст схст
67 Расчет ЭДС для стеклянно-хлорсеребряного гальванического элемента 059, 0199, 0 059, 0 201, 0400, 0 201, 0059, 00. E p. H р. НE р. Не. E ее. E ст схст
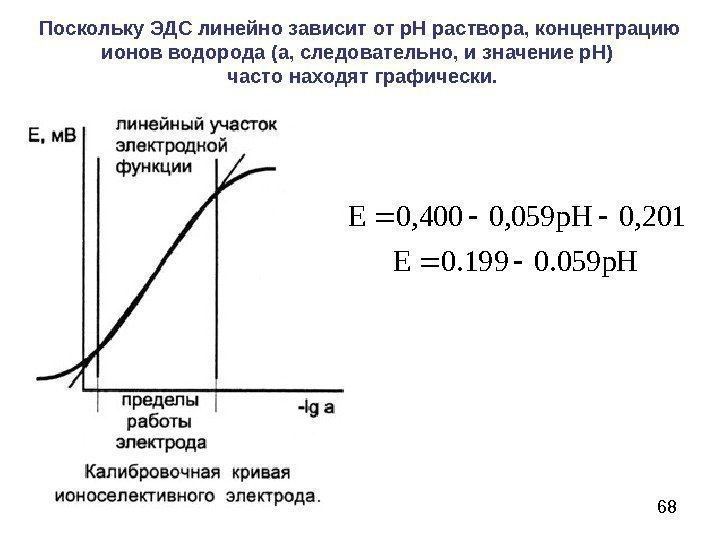
 68 р. НЕ р. НE 059. 0199. 0 201, 0059, 0400, 0 Поскольку ЭДС линейно зависит от р. Н раствора, концентрацию ионов водорода (а, следовательно, и значение р. Н) часто находят графически.
68 р. НЕ р. НE 059. 0199. 0 201, 0059, 0400, 0 Поскольку ЭДС линейно зависит от р. Н раствора, концентрацию ионов водорода (а, следовательно, и значение р. Н) часто находят графически.
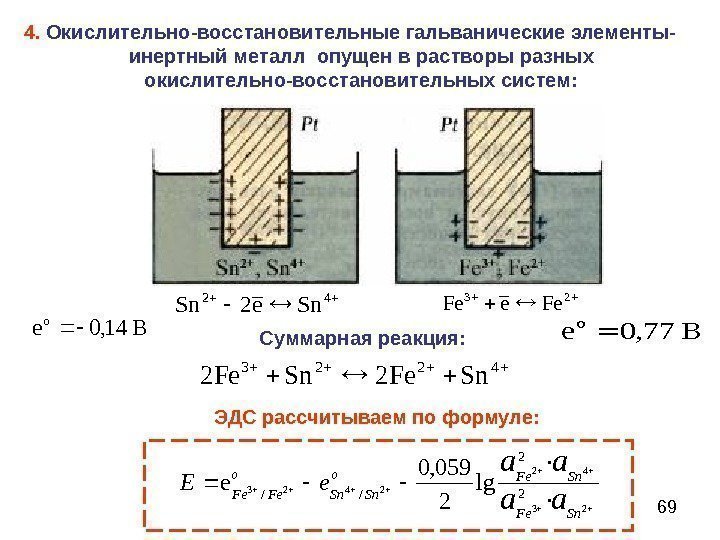
 694. Окислительно-восстановительные гальванические элементы- инертный металл опущен в растворы разных окислительно-восстановительных систем: 23 Fee. Fe 42 2 Sne. Sn В 77, 0 o е В 14, 0 o е Суммарная реакция: 4223 Sn. Fe 2 ЭДС рассчитываем по формуле: 23 42 2423 · · lg 2 059, 0 е 2 2 // Sn. Feo Sn. Sn o Fe. Feaa aa е.
694. Окислительно-восстановительные гальванические элементы- инертный металл опущен в растворы разных окислительно-восстановительных систем: 23 Fee. Fe 42 2 Sne. Sn В 77, 0 o е В 14, 0 o е Суммарная реакция: 4223 Sn. Fe 2 ЭДС рассчитываем по формуле: 23 42 2423 · · lg 2 059, 0 е 2 2 // Sn. Feo Sn. Sn o Fe. Feaa aa е.
 70 Использование ЭДС в потенциометрическом титровании Потенциометрическое титрование имеет ряд преимуществ перед титрованием с индикатором: возможность титрования мутных и окрашенных биологических жидкостей, легкость автоматизации анализа, высокая точность определения
70 Использование ЭДС в потенциометрическом титровании Потенциометрическое титрование имеет ряд преимуществ перед титрованием с индикатором: возможность титрования мутных и окрашенных биологических жидкостей, легкость автоматизации анализа, высокая точность определения
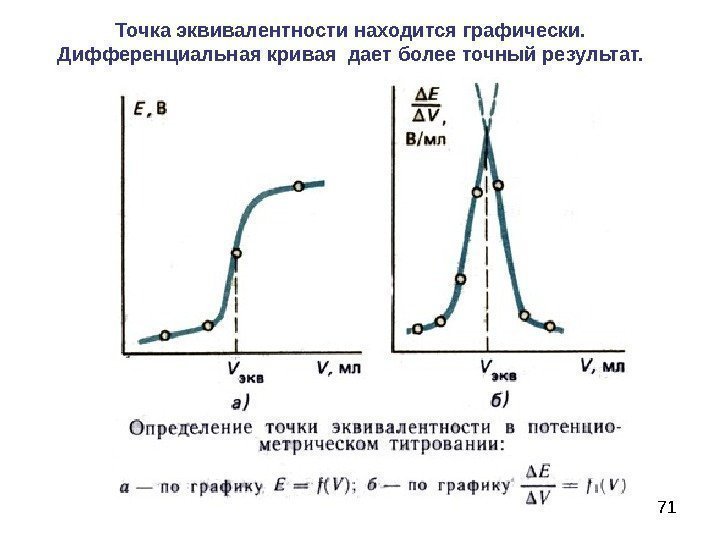
 71 Точка эквивалентности находится графически. Дифференциальная кривая дает более точный результат.
71 Точка эквивалентности находится графически. Дифференциальная кривая дает более точный результат.
 721. р. Н – метрическое — используются стеклянный и хлорсеребряный электроды p. H 059, 0199,
721. р. Н – метрическое — используются стеклянный и хлорсеребряный электроды p. H 059, 0199,
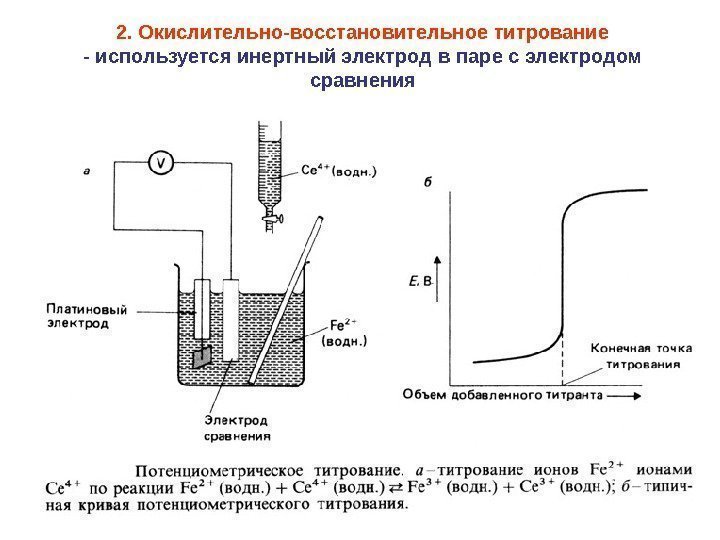
 732. Окислительно-восстановительное титрование — используется инертный электрод в паре с электродом сравнения
732. Окислительно-восстановительное титрование — используется инертный электрод в паре с электродом сравнения
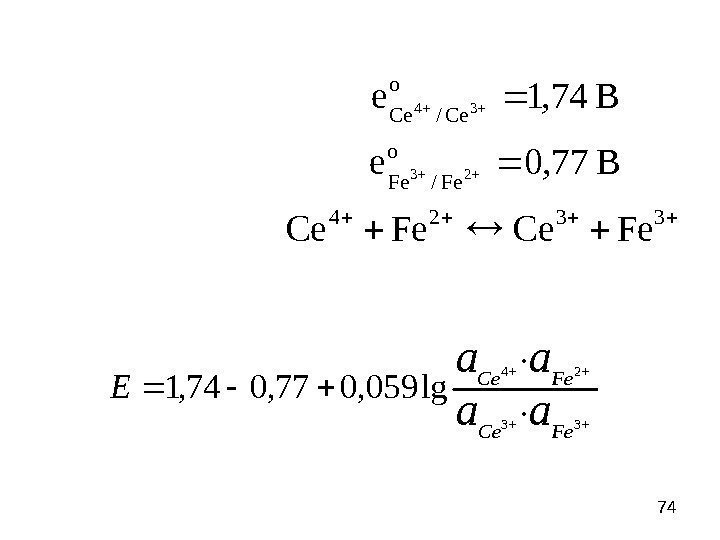 74 3324 / / 77, 0 74, 1 23 34 Fe. Ce Ве Ве o Fe. Fe o Ce. Ce 33 24 · · lg 059, 077, 074, 1 Fe. Ce aa aa
74 3324 / / 77, 0 74, 1 23 34 Fe. Ce Ве Ве o Fe. Fe o Ce. Ce 33 24 · · lg 059, 077, 074, 1 Fe. Ce aa aa
 751. Прогноз совместимости лекарственных препаратов (иодид калия и нитрит натрия, перманганат калия и тиосульфат натрия – несовместимые пары); 2. Нахождение компромиссного потенциала мышечных тканей при диагностике ишемической болезни (норма — 170 -220 м. В, снижение до 160 м. В — при болезни); 3. Использование сильных окислителей в качестве антисептических, противомикробных и дезинфицирующих средств ( йод, перманганат калия, перекись водорода, соли меди, серебра ). Значение окислительно-восстановительных процессов в организме
751. Прогноз совместимости лекарственных препаратов (иодид калия и нитрит натрия, перманганат калия и тиосульфат натрия – несовместимые пары); 2. Нахождение компромиссного потенциала мышечных тканей при диагностике ишемической болезни (норма — 170 -220 м. В, снижение до 160 м. В — при болезни); 3. Использование сильных окислителей в качестве антисептических, противомикробных и дезинфицирующих средств ( йод, перманганат калия, перекись водорода, соли меди, серебра ). Значение окислительно-восстановительных процессов в организме
 76 Тиосульфат натрия Na 2 S 2 O 3 – универсальный антидот!!! а) При отравлении тяжелыми металлами образуются трудно растворимые и поэтому практически неядовитые сульфиты: Р b (СН 3 СОО) 2 + Na 2 S 2 O 3 + Н 2 О → Pb. S + Na 2 SO 4 + 2 СН 3 СООН б) При отравлении синильной кислотой или цианидами тиосульфат превращает эти токсичные вещества в менее ядовитые роданистые соединения, : HCN+ Na 2 S 2 O 3 → Na. CNS + Na. HSO 3 ; KCN + Na 2 S 2 O 3 → KCNS + Na 2 SO 3. 4. Разрушение токсических веществ, образующихся в ходе метаболизма
76 Тиосульфат натрия Na 2 S 2 O 3 – универсальный антидот!!! а) При отравлении тяжелыми металлами образуются трудно растворимые и поэтому практически неядовитые сульфиты: Р b (СН 3 СОО) 2 + Na 2 S 2 O 3 + Н 2 О → Pb. S + Na 2 SO 4 + 2 СН 3 СООН б) При отравлении синильной кислотой или цианидами тиосульфат превращает эти токсичные вещества в менее ядовитые роданистые соединения, : HCN+ Na 2 S 2 O 3 → Na. CNS + Na. HSO 3 ; KCN + Na 2 S 2 O 3 → KCNS + Na 2 SO 3. 4. Разрушение токсических веществ, образующихся в ходе метаболизма
 77 в) При отравлении галогенами и другими сильными окислителями антитоксическое действие Na 2 S 2 O 3 обусловлено его умеренными восстановительными свойствами: С l 2 + Na 2 S 2 O 3 + Н 2 О → 2 НС l + S + Na 2 SO 4 ; 4 Cl 2 + Na 2 S 2 O 3 + 5 Н 2 О → 8 HCl + 2 Na. HSO 4.
77 в) При отравлении галогенами и другими сильными окислителями антитоксическое действие Na 2 S 2 O 3 обусловлено его умеренными восстановительными свойствами: С l 2 + Na 2 S 2 O 3 + Н 2 О → 2 НС l + S + Na 2 SO 4 ; 4 Cl 2 + Na 2 S 2 O 3 + 5 Н 2 О → 8 HCl + 2 Na. HSO 4.
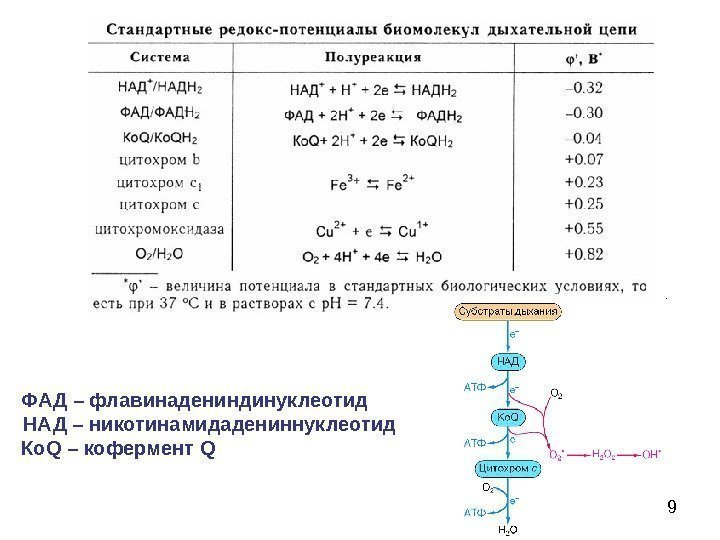
 78 5. Расчет потенциалов в схеме дыхательной цепи В основе процесса дыхания лежит экзэргоническая окислительно-восстановительная реакция О 2 (г) + 4 Н + + 4 е – → 2 Н 2 О(ж). При р. Н 7, 0 ° = 0, 815 В, Δ G 298 = – 457, 52 к. Дж на 1 моль О 2. В биологических системах данная реакция никогда не осуществляется непосредственно, а реализуется через целый ряд промежуточных превращений, каждое из них требует участия определенного фермента.
78 5. Расчет потенциалов в схеме дыхательной цепи В основе процесса дыхания лежит экзэргоническая окислительно-восстановительная реакция О 2 (г) + 4 Н + + 4 е – → 2 Н 2 О(ж). При р. Н 7, 0 ° = 0, 815 В, Δ G 298 = – 457, 52 к. Дж на 1 моль О 2. В биологических системах данная реакция никогда не осуществляется непосредственно, а реализуется через целый ряд промежуточных превращений, каждое из них требует участия определенного фермента.
 79 ФАД – флавинадениндинуклеотид НАД – никотинамидадениннуклеотид Ко Q – кофермент Q
79 ФАД – флавинадениндинуклеотид НАД – никотинамидадениннуклеотид Ко Q – кофермент Q
 80 Значение ионометрии 1. Контроль водно-электролитного баланса и кислотно-щелочного состояния организма и его отдельных органов
80 Значение ионометрии 1. Контроль водно-электролитного баланса и кислотно-щелочного состояния организма и его отдельных органов
 812. Определение состава лекарственных препаратов, ферментов, физиологических растворов, продуктов питания, почв, природных вод, атмосферы.
812. Определение состава лекарственных препаратов, ферментов, физиологических растворов, продуктов питания, почв, природных вод, атмосферы.
 82 3. Определение кислотности желудочного сока путем введения в желудок больного капсулы с двумя миниатюрными электродами-стеклянного и хлорсеребряного
82 3. Определение кислотности желудочного сока путем введения в желудок больного капсулы с двумя миниатюрными электродами-стеклянного и хлорсеребряного
 834. Непрерывный контроль кислотности во время хирургических операций.
834. Непрерывный контроль кислотности во время хирургических операций.
 845. Диагностика ряда кожных заболеваний
845. Диагностика ряда кожных заболеваний
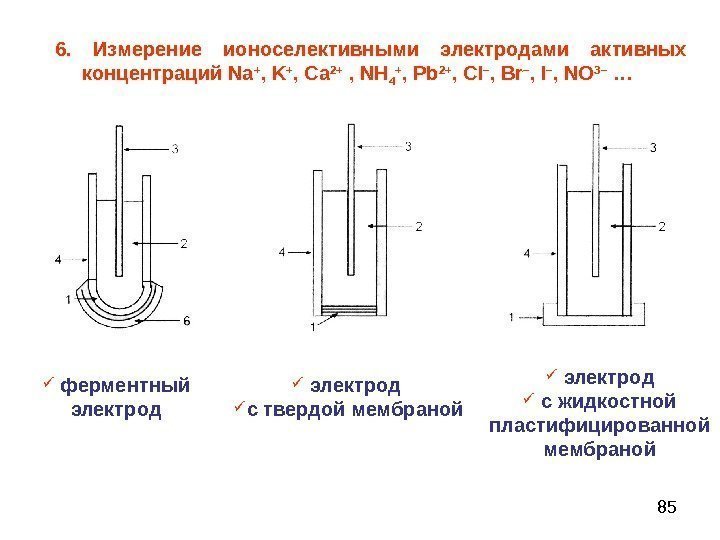
 856. Измерение ионоселективными электродами активных концентраций Na + , K + , Ca 2+ , NH 4 + , Pb 2+ , С l – , Br – , I – , NO 3– … ферментный электрод с жидкостной пластифицированной мембраной электрод с твердой мембраной
856. Измерение ионоселективными электродами активных концентраций Na + , K + , Ca 2+ , NH 4 + , Pb 2+ , С l – , Br – , I – , NO 3– … ферментный электрод с жидкостной пластифицированной мембраной электрод с твердой мембраной
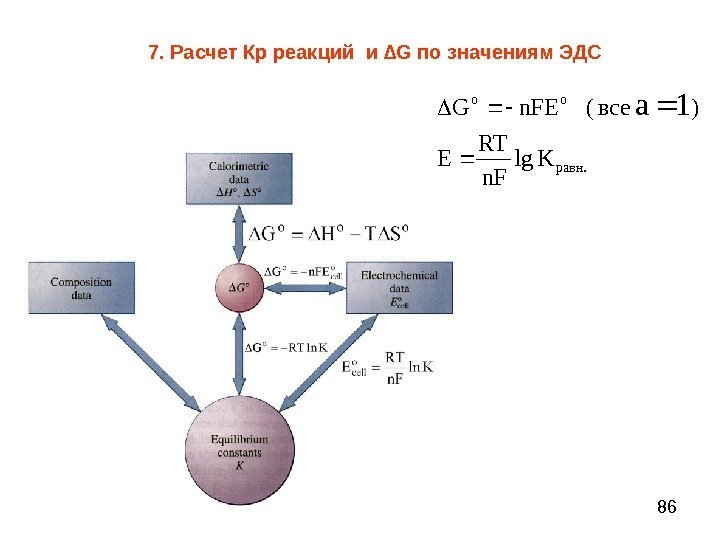
 867. Расчет Кр реакций и ∆ G по значениям ЭДС. равн oo Klg n. F RT E ) все ( n. FEG 1 a
867. Расчет Кр реакций и ∆ G по значениям ЭДС. равн oo Klg n. F RT E ) все ( n. FEG 1 a
 87 Оптимальные диапазоны р. Н для выращивания : Картофель — 4. 8– 5. 7 Рожь — 5. 0 -6. 0 Репа — 5. 8 -6. 8 Ячмень — 7. 0 -7. 5 Сахарная свекла — 7. 0 -7. 5 Пшеница — 6. 5 -7. 58. Контроль за р. Н почв
87 Оптимальные диапазоны р. Н для выращивания : Картофель — 4. 8– 5. 7 Рожь — 5. 0 -6. 0 Репа — 5. 8 -6. 8 Ячмень — 7. 0 -7. 5 Сахарная свекла — 7. 0 -7. 5 Пшеница — 6. 5 -7. 58. Контроль за р. Н почв
 88 Спасибо за внимание!
88 Спасибо за внимание!

