03.05.2017 Русецкая О.П. 1 Проектная работа: Электролитическая диссоциация


03.05.2017 Русецкая О.П. 1 Проектная работа: Электролитическая диссоциация ИКТ фестиваль учителей химии Автор работы Русецкая О.П. учитель химии высшей категории МОУ СОШ № 7 г.Ноябрьска

03.05.2017 Русецкая О.П. 2 Электролитическая диссоциация
03.05.2017 Русецкая О.П. 3 1 1. Рис.1 Электролиты Неэлектролиты
03.05.2017 «Капля воды и камень точит» 4 1. Электролиты и неэлектролиты Вода – хороший растворитель, т.к. молекулы воды полярны. слабый амфотерный электролит. ион гидроксония Ионное произведение воды КН2О = [Н+]•[ОН-] = 10-7•10-7 = 10-14 (КН2О) Вода – Механизм ЭД
03.05.2017 Русецкая О.П. 5 1. Электролиты и неэлектролиты это вещества, растворы и расплавы которых проводят электрический ток. Электролиты -

+ + + + - - - - Анионы Катионы Анод Катод - + 03.05.2017 6 Русецкая О.П. Электролиты Рис.2.

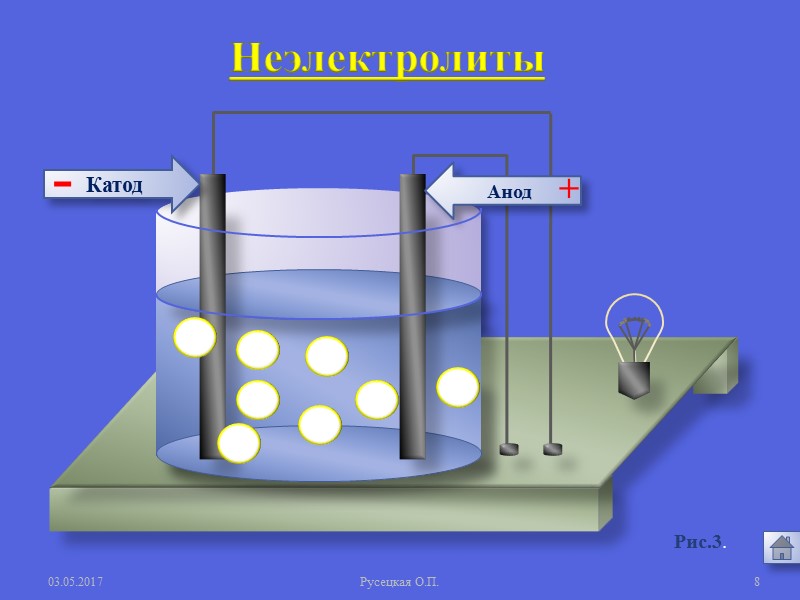
03.05.2017 Русецкая О.П. 7 1. Электролиты и неэлектролиты это вещества, растворы или расплавы которых не проводят электрический ток. Неэлектролиты - Органические вещества: сахар, ацетон,бензин, керосин, глицерин, этиловый спирт, бензол и др. Газы: кислород, водород, азот идр.
Анод Катод - + 03.05.2017 8 Русецкая О.П. Рис.3. Неэлектролиты

03.05.2017 «Честь науке- ей дано уменье, выводить нас из заблужденья». М.Светлов 9 2.Электролитическая диссоциация процесс распада молекул электролита на ионы в растворе или расплаве. С.Аррениус Электролитическая диссоциация - Теория электролитической диссоциации. 1887 г.

03.05.2017 «Честь науке- ей дано уменье, выводить нас из заблужденья». М.Светлов 10 2.Электролитическая диссоциация Аррениус Сванте Август Шведский ученый, академик. В 1887 году сформулировал основные положения теории электролитической диссоциации. В 1903 г. награжден Нобелевской премией. Проводил исследования во многих других областях науки. С.Аррениус (1859 – 1927)

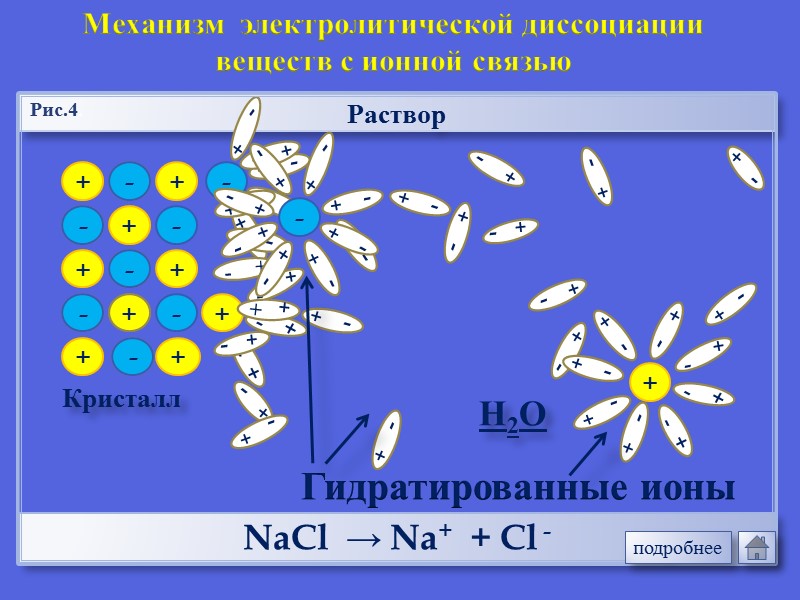
+ + - - + + - - Раствор Кристалл - + + + - - + + - - - + NaCl → Na+ + Cl - Механизм электролитической диссоциации веществ с ионной связью Гидратированные ионы Н2О Рис.4. подробнее

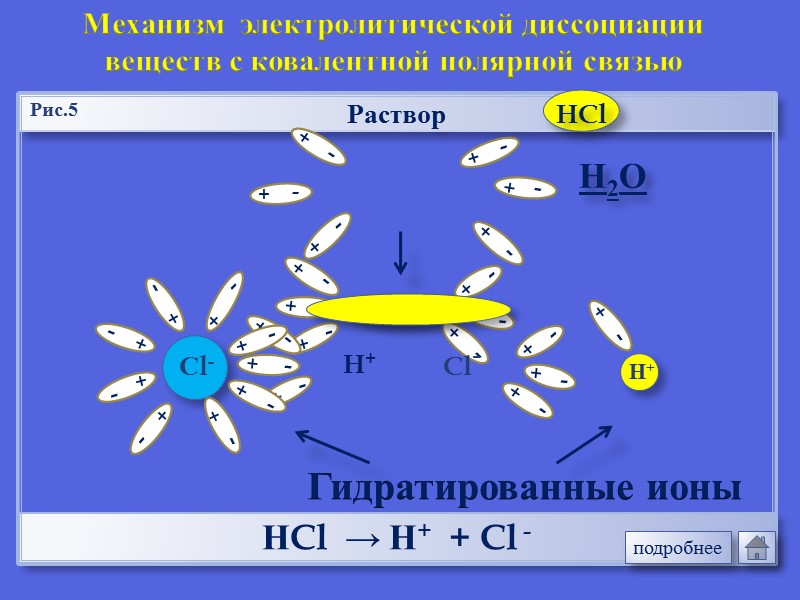
Раствор НCl → Н+ + Cl - Механизм электролитической диссоциации веществ с ковалентной полярной связью Н2О Рис.5. Гидратированные ионы подробнее

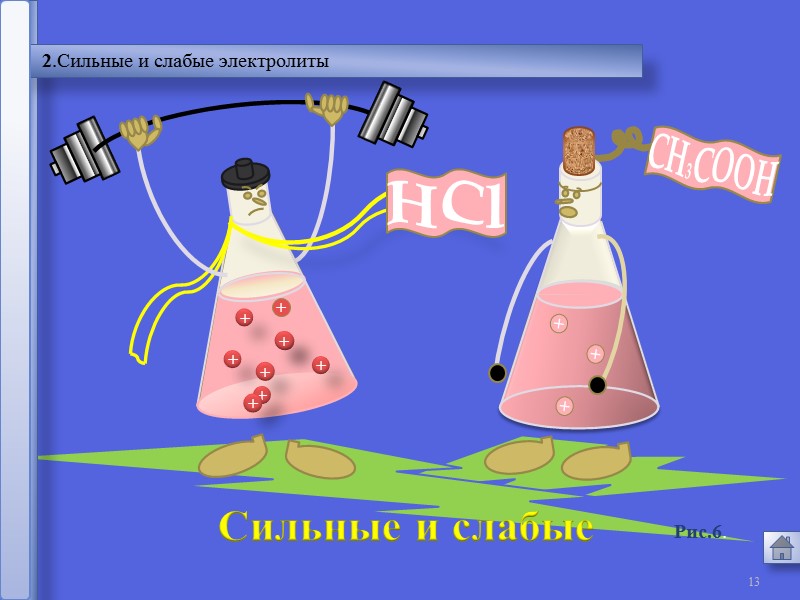
13 2.Сильные и слабые электролиты HCl + + + Сильные и слабые Рис.6.

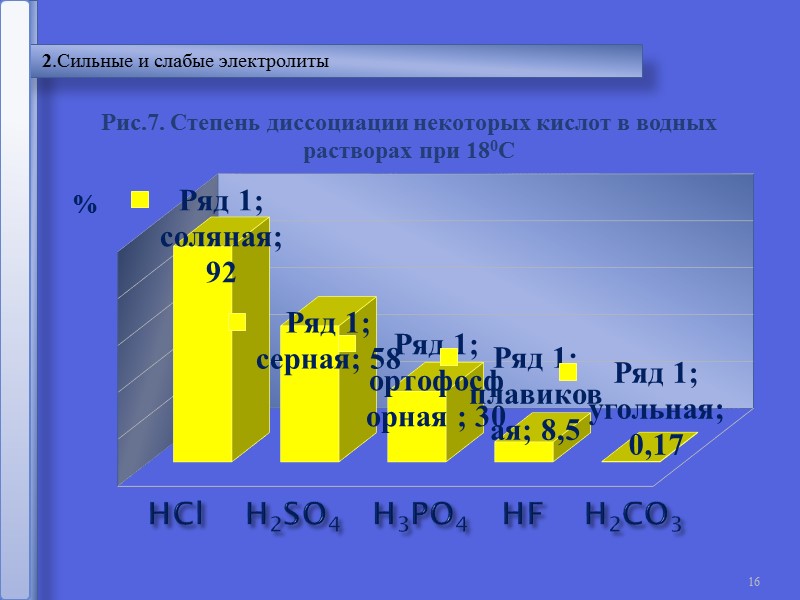
03.05.2017 Русецкая О.П. 14 отношение числа диссоциированных молекул к общему числу молекул, находящихся в растворе. Степень электролитической диссоциации (α) - α = n N Сильные электролиты α > 30% Слабые электролиты α< 30%
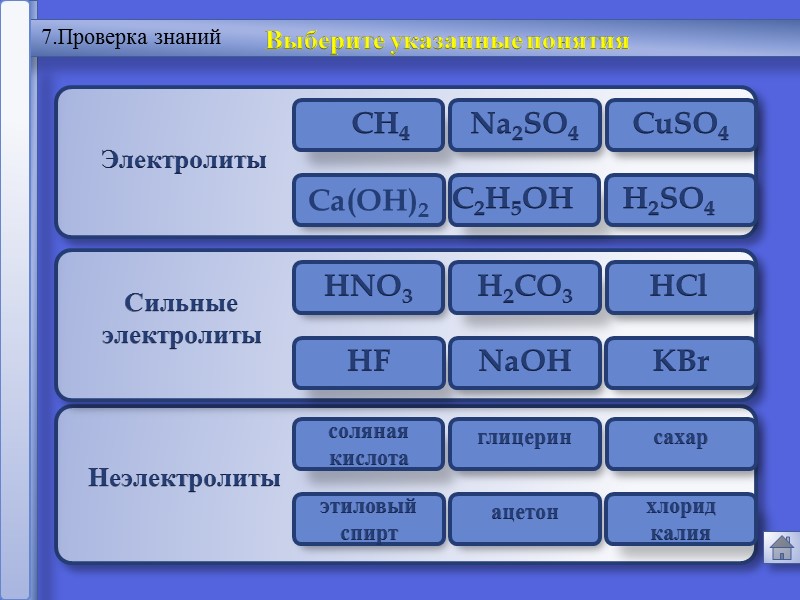
2.Сильные и слабые электролиты Электролиты

16 2.Сильные и слабые электролиты %

03.05.2017 Русецкая О.П. 17 это сложные вещества, при диссоциации которых в водных растворах в качестве катионов отщепляются только ионы водорода. Кислоты - Диссоциация кислот НCl → + Cl - Н2SO4 → 2 + SO4 2- Н2 CO3 2 + CO3 2- Н+ Н+ Н+ 5. Диссоциация кислот, оснований, солей

03.05.2017 Русецкая О.П. 18 это сложные вещества, при диссоциации которых в водных растворах в качестве анионов отщепляются только гидроксид-ионы. Основания - Диссоциация оснований KOH → K + + OН- Ca(OH)2 Ca2+ + 2 Мe(OH)n Men+ + n OН- OН-
03.05.2017 Русецкая О.П. 19 это сложные вещества, которые в водных растворах диссоциируют на катионы металла и анионы кислотного остатка. Соли - Диссоциация солей NaCl → + K2SO4 → 2 + Al(NO3)3 → + 3 Na+ K+ Al3+ (кислотный остаток)в- NO3 - Сl- SO4 2-

20 6. О значении электролитов для живых организмов Электролитическая диссоциация Электролиты – составная часть жидкостей и плотных тканей живых организмов. Ионы Na+,K+,Ca2+,Mg2+,H+; OH-; Cl-; SO4-2; имеют большое значение для физиологических и биохимических процессов: ионы H+; OH- играют большую роль в работе ферментов, обмене веществ, переваривании пищи и др. при нарушении водно-солевого обмена в медицине применяется физиологический раствор – 0,85% раствор NaCl; ионы I - влияют на работу щитовидной железы. НCO3-

21 6. Рис.8. Характерные симптомы дефицита химических элементов в организме человека подробнее
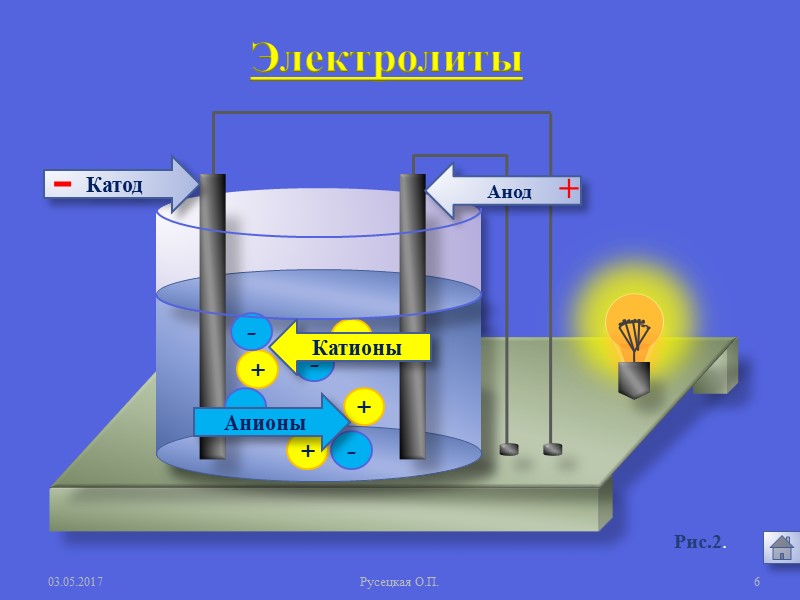
Ошибка Молодец Молодец Ошибка Молодец Молодец Сильные электролиты Ca(OH)2 Электролиты Неэлектролиты 7.Проверка знаний Выберите указанные понятия

03.05.2017 Русецкая О.П. 23 Электролитическая диссоциация 7. Проверка знаний 03.05.2017 Русецкая О.П. 23 Электролитическая диссоциация в растворах – это процесс распада электролита на __________ . Вопрос 1 03.05.2017 Русецкая О.П. 23 Электролитическая диссоциация электролитов в растворах протекает под действием __________ . Вопрос 2 03.05.2017 Русецкая О.П. 23 Слабым электролитом является _______ . Вопрос 3 03.05.2017 Русецкая О.П. 23 Электролитами не являются ________ . Вопрос 4 03.05.2017 Русецкая О.П. 23 Основные положения электролитической диссоциации сформулировал ученый ______. Вопрос 5
03.05.2017 24 03.05.2017 24 03.05.2017 24 03.05.2017 24 03.05.2017 24 03.05.2017 24 Механизм электролитической диссоциации NaCl Разрушение кристаллической решетки под действием молекул воды. Гидратация NaCl + nН2О →Na+ (Н2О)х + Сl-(Н2О)n-х NaCl → Na+ + Cl - HCl Поляризация связи в молекуле НСl под действием молекул воды. Гидратация HCl + nН2О →H+ (Н2О)х + Сl-(Н2О)n-х НCl → Н+ + Cl - Механизм ЭД Механизм ЭД

03.05.2017 25 03.05.2017 25 03.05.2017 25 03.05.2017 25 03.05.2017 25 03.05.2017 25 Литература Баженов А.А. Мастер-класс «Создание презентаций к урокам химии». Сеть творческих учителей. http://www.it-ru/communities.aspx?cat_no=75761&tmpl=com Рудзитис Г.Е., Фельдман Ф.Г. Химия. 8 кл. – М.: Просвещение, 2008. Мартыненко Б.В. Химия: кислоты и основания. – М.: Просвещение, 2000. Слета Л.А. Химия: Справочник. – Харьков: Фолио, 1997. Егоров А.С. Химия. Пособие –репетитор для поступающих в вузы. – Ростов н/Д: изд-во Феникс, 2006. Гаршин А.П.Неорганическая химия. – СПб.: изд-во «Лань», 2000. http://www.alhimik.ru/kunst/man's_elem.html Благодарю за внимание!
37-elektroliticheskaya_dissociaciya.pptx
- Количество слайдов: 25

